Clear Sky Science · es
Base estructural para la inversión de horquilla y la regulación de RAD51 por el complejo ubiquitina-ligasa SCF de la helicasa F-box 1
Cómo las células rescatan una máquina de copia del ADN atascada
Cada vez que una célula se divide, debe copiar miles de millones de letras de ADN de forma rápida y precisa. Pero esta maquinaria de copiado con frecuencia encuentra problemas: daños en el ADN, secuencias difíciles de copiar o tratamientos farmacológicos pueden hacer que el proceso se detenga. Cuando eso ocurre, las células dependen de equipos de reparación de emergencia para estabilizar y reiniciar las horquillas de replicación. Este artículo revela, con un detalle estructural sin precedentes, cómo uno de esos jefes de equipo —un complejo proteico centrado en la helicasa FBH1— remodela el ADN atascado y mantiene bajo control a otra proteína clave de reparación, RAD51. Comprender esta coreografía ayuda a explicar cómo las células evitan roturas genómicas peligrosas y por qué las alteraciones en estos factores se asocian al cáncer.
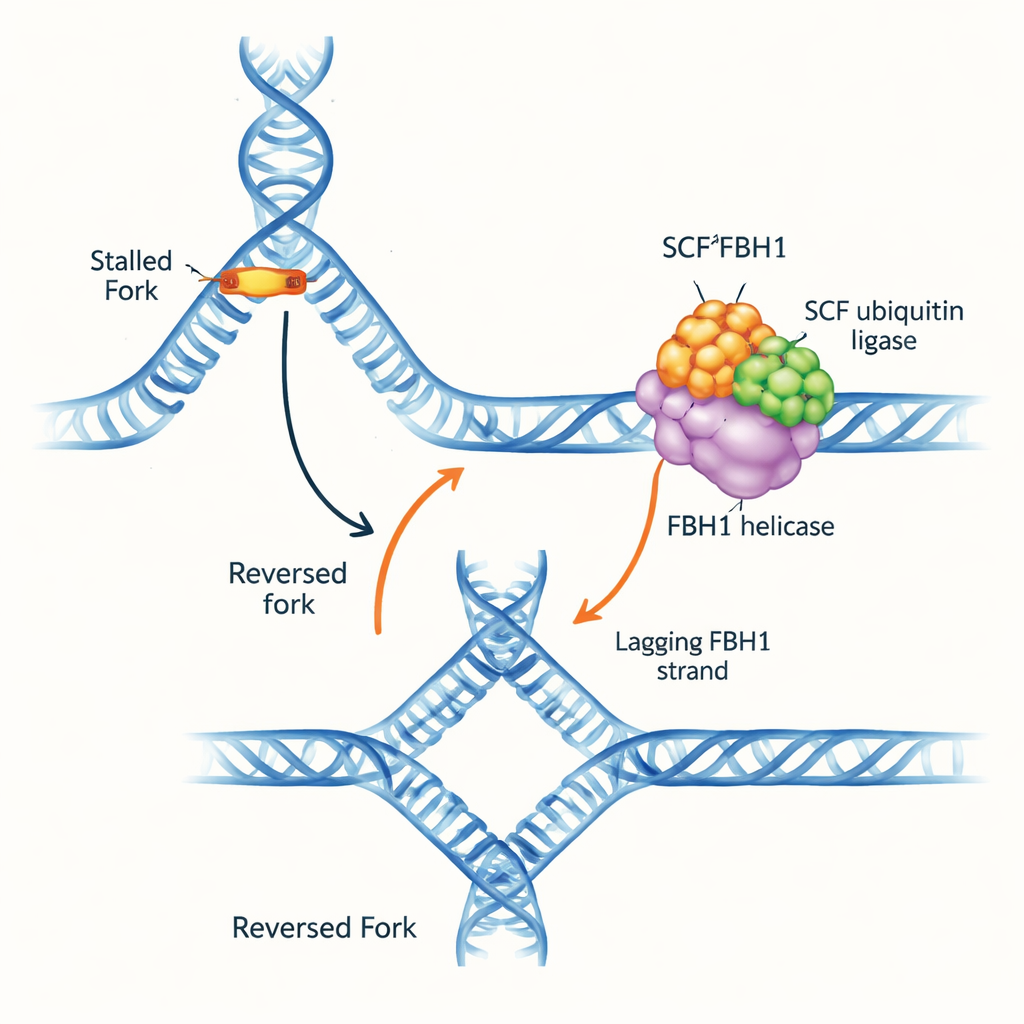
Un atasco en la autopista del ADN
Las horquillas de replicación del ADN son estructuras en forma de Y donde la doble hélice se desenrolla y se copia. Cuando la horquilla encuentra obstáculos, puede invertir la dirección: las cadenas parentales vuelven a aparearse y las cadenas recién sintetizadas se emparejan entre sí, formando una unión de ADN de cuatro vías. Esta “inversión de horquilla” puede ganar tiempo para reparar el daño y reiniciar la replicación con seguridad, pero si se maneja mal también genera ADN frágil que puede romperse. Se conocen varios motores moleculares que empujan las horquillas hacia atrás agarrando el ADN de doble cadena por delante de la horquilla. Sin embargo, FBH1 destacó porque se comporta de forma distinta y con frecuencia está alterado en tumores, lo que sugiere que opera mediante una vía diferente y de importancia médica.
Un especialista en horquillas con preferencia por un lado
Los autores purificaron el complejo humano SCFFBH1, que combina la helicasa FBH1 con un módulo de etiquetado por ubiquitina (SCF). Primero investigaron qué formas de ADN prefiere FBH1. Usando ensayos de unión y desenrollamiento, demostraron que SCFFBH1 favorece con fuerza estructuras que realmente se parecen a horquillas, especialmente donde hay un tramo corto de ADN monocatenario en la hebra molde “rezagada”, el lado que se copia en fragmentos pequeños. En estas estructuras, FBH1 desenrolla el ADN cientos de veces más rápido que en un extremo suelto simple, lo que indica que el enganche correcto en la unión de la horquilla aumenta enormemente su actividad motora. Experimentos con pinzas magnéticas a molécula única confirmaron que el complejo puede desenrollar y luego desplazarse a lo largo de ADN monocatenario durante miles de bases sin desprenderse, comportándose como un motor potente y procesivo.
Invertir la horquilla tirando desde atrás
Para averiguar cómo este motor invierte realmente las horquillas, el equipo probó sustratos de horquilla artificiales con o sin huecos monocatenarios. A diferencia de otros remodeladores de horquillas, SCFFBH1 no pudo actuar sobre una horquilla totalmente apareada; requería un hueco en la hebra rezagada y se movía en dirección 3′–5′ a lo largo de esa hebra simple. Este movimiento de “tirar desde atrás” impulsa a las cadenas parentales a volver a aparearse mientras la enzima permanece clavada en la unión de la horquilla. Una estructura por criomicroscopía electrónica de SCFFBH1 unido a una horquilla estancada muestra cómo ocurre esto: un parche cargado positivamente especial, un “motivo de unión a la unión” en un subdominio de FBH1, se sitúa justo en el punto de ramificación donde se encuentran los tres brazos de ADN. Cuando los investigadores mutaron dos aminoácidos clave en este motivo, la inversión de horquilla cayó alrededor de 25 veces en ensayos in vitro, aunque el motor básico de desenrollamiento seguía funcionando razonablemente bien. En células, la misma mutación impidió la desaceleración normal de las horquillas de replicación en respuesta a un fármaco que induce estrés, un sello distintivo de la falla en invertir horquillas.
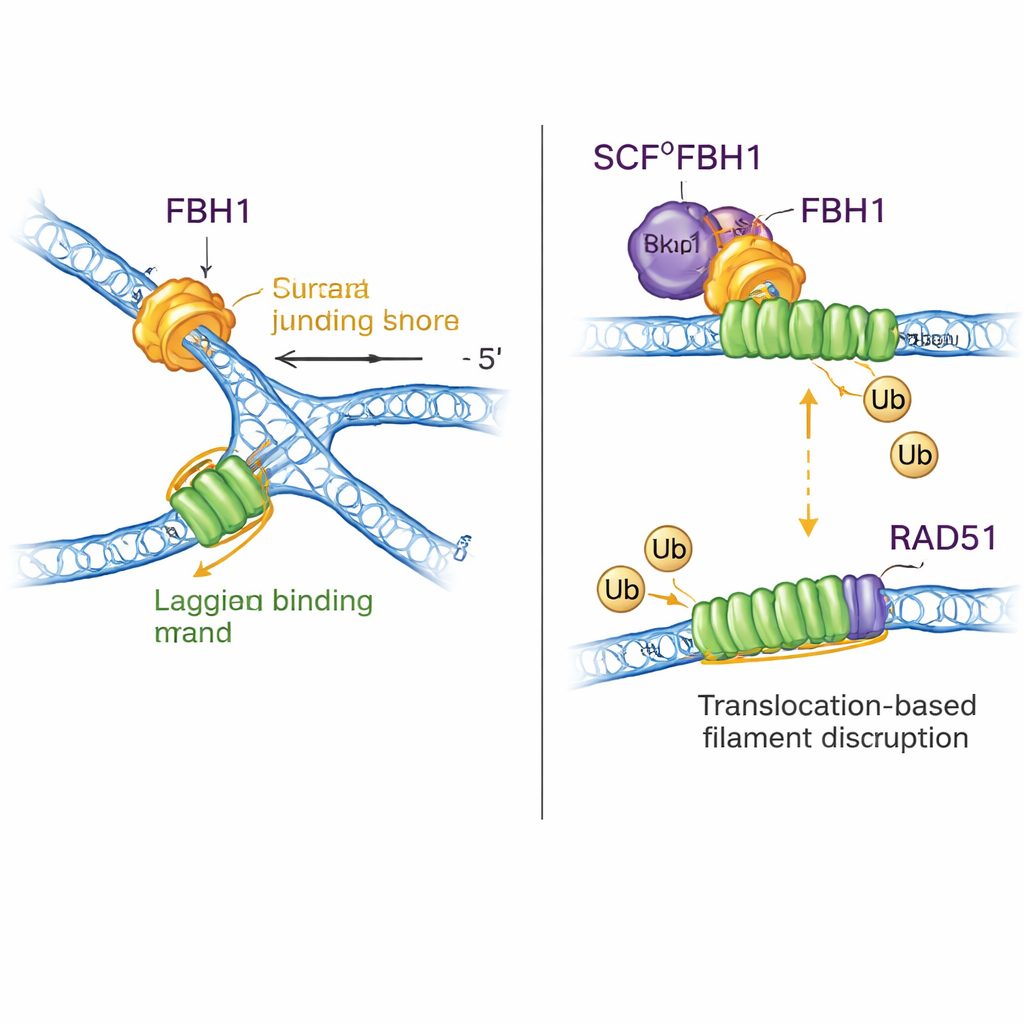
Un doble papel: remodelar el ADN y eliminar RAD51
FBH1 no es solo un motor; a través del complejo SCF también ayuda a unir pequeñas etiquetas de ubiquitina a proteínas. Las nuevas estructuras ensamblan casi todo el complejo SCFFBH1–ADN y muestran que la “cabeza” de transferencia de ubiquitina de la ligasa se sitúa a menos de 45 Å de la hebra rezagada que emerge de FBH1. Sobre la base de acoplamientos con estructuras conocidas de otras ubiquitina-ligasas, los autores proponen que esta geometría posiciona a RAD51 —una enzima que forma filamentos sobre el ADN para promover recombinación— justo en la línea de fuego sobre la hebra rezagada de una horquilla estancada. Trabajos previos mostraron que FBH1 puede arrancar mecánicamente a RAD51 del ADN y también marcarlo con ubiquitina para que no se vuelva a unir con facilidad. El nuevo modelo unifica estas ideas: mientras FBH1 tira a lo largo de la hebra rezagada para remodelar la horquilla, el módulo SCF cercano puede etiquetar subunidades de RAD51, ayudando a desmantelar o prevenir filamentos excesivos de RAD51 que podrían bloquear un procesamiento correcto de la horquilla.
Qué significa esto para la estabilidad del genoma y el cáncer
En conjunto, el estudio muestra que SCFFBH1 invierte horquillas de replicación estancadas mediante un mecanismo distinto del de otros remodeladores conocidos: agarra firmemente el punto de ramificación mientras se transloca por la hebra molde rezagada desde atrás, promoviendo el reapareamiento seguro del ADN parental sin formar una unión de cuatro vías móvil y de larga vida. Al mismo tiempo, su ligasa de ubiquitina integrada está estratégicamente posicionada para eliminar RAD51 de esa misma hebra, evitando recombinación descontrolada durante el estrés de replicación. Dado que FBH1 se pierde o muta con frecuencia en cánceres, estos conocimientos estructurales y mecanísticos ayudan a explicar cómo esos tumores acumulan daño en el ADN y por qué pueden responder de forma distinta a fármacos que provocan estrés de replicación o que atacan vías relacionadas.
Cita: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
Palabras clave: estrés durante la replicación del ADN, inversión de horquilla, helicasa FBH1, regulación de RAD51, estabilidad genómica