Clear Sky Science · es
Mapeo automatizado de la progresión de la horquilla de replicación del ADN en células humanas con ForkML
Por qué importa rastrear la velocidad de copia del ADN
Cada vez que una célula humana se divide, debe copiar más de tres mil millones de letras de ADN de forma rápida y precisa. Si este proceso de copia se ralentiza o se detiene, puede dañar el genoma y contribuir al cáncer y a trastornos del desarrollo. Sin embargo, hasta ahora los científicos no disponían de una manera sencilla de ver exactamente a qué velocidad se desplazan las «máquinas de copia» individuales a lo largo de tramos concretos del ADN humano. Este artículo presenta ForkML, una nueva técnica que utiliza la secuenciación por nanoporo y el aprendizaje automático para automatizar esta tarea a una escala sin precedentes.
Viendo las máquinas de copia de la célula en tiempo casi real
El ADN se duplica mediante diminutas máquinas moleculares llamadas horquillas de replicación que avanzan por la doble hélice formando nuevas hebras. ForkML permite a los investigadores observar estas horquillas de forma indirecta añadiendo una etiqueta química inofensiva, BrdU, al ADN recién sintetizado durante dos pulsos muy cortos separados por un intervalo fijo. Dado que la BrdU puede detectarse en moléculas individuales de ADN mediante secuenciadores por nanoporo, los científicos ven dos «franjas» etiquetadas en cada hebra donde pasó una horquilla durante los dos pulsos. Midiendo la distancia entre las franjas y dividiéndola por el tiempo conocido entre pulsos, pueden calcular la velocidad a la que avanzó cada horquilla en esa región del genoma. 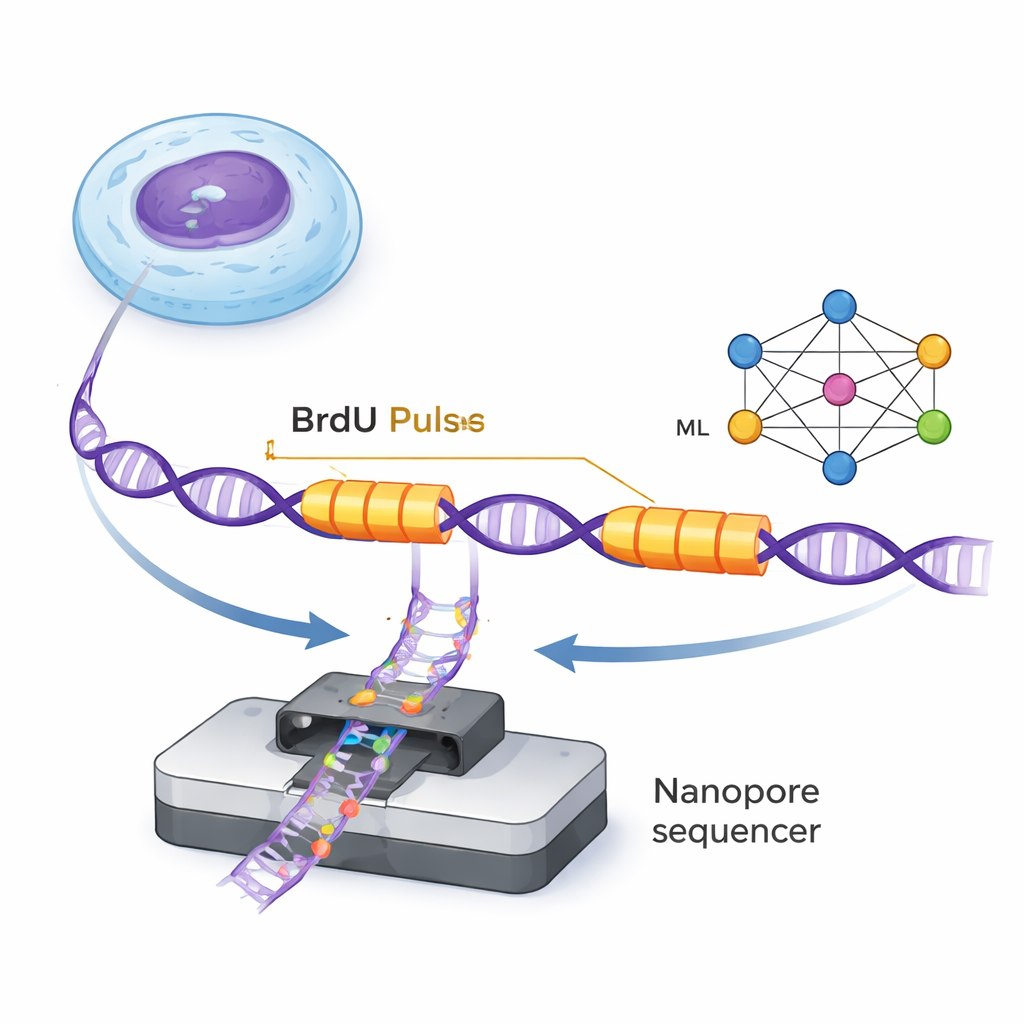
Enseñar a un ordenador a leer las huellas químicas
En trabajos anteriores con levadura, los autores podían detectar estas marcas de BrdU usando reglas sencillas, pero en células humanas las señales son más débiles y complejas. Los expertos humanos aún pueden reconocer el patrón característico—un aumento brusco de BrdU al inicio del pulso, seguido de un descenso gradual cuando se elimina—pero hacerlo a mano para millones de fragmentos de ADN es imposible. ForkML resuelve esto entrenando una red neuronal, una forma de aprendizaje automático, con miles de ejemplos anotados manualmente. El modelo aprende a clasificar cada tramo de ADN como fondo o como una horquilla que se mueve hacia la derecha o hacia la izquierda, y a localizar con alta precisión el inicio de cada pulso de BrdU. Esto permite el mapeo completamente automatizado de miles de velocidades de horquilla individuales a partir de una sola corrida de secuenciación.
Medir el estrés y las diferencias a lo largo del genoma
Aplicando ForkML a una línea celular humana de cáncer colorrectal, el equipo obtuvo más de 2.000 mediciones de velocidad de horquilla por experimento y encontró que la horquilla típica se mueve a aproximadamente 1,2 kilobases por minuto, consistente con métodos anteriores de menor rendimiento. Cuando trataron las células con fármacos conocidos por ralentizar la replicación del ADN, ForkML detectó claramente la desaceleración, demostrando que puede medir con sensibilidad el estrés de replicación. Como cada horquilla se asigna de nuevo a su posición en el genoma de referencia, los autores pudieron relacionar la velocidad con otras características, como cuándo se replica una región durante el ciclo celular, qué tan compactado está su ADN y cuán activamente se transcribe a ARN. 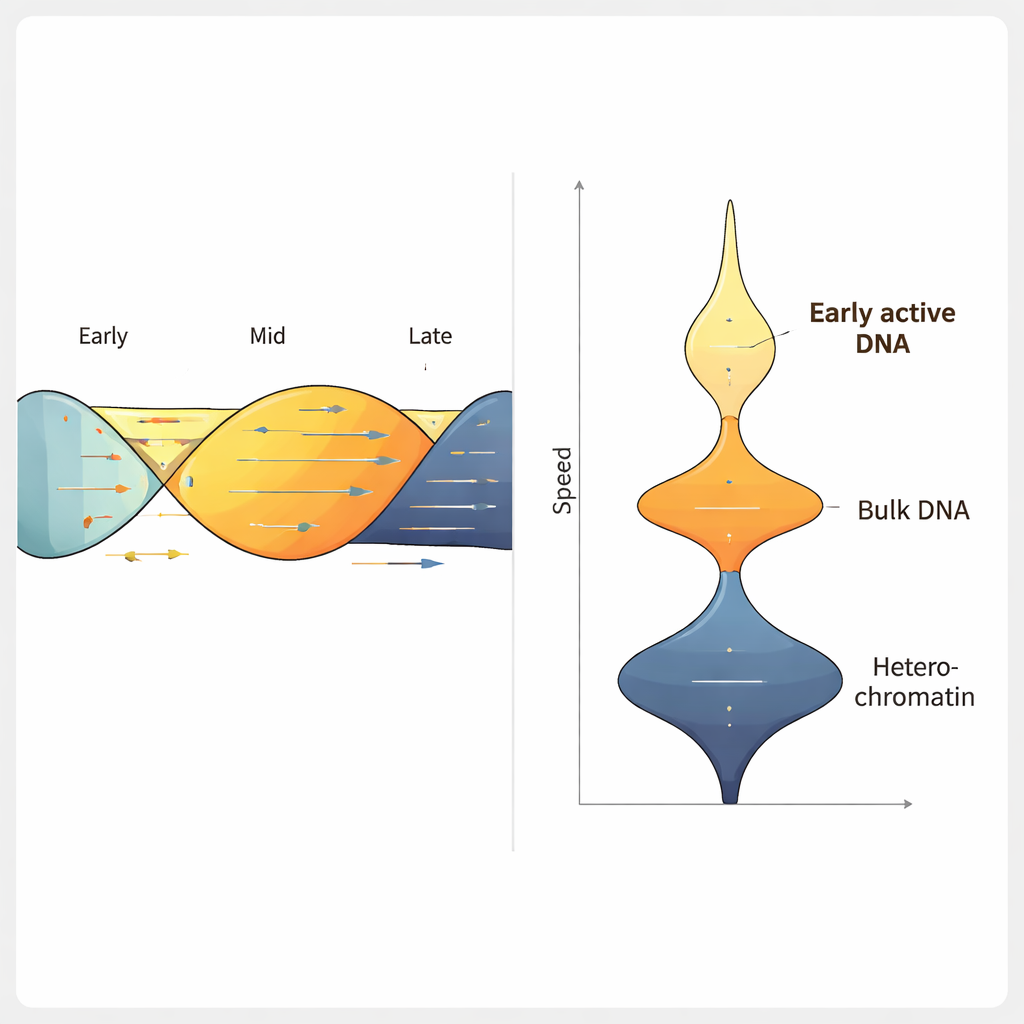
Revelar dónde comienza la copia del ADN y cómo difieren las hebras
Más allá de la velocidad, ForkML también identifica dónde comienza y termina la replicación del ADN, detectando puntos donde las horquillas divergen o convergen a lo largo de la misma molécula. Al mapear más de 20.000 de estos sitios de inicio, los autores confirman que las células humanas usan una estrategia mixta: algunos inicios de replicación ocurren en zonas de iniciación bien definidas, pero la mayoría de los inicios están dispersos por el genoma. Al combinar la dirección de la horquilla con qué hebra de ADN fue leída por el secuenciador, ForkML también puede distinguir las velocidades de síntesis de la hebra líder y la retardada, algo que los ensayos clásicos basados en fibras no pueden hacer. Pruebas en seis líneas celulares humanas diferentes—tanto normales como cancerosas—muestran que las mismas condiciones sencillas de marcado con BrdU son ampliamente aplicables y proporcionan estimaciones de velocidad robustas en cada caso.
Una actualización digital de una técnica clásica
Para los no especialistas, ForkML puede verse como una versión moderna y digital del clásico ensayo de fibras de ADN: emplea un esquema de marcado similar, pero reemplaza la microscopía manual por secuenciación de lecturas largas y aprendizaje automático. Esto aporta un rendimiento mucho mayor, la colocación directa de cada medida en el genoma y más información detallada sobre dónde y con qué rapidez se copia el ADN. Dado que el protocolo es sencillo, compatible con el hardware de nanoporo actual y adaptable a otros organismos, ForkML está listo para convertirse en una herramienta estándar para estudiar la replicación del ADN. En términos prácticos, ofrece a los investigadores una forma potente de relacionar la velocidad local de copia del ADN—normal o bajo estrés—con la actividad génica, el estado de la cromatina y los cambios del genoma relacionados con enfermedades.
Cita: Rojat, V., Ciardo, D., Tourancheau, A. et al. Automated mapping of DNA replication fork progression in human cells with ForkML. Nat Commun 17, 1975 (2026). https://doi.org/10.1038/s41467-026-68750-4
Palabras clave: Replicación del ADN, velocidad de la horquilla de replicación, secuenciación por nanoporo, marcado con BrdU, aprendizaje automático en genómica