Clear Sky Science · es
Un atlas proteogenómico de 1.032 metástasis cerebrales identifica subtipos moleculares, paisajes inmunitarios y vulnerabilidades terapéuticas
Por qué importa que los cánceres se diseminen al cerebro
A medida que mejora la atención contra el cáncer, más personas viven el tiempo suficiente para que sus tumores se diseminen a nuevos órganos, incluido el cerebro. Estas metástasis cerebrales son ahora una complicación frecuente y a menudo devastadora, pero los médicos continúan tratándolas en gran medida según el lugar donde se originó el tumor—pulmón, mama, piel, colon—en lugar de según cómo el cáncer se ha adaptado a la vida dentro del cerebro. Este estudio construyó un detallado “atlas” de más de mil metástasis cerebrales para comprender su biología oculta, cómo interactúan con las células y el sistema inmunitario del cerebro, y dónde podrían existir nuevas oportunidades de tratamiento.
Construyendo un mapa gigante de tumores cerebrales
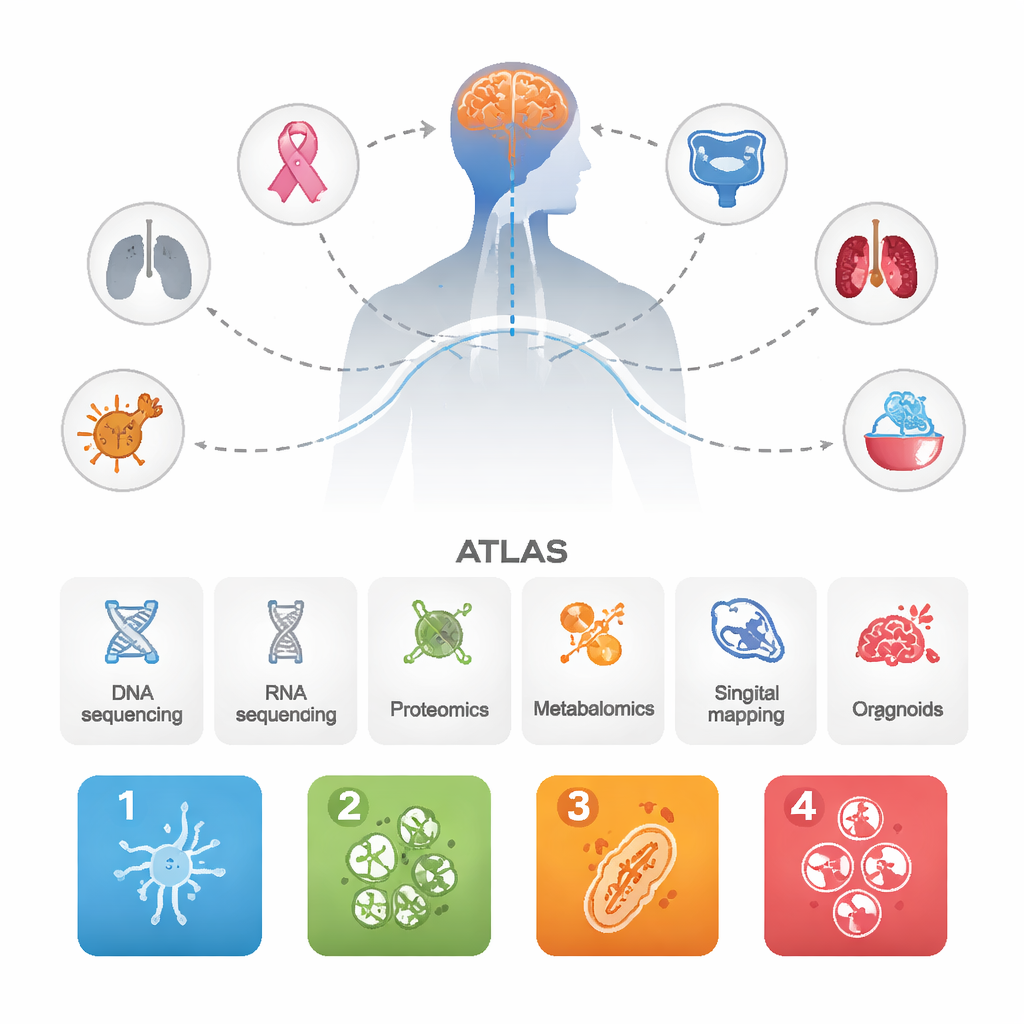
Los investigadores recopilaron datos de 1.032 metástasis cerebrales procedentes de diversos cánceres primarios, junto con docenas de tumores primarios coincidentes y algunos tumores cerebrales primarios agresivos para comparación. Combinó varias aproximaciones de vanguardia: secuenciación de ADN y ARN, mediciones a gran escala de proteínas y metabolitos, mapeo unicelular y espacial de células tumorales e inmunitarias, y organoides derivados de pacientes cultivados en el laboratorio. Al integrar todas estas capas, no se limitaron a enumerar genes, sino a ver cómo se comportan sistemas biológicos completos dentro de las metástasis cerebrales.
Cuatro “personalidades” recurrentes de las metástasis cerebrales
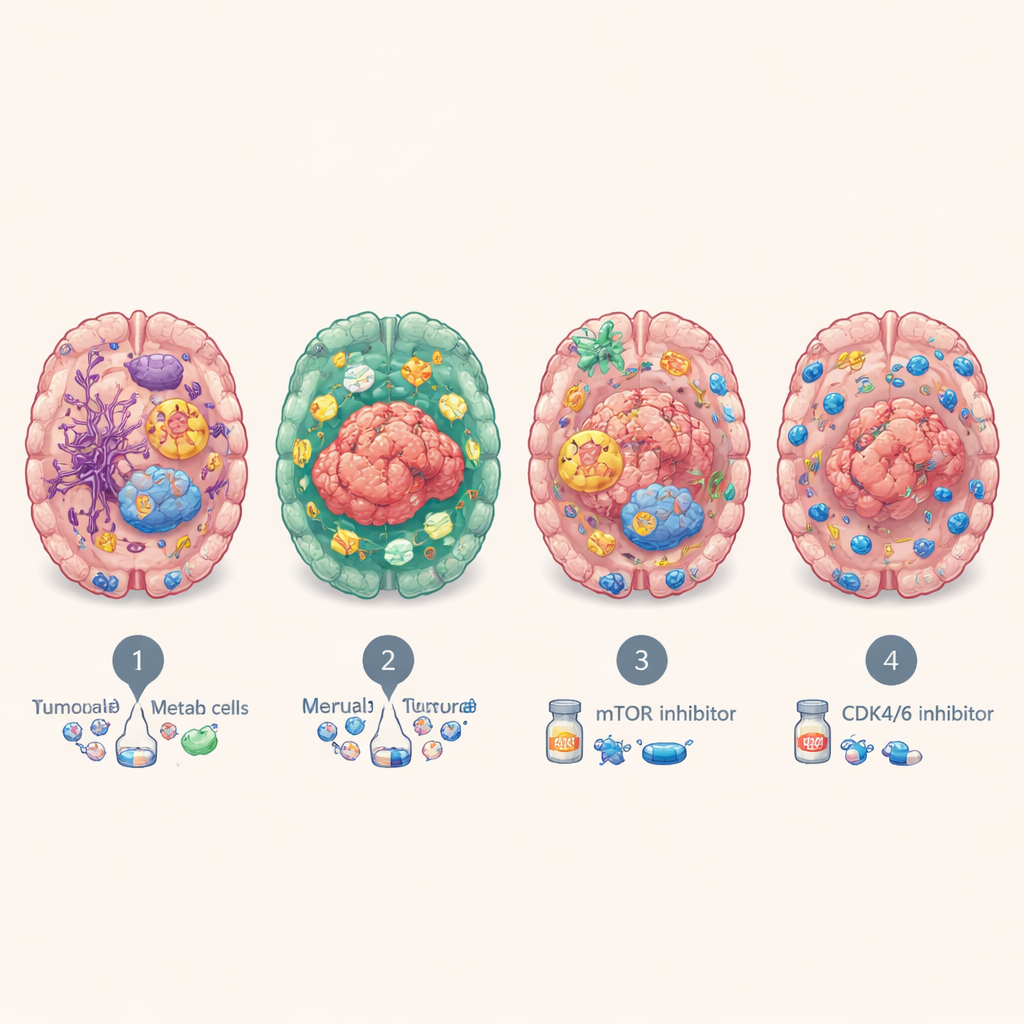
A pesar de proceder de muchos órganos, las metástasis cerebrales se agruparon repetidamente en cuatro grandes subtipos moleculares. Uno, denominado BrMS1, parece “de tipo neural”: las células tumorales y el tejido circundante expresan muchos programas propios del cerebro y de las neuronas, y muestran una vigilancia inmunitaria relativamente activa. BrMS2 es “con infiltración inmunitaria”, repleto de células inmunitarias, especialmente linfocitos T, y presenta un programa conocido como transición epitelio–mesénquima, que afloja las adhesiones celulares y remodela el entorno local. BrMS3 es “metabólico”, dominado por células cancerosas altamente activas que reajustan su uso energético—consumiendo combustible a través de vías como el metabolismo de ácidos grasos y la fosforilación oxidativa. BrMS4 es “proliferativo”, caracterizado por una rápida división celular, rasgos similares a células madre y alta inestabilidad genómica, pero, llamativamente, con muy pocas células inmunitarias.
Lo que revela el entorno del tumor
Al ampliar la resolución a nivel unicelular y espacial, el equipo mostró que cada subtipo habita un vecindario distintivo dentro del cerebro. Las lesiones BrMS1 son ricas en células de soporte cerebral como astrocitos y neuronas, lo que sugiere que el tumor imita y secuestra de cerca el tejido cerebral normal. Los tumores BrMS2, en cambio, están salpicados de densos cúmulos de linfocitos T, incluidos muchos linfocitos T “exhaustos” que expresan moléculas de control inmunitario como PD-1, y presentan vasos sanguíneos activados y señales inflamatorias. Las lesiones BrMS3 se localizan en zonas metabólicamente activas, mientras que las BrMS4 forman islas de células que se dividen rápidamente rodeadas por territorios relativamente pobres en inmunidad. En términos generales, el estudio encontró que, en las metástasis cerebrales—pero no en los tumores primarios—la fuerte activación de la transición epitelio–mesénquima suele ir de la mano con una mayor infiltración de linfocitos T, lo que sugiere que este programa podría facilitar la entrada de células inmunitarias.
Pistas sobre tratamiento y pronóstico
Estas personalidades moleculares no fueron solo académicas. Los pacientes con el subtipo con infiltración inmunitaria BrMS2 tendieron a vivir más tiempo que aquellos con el subtipo proliferativo BrMS4, que consistentemente tuvo los peores resultados. Al probar fármacos en organoides derivados de pacientes, el equipo encontró que los tumores metabólicos BrMS3 eran especialmente sensibles al bloqueo de la vía de señalización mTOR, que contribuye al control del crecimiento y el metabolismo celular, y que los tumores de rápida división BrMS4 eran más vulnerables a inhibidores de CDK4/6, fármacos que ralentizan el ciclo celular. Análisis independientes sugirieron que los tumores BrMS1 pueden responder mejor a la radioterapia, mientras que el entorno inflamado y rico en puntos de control de BrMS2 podría hacerlos más propensos a beneficiarse de inmunoterapias que reactivan a los linfocitos T exhaustos—aunque esto requiere confirmación directa en pacientes con metástasis cerebrales.
Qué significa esto para las personas con metástasis cerebrales
Este atlas muestra que, una vez que las células cancerosas llegan al cerebro, tienden a converger en unos pocos estados biológicos compartidos que atraviesan el origen primario. Entender si la metástasis cerebral de una persona es de tipo neural, rica en inmunidad, metabólica o altamente proliferativa podría, en el futuro, guiar tratamientos más personalizados—como elegir entre radioterapia, inmunoterapia o fármacos que apunten al metabolismo o a la división celular. Aunque este trabajo aún no cambia la atención estándar, ofrece una hoja de ruta detallada para futuras investigaciones y ensayos clínicos orientados a convertir estas vulnerabilidades moleculares en terapias mejores y más precisas para pacientes con metástasis cerebrales.
Cita: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Palabras clave: metástasis cerebral, subtipos tumorales, microambiente tumoral, inmunoterapia contra el cáncer, metabolismo del cáncer