Clear Sky Science · es
La composición de fosfolípidos afecta fuertemente el ensamblaje de proteínas en barril β en membranas externas bacterianas purificadas
Por qué importan las cubiertas bacterianas
Los “superbacterias” resistentes a los medicamentos suponen una amenaza creciente porque muchos antibióticos simplemente no logran atravesar sus defensas externas. Este estudio examina de cerca una pieza clave de esa defensa en bacterias Gram‑negativas como E. coli: una cubierta externa protectora repleta de proteínas con forma de barril y lípidos especializados. Al desentrañar cómo la mezcla de esos lípidos controla la construcción de la cubierta externa, los autores ponen al descubierto puntos débiles que podrían aprovecharse al diseñar futuros antibióticos.
El escudo de doble pared
Las bacterias Gram‑negativas son inusuales porque tienen dos membranas. La membrana interna se ocupa de las funciones celulares cotidianas, mientras que la membrana externa actúa como un impermeable robusto que mantiene fuera muchas toxinas y antibióticos. Esta capa externa está formada por dos tipos de lípidos: fosfolípidos comunes en el lado interno y una grasa azucarada rígida llamada lipopolisacárido (LPS) en el lado externo. A través de esta envoltura se extienden muchas proteínas «barril‑beta», cilindros huecos que forman poros y compuertas para nutrientes. Una máquina molecular llamada BAM (por barrel assembly machine) es la responsable de plegar estas proteínas y colocarlas en la membrana externa.
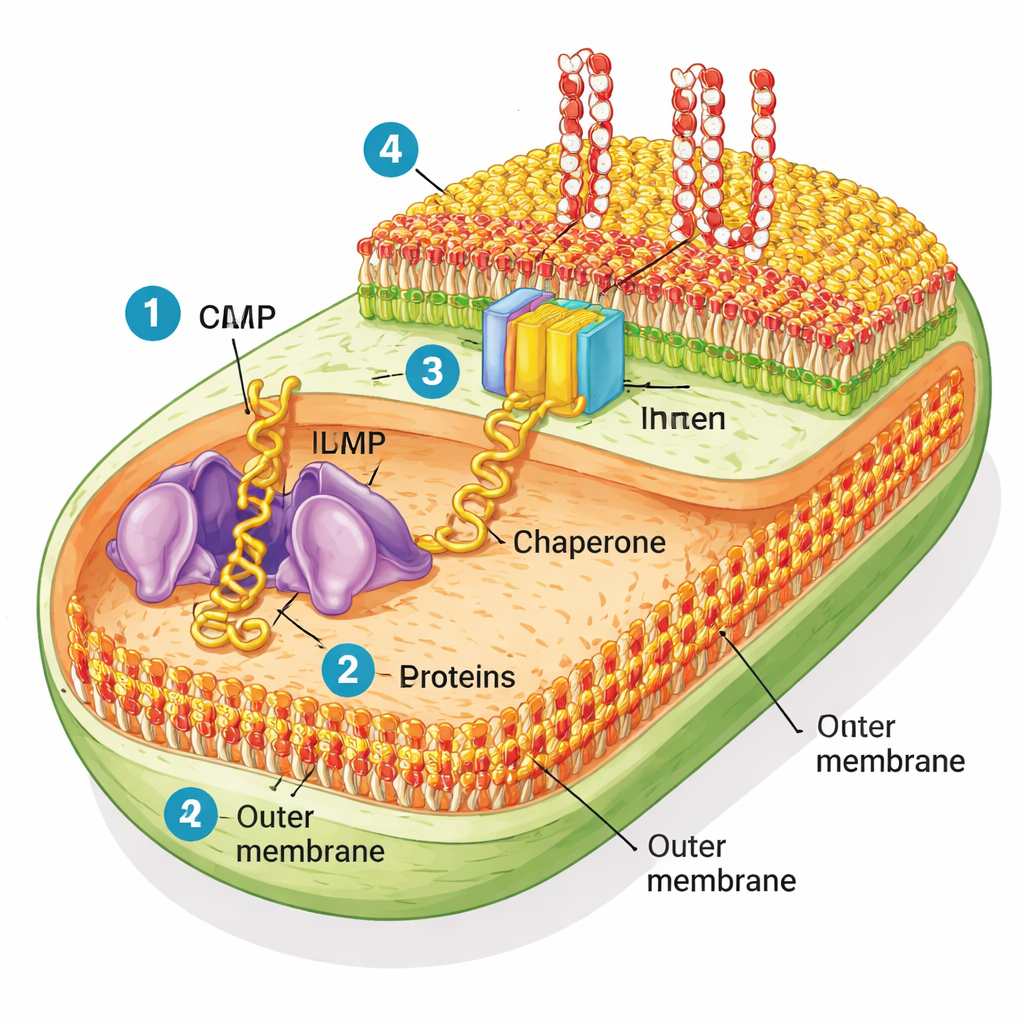
Recrear la cubierta bacteriana en un tubo de ensayo
Para ver qué tan bien funciona BAM en un entorno realista, los investigadores purificaron fragmentos de la membrana externa de E. coli, creando pequeñas burbujas que denominan «OMs nativas». A diferencia de las membranas artificiales sencillas usadas en muchos estudios de laboratorio, estas membranas nativas conservan su mezcla completa de proteínas y lípidos. El equipo empleó luego una fábrica de proteínas sin células para sintetizar nuevas proteínas de la membrana externa desde cero y observó si BAM en estas burbujas nativas podía plegarlas e insertarlas. Se centraron en una proteína modelo de barril‑beta llamada EspP, junto con algunas otras. Cuando la proteína auxiliar SurA estaba presente, BAM en las membranas nativas plegó EspP de forma eficiente, y este proceso fue bloqueado por un antibiótico conocido que apunta a BAM llamado darobactina—una evidencia clara de que la máquina natural seguía activa.
Cuando la mezcla de grasas falla
Los autores se preguntaron después qué ocurre cuando se altera el equilibrio de lípidos de la membrana externa. Estudiaron cepas mutantes de E. coli que carecían de sistemas clave que normalmente corrigen fosfolípidos mal ubicados en la monocapa externa. Un sistema, MlaA, transporta fosfolípidos errantes de vuelta a la membrana interna; otro, la enzima PldA, los degrada. Usando membranas nativas de estos mutantes, el equipo encontró que el ensamblaje de EspP impulsado por BAM disminuía notablemente en cepas sin MlaA y quedaba gravemente afectado cuando faltaba PldA. Estos efectos no se debieron a la pérdida de BAM u otras proteínas principales, que estaban presentes en niveles normales, lo que apunta al entorno lipídico alterado como la causa.
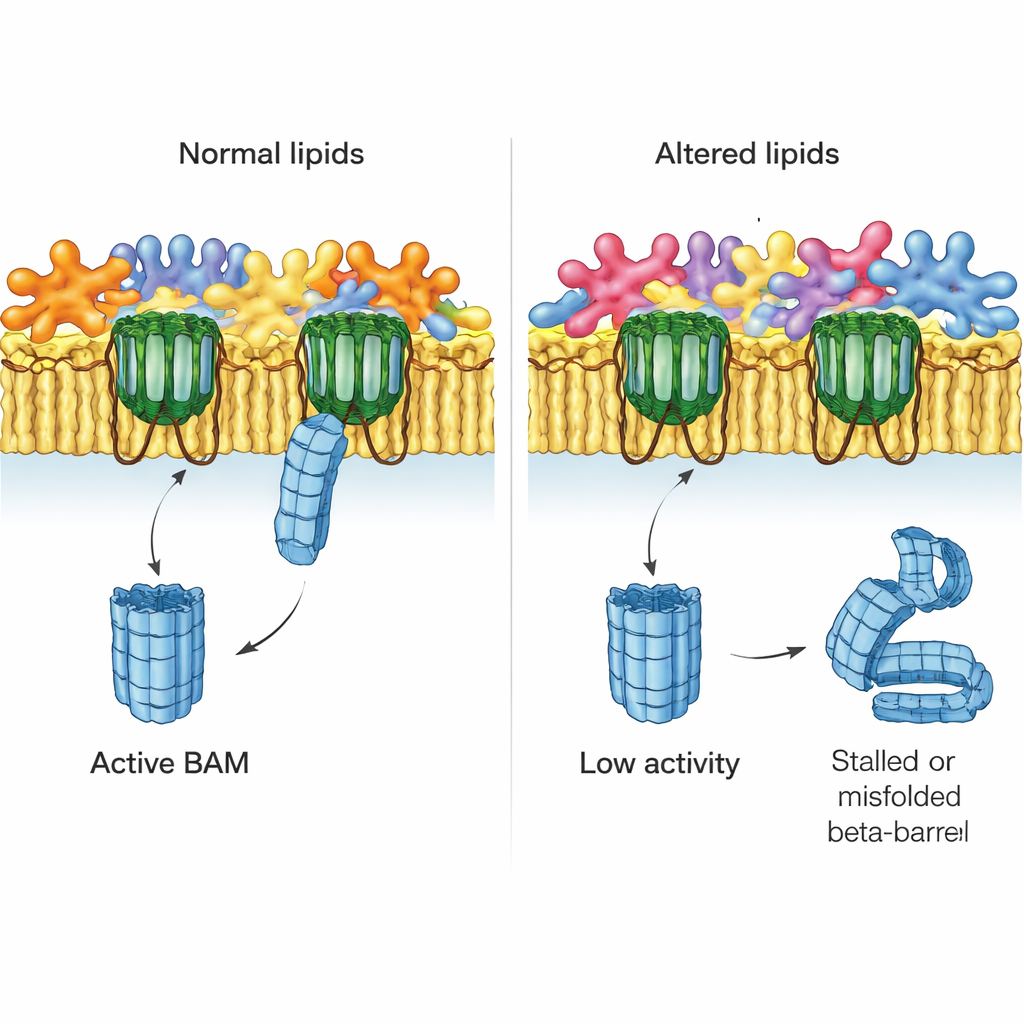
Cartografiar el paisaje lipídico en detalle
Para vincular la función con la química, los investigadores desarrollaron un método sensible de espectrometría de masas para catalogar cientos de fosfolípidos individuales en células enteras y en membranas externas purificadas. En E. coli normal, confirmaron que un tipo de lípido (fosfatidiletanolamina, o PE) está enriquecido en la membrana externa, mientras que otros (fosfatidilglicerol y cardiolipina) están relativamente empobrecidos allí. También encontraron que los «liso‑lípidos», que tienen solo una cola grasa y tienden a curvar las membranas, se concentran sorprendentemente en la membrana externa. En cepas mutantes, especialmente las sin PldA, estos patrones se trastocaron: las diferencias habituales entre membrana interna y externa se redujeron o incluso se invirtieron, y la longitud y el tipo de las colas grasas cambiaron. Las cepas con los perfiles lipídicos más alterados eran las mismas en las que BAM funcionaba peor.
Implicaciones para estrategias antibióticas
En conjunto, el trabajo muestra que la membrana externa no es solo un andamiaje pasivo para las proteínas. Su composición precisa de fosfolípidos influye fuertemente en la capacidad de BAM para construir los poros de barril‑beta que mantienen con vida a la bacteria. Cuando el equilibrio lipídico se altera, menos complejos BAM funcionan correctamente y algunos lo hacen más lentamente. Aunque las bacterias vivas pueden compensar estos cambios de maneras que un sistema in vitro no puede, este estudio pone de manifiesto cómo ajustar o perturbar lípidos específicos podría debilitar la cubierta bacteriana. Esa idea abre nuevas posibilidades para fármacos que ataquen BAM directamente o que desestabilicen sutilmente los lípidos de la membrana externa, haciendo incluso a las bacterias Gram‑negativas más resistentes más vulnerables.
Cita: Nilaweera, T.D., Brandes, N.T., LaCroix, I.S. et al. Phospholipid composition strongly affects the assembly of β barrel proteins into purified bacterial outer membranes. Nat Commun 17, 1915 (2026). https://doi.org/10.1038/s41467-026-68743-3
Palabras clave: bacterias Gram‑negativas, proteínas de la membrana externa, ensamblaje de barril‑beta, lípidos bacterianos, resistencia a los antibióticos