Clear Sky Science · es
La quinurenina media la toxicidad intestinal inducida por la quimioterapia a través de la modulación del microbioma intestinal
Por qué esto importa para las personas que reciben quimioterapia
La quimioterapia salva vidas, pero con frecuencia conlleva efectos secundarios difíciles en el intestino —dolor, diarrea, pérdida de peso— que pueden obligar a los médicos a reducir las dosis o interrumpir el tratamiento prematuramente. Este estudio desvela una reacción en cadena oculta entre un compuesto circulante, células inmunitarias y microbios intestinales que ayuda a explicar por qué un fármaco oncológico común, la oxaliplatino, puede ser tan agresivo para los intestinos, y apunta a nuevas formas de proteger a los pacientes sin debilitar su terapia anticancerígena.
Un vínculo químico entre el tratamiento y el daño intestinal
Los investigadores partieron de pacientes con cáncer colorrectal que recibían quimioterapia basada en oxaliplatino. Compararon muestras de sangre de personas que desarrollaron efectos intestinales severos con las de quienes toleraron mejor el tratamiento. Mediante perfiles químicos dirigidos, hallaron que varios productos de degradación del aminoácido triptófano estaban más elevados en el grupo de alta toxicidad, destacando una molécula —L-quinurenina— como la más aumentada de forma significativa. Los pacientes con más L-quinurenina en sangre también mostraron más signos de inflamación y recuentos bajos de glóbulos blancos, lo que sugiere que esta molécula podría estar vinculada directamente al daño relacionado con el tratamiento.
Demostrando causa y efecto en ratones
Para ir más allá de la correlación, el equipo recurrió a modelos murinos. Cuando ratones sanos recibieron dosis altas de oxaliplatino, desarrollaron signos clásicos de lesión intestinal: pérdida de peso, acortamiento del colon, engrosamiento de la pared intestinal, menos células en división y más células que morían en el revestimiento intestinal. Estos ratones también mostraron un fuerte aumento de L-quinurenina en sangre, reflejando los datos humanos. Cuando los investigadores administraron L-quinurenina adicional a ratones tratados con oxaliplatino, el daño intestinal empeoró —sin embargo, el poder anticancerígeno del fármaco sobre los tumores se mantuvo. Por el contrario, al eliminar o bloquear la enzima IDO1, que el organismo usa para convertir el triptófano en L-quinurenina, los ratones fueron mucho más resistentes a la toxicidad intestinal mientras seguían beneficiándose de la quimioterapia.
Células inmunitarias y microbios intestinales en la línea de fuego
Profundizando, los científicos investigaron qué células eran responsables de producir exceso de L-quinurenina durante el tratamiento. Descubrieron que la oxaliplatino estimula a ciertas células inmunitarias (linfocitos CD8) a liberar la proteína señal interferón-gamma, que a su vez activa IDO1 en células mieloides cercanas —una clase de glóbulos blancos. Ratones diseñados para que solo sus células mieloides carecieran de IDO1 produjeron mucha menos L-quinurenina y quedaron protegidos del daño intestinal, mientras que eliminar IDO1 solo en las células del epitelio intestinal tuvo poco efecto. Al mismo tiempo, la composición del microbiota intestinal cambió. En ratones normales, la oxaliplatino y los niveles altos de L-quinurenina se asociaron con la pérdida de una bacteria beneficiosa, Lactobacillus johnsonii. En contraste, los ratones con niveles reducidos de L-quinurenina mantuvieron niveles más altos de L. johnsonii. Cuando las bacterias intestinales fueron eliminadas con antibióticos, el efecto protector de la baja L-quinurenina desapareció, y cuando se trasplantaron bacterias de ratones con baja quinurenina a ratones normales, esos receptores se volvieron más resistentes al daño intestinal inducido por la oxaliplatino.
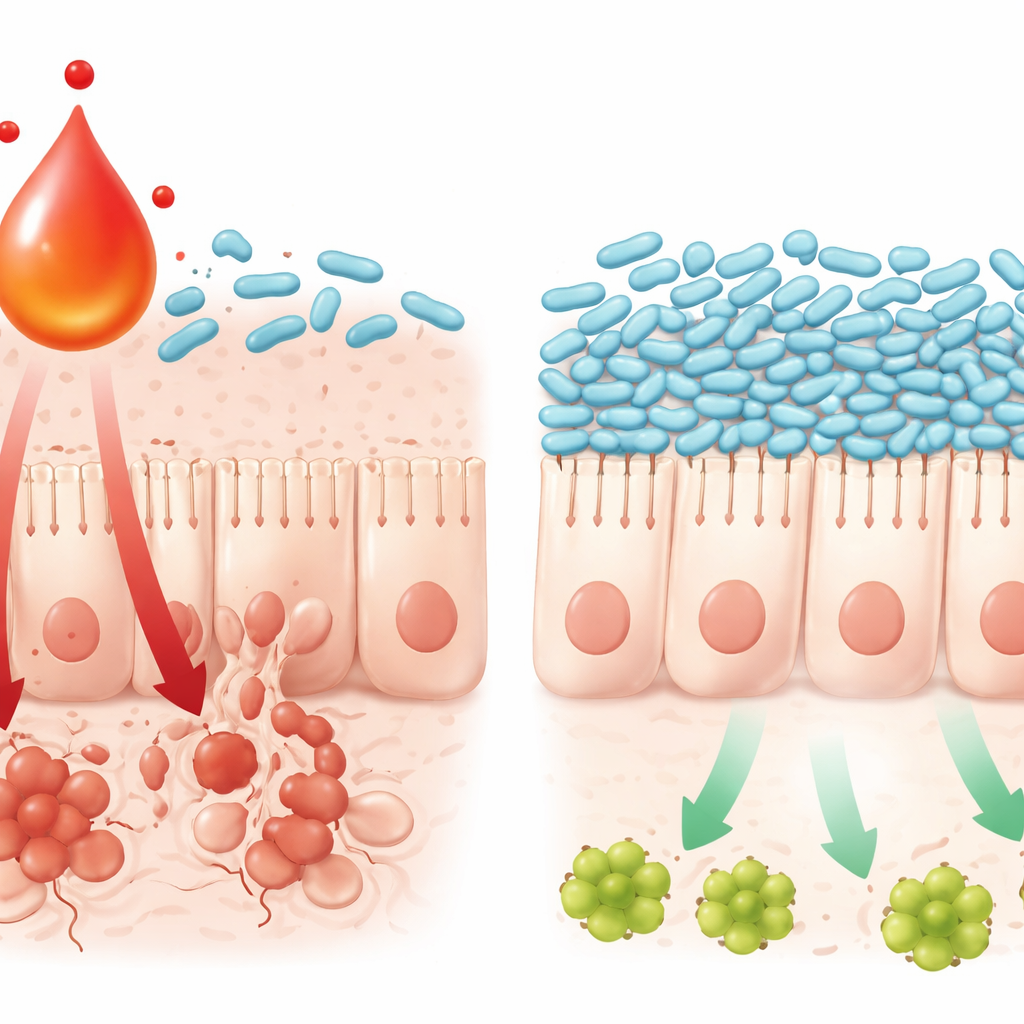
Cómo un metabolito provoca la muerte celular en el intestino
El estudio también siguió cómo esta interacción química-microbiana daña el revestimiento intestinal. Niveles altos de L-quinurenina se asociaron con una mayor actividad de una vía inflamatoria bien conocida en el tejido intestinal, la vía TNFα/JNK, que empuja a las células hacia la muerte programada. En cultivo celular, combinar oxaliplatino con L-quinurenina aumentó la propensión de las células intestinales a activar esta vía y morir, mientras que añadir la bacteria L. johnsonii amortiguó la señal y preservó la supervivencia celular. La L-quinurenina por sí sola pudo frenar el crecimiento y deteriorar los mecanismos de supervivencia de L. johnsonii en placas de laboratorio, lo que ayuda a explicar por qué la bacteria desaparece cuando el metabolito se acumula. En conjunto, estos hallazgos describen un bucle auto-reforzador: la quimioterapia desencadena señales inmunitarias, las células inmunes aumentan la L-quinurenina, esto perturba bacterias beneficiosas como L. johnsonii, y la comunidad microbiana alterada a su vez amplifica señales inflamatorias que eliminan las células del intestino.
Nuevas formas de proteger a los pacientes durante el tratamiento
De forma alentadora, el trabajo también apunta a estrategias prácticas. Tratar ratones con un fármaco llamado Epacadostat, que inhibe IDO1, redujo los niveles de L-quinurenina y disminuyó notablemente la lesión intestinal inducida por oxaliplatino sin mermar el control tumoral. En un enfoque complementario, el equipo diseñó una cepa inofensiva de E. coli para sobreproducir una enzima que degrada L-quinurenina en el intestino. Los ratones que recibieron estas bacterias modificadas estuvieron igualmente protegidos de la toxicidad intestinal, otra vez sin comprometer los efectos anticancerígenos de la quimioterapia. Suplementar con L. johnsonii también alivió los síntomas y preservó la estructura intestinal.
Qué significa esto para las personas con cáncer
En conjunto, este estudio revela que un solo metabolito inducido por el tratamiento —la L-quinurenina— actúa como un intermediario clave entre la quimioterapia, el sistema inmune, los microbios intestinales y la lesión intestinal. Al mostrar que bloquear su producción, potenciar su degradación o restaurar bacterias protectoras puede atenuar el impacto de la quimioterapia en el intestino, la investigación abre la vía a terapias complementarias que mantengan a los pacientes con más fuerza y comodidad mientras luchan contra el cáncer.
Cita: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
Palabras clave: efectos secundarios de la quimioterapia, microbioma intestinal, metabolismo del triptófano, L-quinurenina, cáncer colorrectal