Clear Sky Science · es
Las características intrínsecas del tumor moldean la diferenciación de los linfocitos T desde precursor hasta mieloma múltiple sintomático
Por qué importa esta investigación
El mieloma múltiple es un cáncer de la sangre que se origina en la médula ósea y casi siempre está precedido por estados más silenciosos y tempranos que pueden o no evolucionar hacia la enfermedad manifiesta. Muchas personas viven años con estos estadios precursores sin saber si progresarán y cuándo. Este estudio plantea una pregunta oportuna: ¿podemos leer el “estado de ánimo” y la historia del sistema inmune—especialmente de los linfocitos T—para entender cómo se desarrolla el mieloma, cómo responde al tratamiento y quién tiene mayor riesgo de progresar?
Los exploradores del cuerpo contra el cáncer
Los linfocitos T son células inmunitarias versátiles capaces de reconocer y destruir células anormales, incluidos los tumores. En cánceres sólidos como los de pulmón o piel, la estimulación prolongada puede empujar a los T hacia un estado de agotamiento en el que se vuelven ineficaces, un cambio que las inmunoterapias modernas intentan revertir. Los autores ensamblaron un enorme mapa unicelular de más de un millón de células procedentes de médula ósea y sangre de personas con mieloma múltiple, sus estadios precursores (MGUS y mieloma latente) y controles sin cáncer. Midiendo tanto la actividad génica como las secuencias únicas de los receptores que definen cada clon T, reconstruyeron cómo se organizan los T, cuán “viejos” o “experimentados” parecen y hasta qué punto siguen el comportamiento del tumor subyacente.
No agotados, sino envejecidos prematuramente
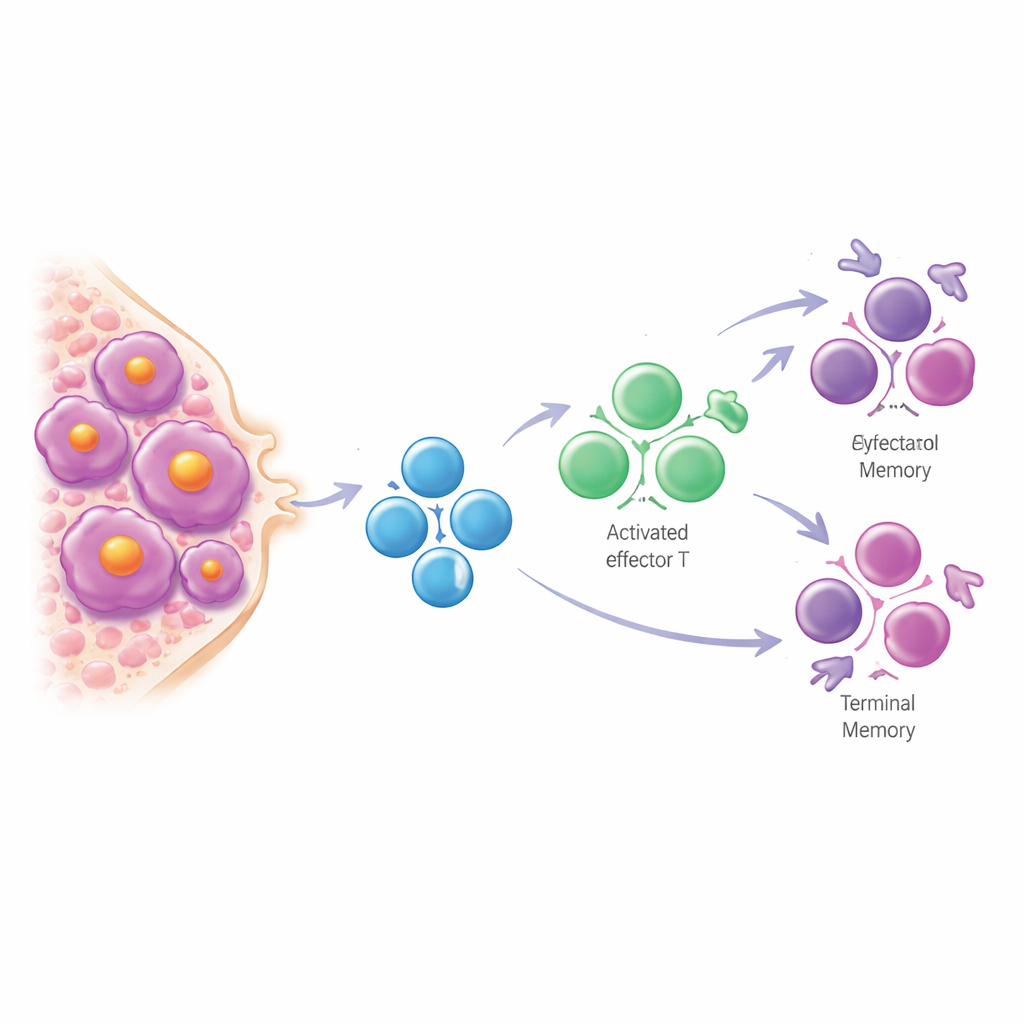
Contrariamente a lo observado en muchos cánceres sólidos, el equipo halló que los linfocitos T en el mieloma rara vez están verdaderamente agotados. Las células con marcadores clásicos de agotamiento se limitaron en gran medida a un único paciente inusual. En cambio, los T de la médula ósea en mieloma latente y sintomático se desplazaron desde células naïve o inactivas hacia tipos de “memoria terminal” muy experimentados que recuerdan a los linfocitos T de individuos mayores. Este patrón—denominado sesgo de linfocitos T—paraleló el envejecimiento natural del sistema inmune pero apareció exagerado en los pacientes, como si sus T se hubieran envejecido más rápido que el resto del organismo. Cuanto más avanzada la enfermedad y mayor la carga tumoral, más pronunciado fue este sesgo hacia células de memoria tardía, y cambios similares podían detectarse también en la sangre.
Pistas en las huellas dactilares de los T
Cada linfocito T porta un receptor único, y las células que comparten la misma secuencia de receptor pertenecen a un clon que se ha expandido en respuesta a algún estímulo. Rastreados estos receptores, los investigadores mostraron que las médulas con mieloma contienen numerosos clones T expandidos con rasgos de células asesinas potentes. Estos clones no reconocían mayoritariamente virus comunes. En lugar de ello, presentaban una firma génica “no viral” distintiva ligada a una potente maquinaria citotóxica y estaban enriquecidos en personas con mieloma frente a los estadios precursores. Los tumores que eran más eficaces en mostrar fragmentos de proteína en su superficie—mediante mayor actividad de genes de presentación de antígeno—tendían a asociarse con estos T no virales y altamente diferenciados. Los pacientes cuyos tumores exhibían este compromiso inmune más fuerte en general tuvieron mejor supervivencia, lo que sugiere que estos T son, al menos en parte, verdaderamente antitumorales.
Tratamiento, recaída y señales de aviso tempranas
El estudio siguió también a pacientes sometidos a trasplante autólogo de células madre, una terapia intensiva común. Tras el trasplante, el repertorio de receptores T pasó a estar dominado por unos pocos clones grandes. Muchos de estos clones en expansión pudieron rastrearse hasta linfocitos CD8 terminalmente diferenciados que ya estaban presentes antes del tratamiento y que portaban la misma firma no viral asociada al mieloma. Los pacientes que presentaban enfermedad residual tras el trasplante tendieron a tener repertorios T especialmente clónicos y sesgados, lo que sugiere que una respuesta T vigorosa pero de tipo envejecido puede no ser suficiente para erradicar completamente la enfermedad. Explorando etapas más tempranas, los autores hallaron que los pacientes con mieloma latente que posteriormente progresaron a mieloma activo a menudo mostraban una disminución de los linfocitos CD4 reguladores—células que normalmente ayudan a mantener el equilibrio de las respuestas inmunes y del microambiente medular. Los niveles bajos de estas células predecían una progresión más rápida, independientemente de las puntuaciones de riesgo clínicas existentes.
Qué significa esto para los pacientes
Para las personas que conviven con el mieloma y sus estadios precursores, este trabajo replantea cómo responde el sistema inmune frente al cáncer. En lugar de limitarse a agotarse, los linfocitos T en el mieloma parecen ser empujados de forma crónica hacia un estado tardío y envejecido por las batallas continuas con las células tumorales. Este paisaje T clónico y sesgado refleja la carga tumoral, condiciona la respuesta a tratamientos como el trasplante y a fármacos que movilizan T, y, en el caso de la pérdida de células T reguladoras, puede incluso señalar a individuos con mayor riesgo de progresar de mieloma latente a enfermedad sintomática. A largo plazo, estos hallazgos podrían orientar nuevas inmunoterapias que rejuvenezcan o redirijan a los T, y ayudar a los clínicos a emplear características inmunes junto con marcadores tradicionales para ajustar con mayor precisión el seguimiento y la intervención temprana.
Cita: Foster, K.A., Rees, E., Ainley, L. et al. Tumour-intrinsic features shape T cell differentiation through precursor to symptomatic multiple myeloma. Nat Commun 17, 2400 (2026). https://doi.org/10.1038/s41467-026-68718-4
Palabras clave: mieloma múltiple, linfocitos T, envejecimiento inmunitario, secuenciación unicelular, inmunología del cáncer