Clear Sky Science · es
Determinación por click de la acumulación de moléculas en Escherichia coli
Por qué las moléculas pequeñas tienen dificultades para alcanzar bacterias peligrosas
La medicina moderna depende de los antibióticos, pero algunas de las bacterias más peligrosas están ahora protegidas por pared externas resistentes que impiden la entrada de muchos fármacos. Las bacterias Gram negativas como Escherichia coli poseen una barrera de membrana externa especialmente eficaz, lo que dificulta diseñar medicamentos que realmente penetren y alcancen sus blancos. Este artículo presenta una nueva prueba de laboratorio, denominada ensayo CHAMP, que permite a los científicos medir rápidamente qué tan bien miles de moléculas pequeñas distintas sortean estas defensas y se acumulan dentro de células vivas de E. coli.
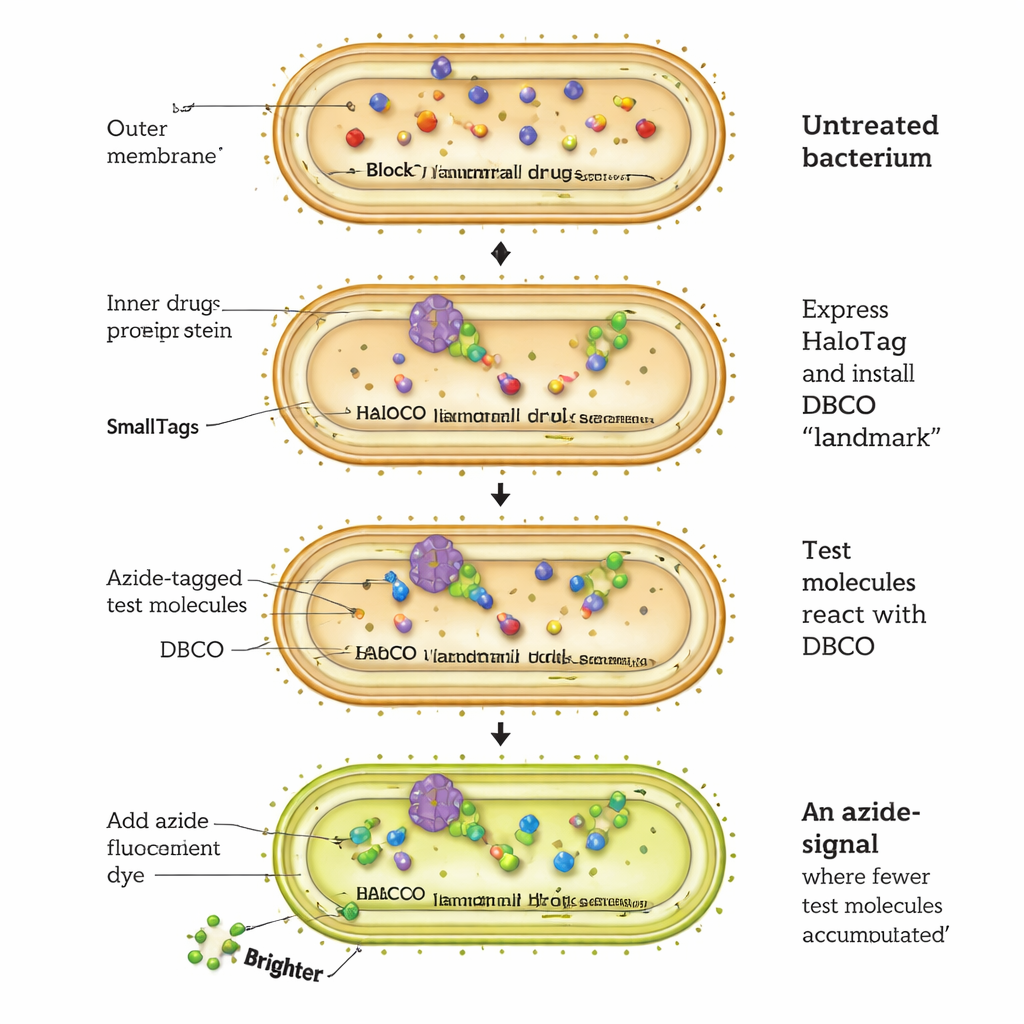
Una nueva forma de ver cómo los fármacos entran en las células bacterianas
El descubrimiento tradicional de antibióticos se basaba en compuestos naturales y ensayos simples de crecimiento para ver si las bacterias vivían o morían. Esos ensayos no revelan cuánto fármaco entró realmente en la célula, ni dónde fue una vez dentro. Los autores se propusieron construir un método directo y ampliamente utilizable para seguir la entrada de fármacos en el citosol bacteriano —el interior fluido donde residen muchos blancos antibióticos—. Su objetivo era ir más allá de lecturas toscas como la concentración inhibitoria mínima, que combina efectos de captación, unión al blanco y biología downstream, y en su lugar obtener una medida clara de la acumulación intracelular.
Convertir bacterias en pequeños registradores químicos
El ensayo CHAMP funciona reconectando una proteína bacteriana llamada HaloTag en una especie de plataforma de aterrizaje molecular. Las células de E. coli se modifican para producir HaloTag en su citosol. Los investigadores primero unen un asa química especial, un alquino «tensionado» llamado DBCO, a HaloTag mediante un enlazador corto de cloroalcano. A continuación, exponen las bacterias a moléculas de prueba que llevan cada una una muy pequeña etiqueta azida. Solo aquellas moléculas de prueba que atraviesen la membrana externa, pasen la membrana interna y lleguen al citosol pueden reaccionar con el asa DBCO en una reacción de “click” altamente selectiva, marcando permanentemente a HaloTag. Finalmente, las células se tratan con un tinte fluorescente azida que solo puede unirse a cualquier DBCO no ocupado. Cuanto más brillante sea la fluorescencia, menos moléculas de prueba llegaron al citosol; células más tenues indican mayor acumulación.
Explorar cómo la química y la biología modelan la entrada de fármacos
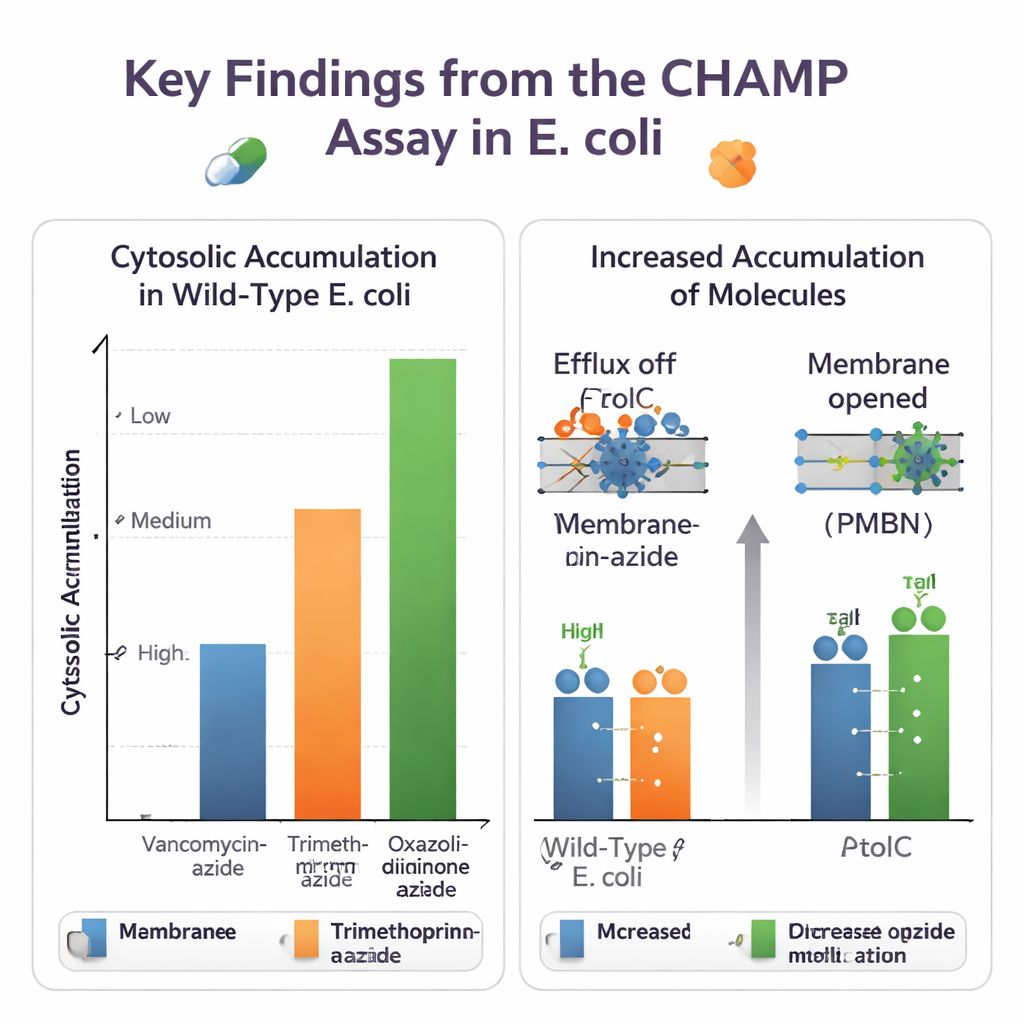
Usando CHAMP, el equipo ajustó primero la expresión de HaloTag, la cantidad del anclaje DBCO y la elección de tintes fluorescentes para obtener una ventana de señal amplia y fiable. Luego emplearon conjuntos de moléculas pequeñas estrechamente relacionadas para ver cómo cambios químicos afectan la entrada. Convertir ácidos carboxílicos en amidas, y añadir o eliminar grupos amino básicos, podía alterar de forma notable los niveles citosólicos. En muchos casos, las aminas primarias aumentaron la acumulación, en consonancia con las reglas «eNTRy» independientes desarrolladas por otros grupos. El ensayo también manejó versiones azida-decoradas de antibióticos reales, revelando grandes diferencias: fármacos voluminosos como la vancomicina apenas alcanzaron el citosol, mientras que antibióticos más pequeños como derivados del trimetoprim y algunos oxazolidinonas entraron con mucha más facilidad.
Desenmascarando defensas bacterianas que bombean los fármacos hacia afuera
Puesto que el método se ejecuta en bacterias vivas y genéticamente programables, puede desenredar los papeles de distintas defensas celulares. Los autores compararon E. coli normal con cepas carentes de TolC, un componente clave de una bomba de eflujo multidroga mayor, o con células tratadas con un inhibidor de TolC de pequeña molécula. Para la novobiocina y varios otros antibióticos azida-tag, CHAMP mostró una acumulación citosólica claramente mayor cuando TolC estaba desactivada, confirmando a estos compuestos como sustratos de eflujo. También probaron formas de aflojar la barrera de la membrana externa, ya sea químicamente con el péptido PMBN o genéticamente sobreexpresando un poro muy abierto. Muchas moléculas que antes acumulaban poco mostraron grandes ganancias cuando la membrana se permeabilizó, lo que subraya cómo la entrada y el eflujo actúan conjuntamente para fijar los niveles internos de fármaco.
Escalar a miles de moléculas para hallar patrones y reglas
Para demostrar verdadero alto rendimiento, los investigadores tamizaron un conjunto comercial de 404 compuestos azida-tag y una biblioteca personalizada de 1.152 moléculas portadoras de azida. Midieron la acumulación en varios contextos bacterianos, incluidas células sin tratar, células tratadas con PMBN, células hiperporinadas y células hiperporinadas sin TolC. Al comparar la misma molécula en estas condiciones, pudieron ver qué cambios se debían a la biología celular en lugar de particularidades de la velocidad de la reacción click. Combinando los datos de CHAMP con análisis computacional, vincularon ciertas características fisicoquímicas —como área de superficie polar, capacidad de formar enlaces de hidrógeno y andamiajes de anillos específicos— con un reconocimiento más fuerte por el eflujo basado en TolC. Este tipo de perfilado a gran escala comienza a delinear reglas de diseño para moléculas que o bien evaden las bombas o explotan mejor los poros.
Qué significa esto para futuros antibióticos
En términos sencillos, este trabajo convierte a E. coli en un sensor de alto rendimiento que informa exactamente cuánto de un compuesto de prueba llega a la parte de la célula donde viven muchos blancos farmacológicos. CHAMP no reemplaza las pruebas de si las bacterias son asesinadas, pero llena una laguna crucial al separar «entrar» de «hacer daño». Con la capacidad de medir más de mil moléculas en distintas cepas mutantes o químicamente alteradas en cuestión de días, los investigadores pueden ahora aprender sistemáticamente qué características químicas favorecen la entrada, reducen el eflujo o se benefician de socios que alteran la membrana. Ese conocimiento debería acelerar el diseño de nuevos antibióticos y fármacos auxiliares que puedan franquear las formidables defensas de patógenos Gram negativos antes de que la resistencia reduzca aún más el arsenal antibiótico.
Cita: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Palabras clave: resistencia a antibióticos, Escherichia coli, permeabilidad de fármacos, bombas de eflujo, química click