Clear Sky Science · es
Microscopía de iluminación estructurada ciega y de alta velocidad mediante desenrollado de algoritmo no supervisado
Películas más nítidas de la vida dentro de las células
La biología moderna a menudo depende de observar células vivas en acción, pero muchas estructuras clave son simplemente demasiado pequeñas y rápidas para que los microscopios convencionales las capten con claridad. Este artículo presenta una nueva forma de convertir imágenes borrosas, capturadas rápidamente, en películas nítidas y con súper detalle en tiempo real, sin necesitar un hardware perfectamente ajustado. El método, denominado microscopía de iluminación estructurada ciega desenrollada (UBSIM), promete hacer la imagen celular avanzada y de alta velocidad más accesible para laboratorios de biología cotidianos.
Por qué los microscopios convencionales se quedan cortos
Los microscopios ópticos tradicionales están limitados por la difracción, una propiedad básica de la luz que difumina detalles finos por debajo de unas pocas centenas de nanómetros. La microscopía de iluminación estructurada (SIM) aborda esto iluminando la muestra con patrones y usando la interferencia resultante para extraer detalle adicional, aproximadamente doblando la resolución. Sin embargo, la SIM clásica exige patrones de iluminación conocidos con precisión y una calibración cuidadosa, lo que puede ser costoso y frágil. Una variante más reciente, la blind‑SIM, relaja estas exigencias de hardware permitiendo patrones aleatorios y resolviendo simultáneamente la muestra y la iluminación a partir de los datos. La desventaja es que este proceso de resolución es lento e iterativo, tardando segundos a minutos por fotograma—demasiado lento para películas en tiempo real de células vivas.
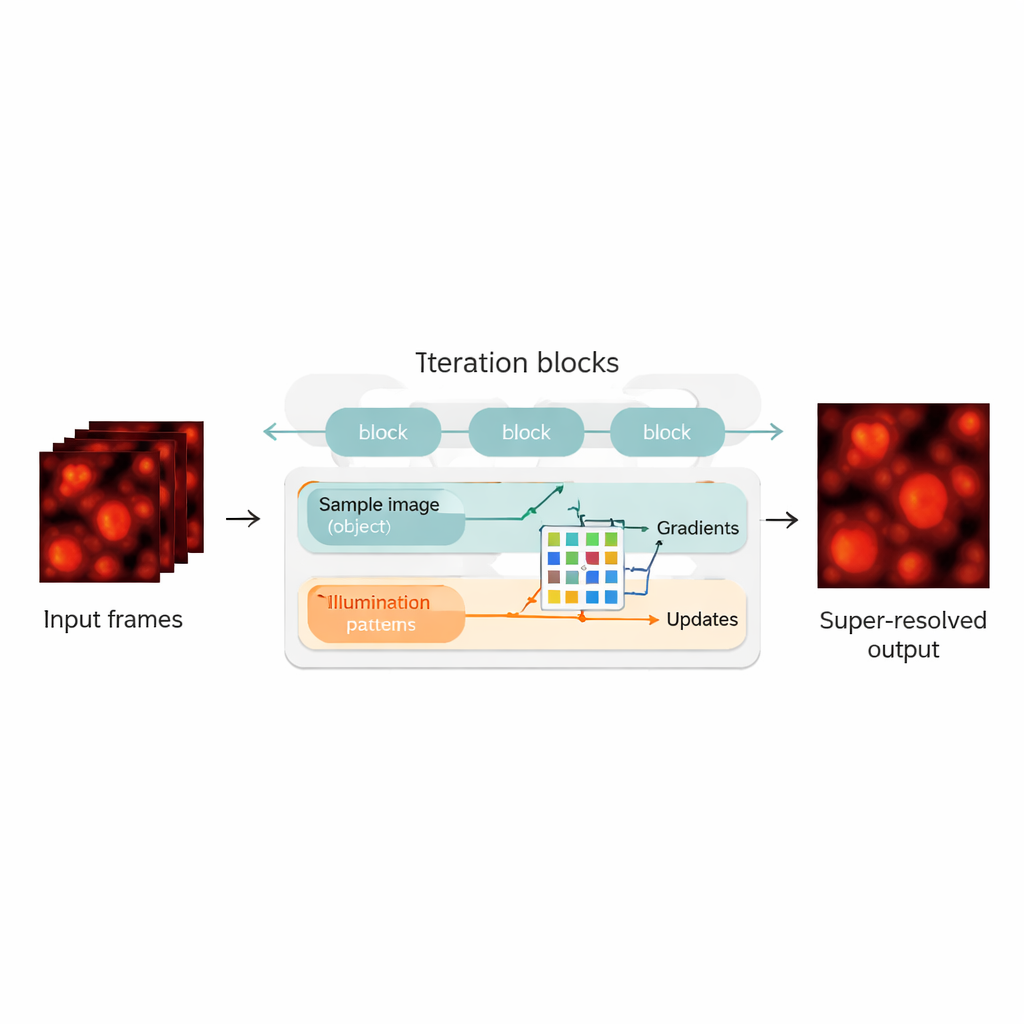
Combinando física con redes neuronales
Los autores salvan esta brecha rediseñando la reconstrucción blind‑SIM como un híbrido entre un modelo basado en la física y una red neuronal. «Desenrollan» el algoritmo iterativo original: cada iteración se convierte en una capa de la red neuronal, formando una cadena de bloques de actualización. Dentro de cada bloque, el método calcula qué tan bien la estimación actual de la muestra y la iluminación explica las imágenes medidas, calcula gradientes (direcciones de mejora) y luego los alimenta a una red neuronal convolucional compacta. Esta red aprende a realizar pasos de corrección más inteligentes, desempeñando un papel similar al de un acelerador afinado automáticamente para el algoritmo original. De forma crucial, UBSIM se entrena de manera no supervisada: en lugar de necesitar imágenes perfectas de referencia como verdad de partida, solo requiere el modelo físico de cómo la luz atraviesa el microscopio. Eso reduce el riesgo de que la red «alucine» estructuras plausibles pero incorrectas.
Rápido, preciso y menos propenso a conjeturas
Para probar UBSIM, el equipo utilizó primero imágenes de microscopía simuladas donde se conocen las estructuras subyacentes verdaderas. Mostraron que UBSIM recupera aproximadamente el doble de resolución que las imágenes de campo ancho ordinarias, comparable a la blind‑SIM estándar, pero funciona de dos a tres órdenes de magnitud más rápido: una imagen de 256×256 puede reconstruirse en unos 10 milisegundos en lugar de segundos. Las métricas de calidad de imagen, incluyendo error, similitud y medidas señal‑ruido, mejoraron notablemente en comparación con las imágenes convencionales. UBSIM también demostró ser más confiable que redes populares de superresolución por aprendizaje profundo cuando se enfrentó a datos desconocidos. Mientras que las redes estándar entrenadas en un tipo de estructura tendían a imponer ese patrón sobre nuevas muestras diferentes—introduciendo artefactos sutiles pero engañosos—UBSIM mantuvo una fidelidad consistente, porque está anclado en la física subyacente de la imagen en lugar de basarse solo en ejemplos visuales.
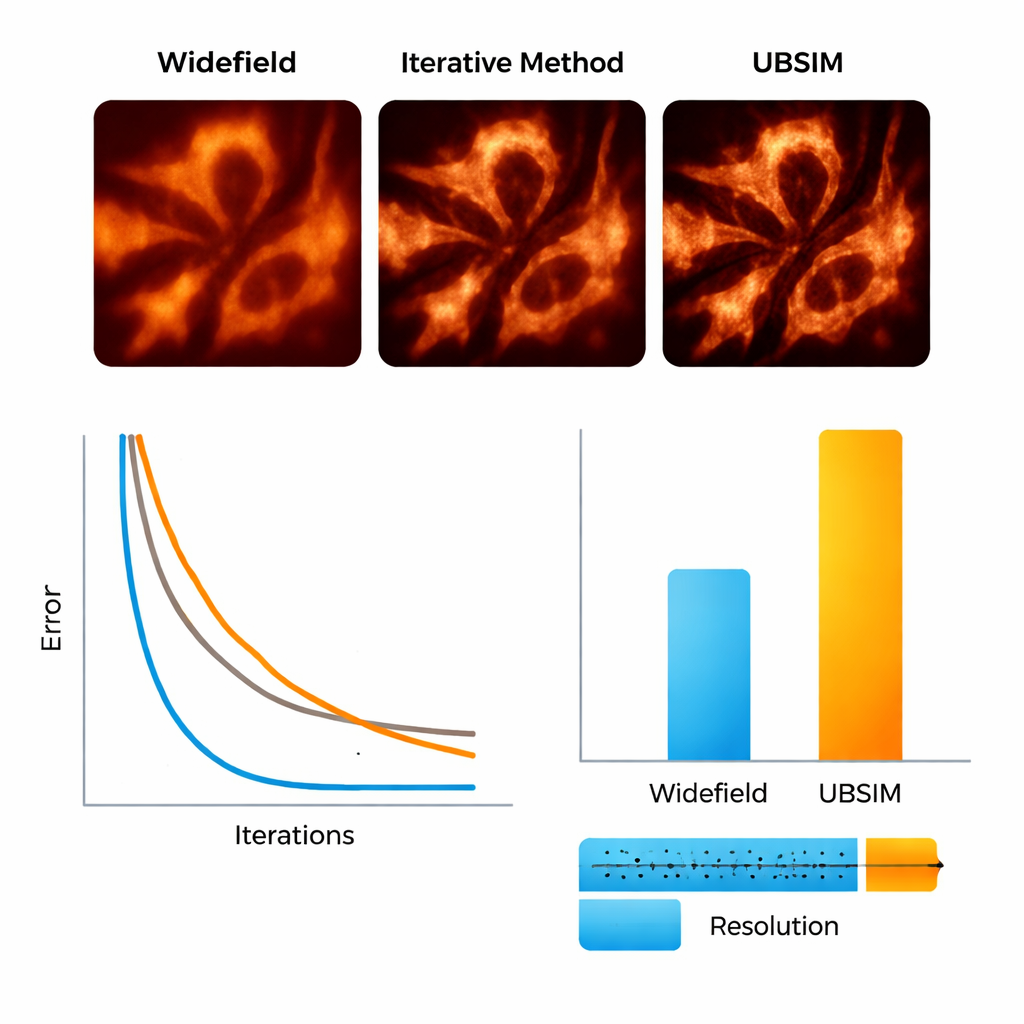
Ver esqueletos y membranas celulares en movimiento
Los investigadores pasaron luego a muestras biológicas reales. Utilizando una configuración flexible que proyecta patrones de moteado aleatorio sobre células vivas, imagenaron filamentos de actina—el «andamiaje» proteico dentro de las células—y el retículo endoplásmico (RE), una red de membranas ramificada implicada en la producción de proteínas y en la respuesta al estrés celular. Con UBSIM, fibras de actina que aparecían como bandas difusas en imágenes ordinarias se separaron en hebras nítidas, con la resolución mejorando de aproximadamente 300 nanómetros a cerca de 150 nanómetros. Lo más llamativo fue que UBSIM permitió superresolución a velocidad de vídeo: capturando datos crudos hasta 100 fotogramas por segundo y reconstruyendo hasta 50 fotogramas superresueltos por segundo, el equipo pudo observar tubulaciones del RE crecer, colapsar y reorganizarse en tiempo real. Estas dinámicas, que ocurren en fracciones de segundo a unos pocos segundos, normalmente son difíciles de visualizar con suficiente detalle.
Qué significa esto para la imagen celular futura
Para los no especialistas, la conclusión clave es que UBSIM hace mucho más práctico observar estructuras celulares diminutas en movimiento, en tiempo real y con claridad más allá de los límites normales de los microscopios ópticos—todo ello sin exigir una calibración perfecta del hardware ni conjuntos de datos de entrenamiento masivos. Al combinar la fiabilidad de los modelos basados en la física con la rapidez de las redes neuronales modernas, este enfoque convierte pilas de imágenes ruidosas y patrónadas en películas ultra‑nítidas y confiables lo bastante rápidas para experimentos rutinarios. A medida que el método se refine y se combine con mejores estrategias de iluminación, podría ayudar a los investigadores a sondear cómo orgánulos como el RE responden al estrés, cómo se reorganiza el andamiaje celular durante el movimiento o la división, y cómo las enfermedades alteran la arquitectura celular a escala nanométrica.
Cita: Burns, Z., Zhao, J., Sahan, A.Z. et al. High-speed blind structured illumination microscopy via unsupervised algorithm unrolling. Nat Commun 17, 1967 (2026). https://doi.org/10.1038/s41467-026-68693-w
Palabras clave: microscopía de superresolución, iluminación estructurada, aprendizaje profundo, imagen en células vivas, dinámica del retículo endoplásmico