Clear Sky Science · es
Perspectivas funcionales y estructurales sobre las interacciones entre β-arrestina 1 y Gαs o Gαi1
Por qué esto importa para la salud y la medicina
Muchos de los medicamentos actuales, desde los antihistamínicos hasta fármacos cardíacos y tratamientos psiquiátricos, actúan sobre una gran familia de proteínas en la superficie celular llamadas receptores acoplados a proteínas G, o GPCR. Estos receptores transmiten mensajes al interior de la célula usando dos ayudantes principales: las proteínas G y unas proteínas llamadas beta-arrestinas. Este estudio examina cómo una beta-arrestina (beta-arrestina 1) se comunica directamente con dos tipos de subunidades alfa de proteínas G dentro de la célula. Comprender esta conversación oculta podría ayudar a los científicos a diseñar fármacos más precisos y con menos efectos secundarios al ajustar con mayor finura cómo fluyen las señales dentro de nuestras células.
Dos mensajeros principales dentro de nuestras células
Cuando una hormona o un fármaco se une a un GPCR en la superficie celular, se desencadenan dos grandes vías de comunicación. Una vía utiliza proteínas G, que se activan y desactivan como relojes moleculares intercambiando un nucleótido (GDP) por otro (GTP). La otra vía emplea beta-arrestinas, que pueden tanto apagar la señalización por proteínas G como iniciar sus propias rutas de señalización. Durante mucho tiempo, los científicos estudiaron principalmente cómo los receptores se comunican por separado con las proteínas G o con las beta-arrestinas. Trabajos más recientes sugerían que las proteínas G y las beta-arrestinas también podrían unirse entre sí o incluso formar grandes “mega-complejos” con el receptor. Pero los detalles de cómo se conectan estas proteínas y qué supone eso para la señalización han sido poco claros.
Midiendo quién se une con quién
En este estudio, los investigadores se centraron en la beta-arrestina 1 y en dos subunidades “alfa” de proteínas G: Gαs, que suele estimular la actividad celular, y Gαi1, que generalmente la atenúa. Usando una técnica sensible de unión, evaluaron con qué fuerza la beta-arrestina 1 purificada y cada proteína G se adhieren entre sí en distintas condiciones. Encontraron que el factor clave no es tanto si la proteína G está “encendida” o “apagada”, sino si la beta-arrestina 1 adopta una forma más activa y flexible. Una versión de la beta-arrestina 1 a la que le falta la cola —que se comporta como un conjunto suelto y activo de conformaciones— se unió fuertemente tanto a Gαs como a Gαi1. En contraste, la forma en reposo de la beta-arrestina 1, o una forma bloqueada por un péptido similar a la cola del receptor, se unió débilmente o no se unió en absoluto. Esto sugiere que las proteínas G reconocen preferentemente a la beta-arrestina 1 cuando ésta explora conformaciones parecidas a las activas que pueden existir tras la activación del receptor. 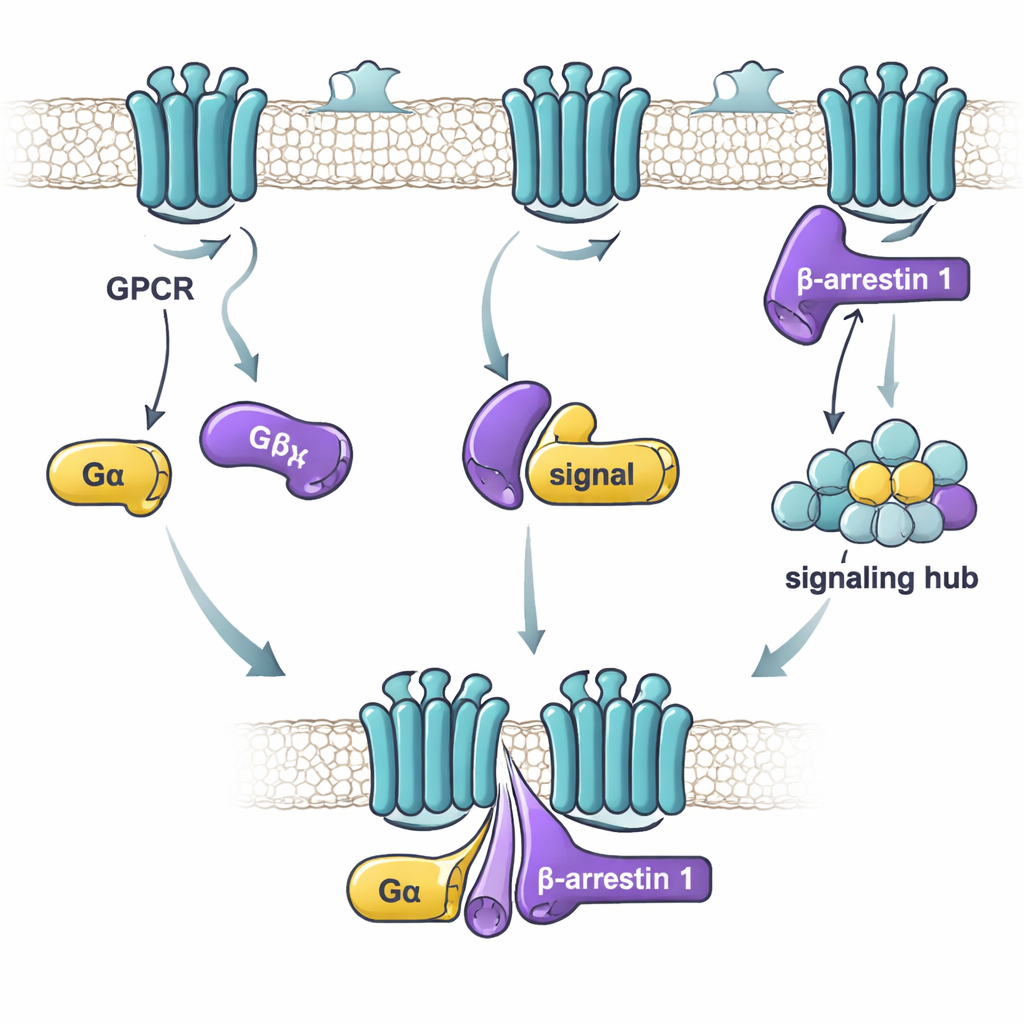
Observando cambios sutiles de forma
Para ver cómo la unión afecta la estructura proteica, el equipo usó un método que sigue la velocidad con la que los hidrógenos del esqueleto proteico se intercambian por deuterio del solvente. Un intercambio más lento suele indicar que una región se ha vuelto más protegida o rígida; un intercambio más rápido indica que se ha vuelto más flexible o expuesta. Cuando el fragmento de beta-arrestina 1 en estado activo se unió a Gαs o Gαi1, ambas proteínas G mostraron cambios de patrón claros en varias regiones, lo que indica que se estaban remodelando alrededor del complejo. En contraste, la propia beta-arrestina 1 cambió sólo ligeramente, principalmente en bucles flexibles. Trabajando con dominios aislados de las proteínas G, los investigadores también mostraron que tanto la porción catalítica principal tipo Ras como la porción helicoidal alfa circundante contribuyen a la unión. En Gαs, la región helicoidal desempeña un papel particularmente importante; en Gαi1, ambas regiones importan en proporciones aproximadamente iguales.
Función sin activar el interruptor principal
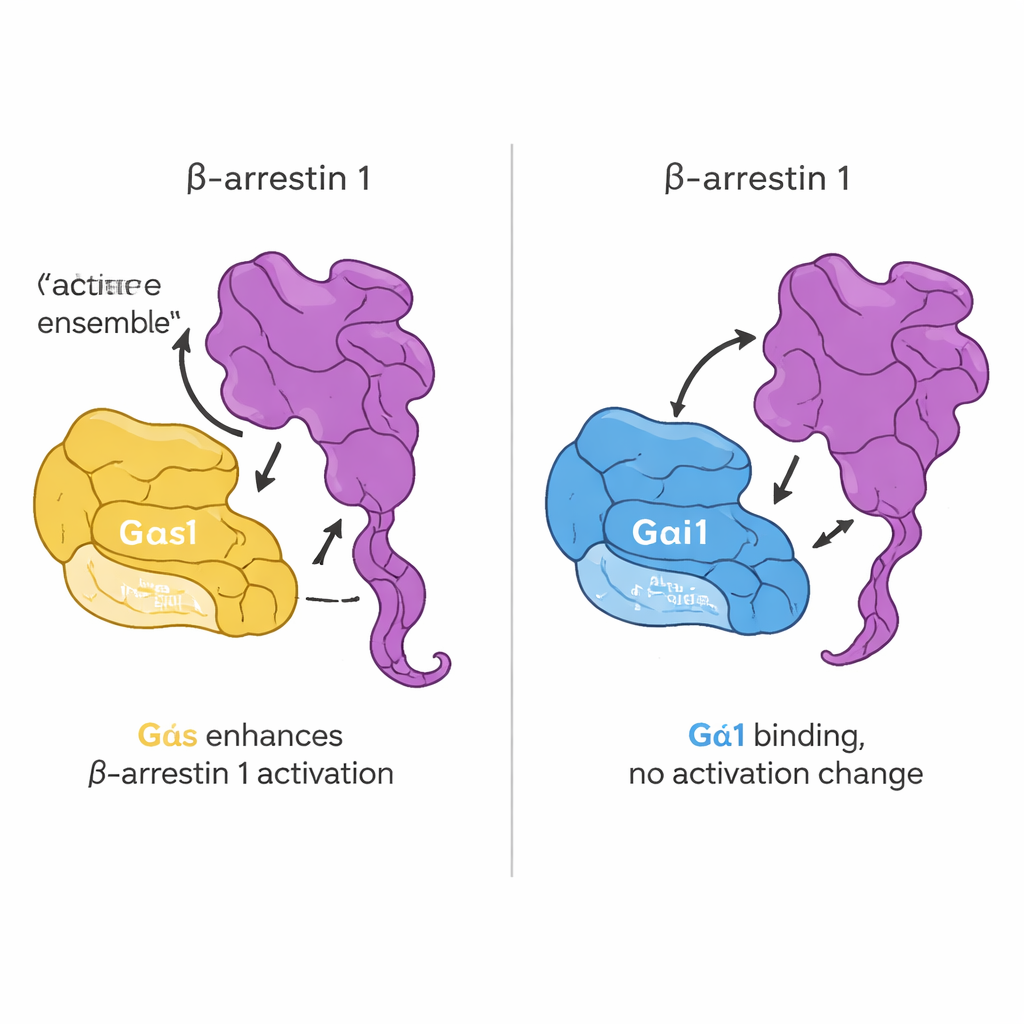
La siguiente pregunta fue si este contacto directo altera cómo se activan las proteínas G. El equipo empleó una sonda fluorescente que imita el GTP y que se ilumina cuando una proteína G cambia de GDP a GTP, una medida estándar de activación. Sorprendentemente, la adición de beta-arrestina 1 no cambió la velocidad ni la magnitud de este intercambio de nucleótidos para Gαs ni para Gαi1. En otras palabras, la beta-arrestina 1 no actúa como una enzima clásica que funciona como “interruptor de encendido” para las proteínas G. En su lugar, su influencia se detecta en su propia estructura. Usando una beta-arrestina 1 ingenierizada cuyo movimiento de la cola podía seguirse por fluorescencia, encontraron que Gαs activo, pero no Gαi1, potencia la liberación de la cola C-terminal de la beta-arrestina cuando está presente un péptido derivado del receptor. En células vivas, estudios de imagen adicionales y sensores de transferencia de energía confirmaron que Gαs y la beta-arrestina 1 se aproximan tras la estimulación hormonal y que Gαs ayuda a empujar a la beta-arrestina 1 hacia una conformación más activa.
Una nueva capa de control en la señalización celular
Uniendo estos resultados, el estudio propone que Gαs y Gαi1 se unen ambos directamente a la beta-arrestina 1, pero de maneras ligeramente distintas y con consecuencias diferentes. Ninguna de las proteínas G modifica su comportamiento principal de “encendido/apagado” por este contacto. En cambio, sobre todo en el caso de Gαs, la interacción actúa más bien como un control de ajuste fino sobre la beta-arrestina 1, empujándola o estabilizándola en una forma más activa con la cola liberada. Esto añade una capa previamente poco valorada a la señalización de los GPCR: no solo los receptores pueden coordinar proteínas G y beta-arrestinas, sino que las proteínas G y las beta-arrestinas también pueden modularse directamente entre sí. A la larga, mapear estas interacciones sutiles podría ayudar a los diseñadores de fármacos a dirigir la señalización hacia vías beneficiosas—potenciando rutas útiles mientras se evitan aquellas que causan efectos secundarios.
Cita: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Palabras clave: Receptores acoplados a proteínas G, beta-arrestina, señalización por proteínas G, mecanismos de señalización celular, biología estructural