Clear Sky Science · es
Análisis del epigenoma identifica metilación del ADN que media el riesgo cardiometabólico relacionado con el tratamiento en supervivientes de cáncer infantil
Por qué los efectos tardíos del cáncer perduran en el cuerpo
Gracias a mejores tratamientos, la mayoría de los niños con cáncer llegan a la edad adulta. Pero muchos de estos supervivientes enfrentan nuevos problemas de salud décadas después, como obesidad, hipertensión y trastornos similares a la diabetes. Este estudio plantea una pregunta urgente: ¿cómo dejan los tratamientos administrados en la infancia sombras tan largas sobre el corazón y el metabolismo? Al observar marcas químicas en el ADN de las células sanguíneas, los investigadores revelan pistas de que quimioterapia y radiación pasadas pueden “reprogramar” el organismo de forma que aumente el riesgo cardiometabólico a largo plazo.
Rastreando riesgos ocultos en supervivientes adultos de cáncer infantil
El equipo estudió a casi 3.000 adultos que sobrevivieron al cáncer infantil y forman parte del seguimiento a largo plazo de la cohorte St. Jude Lifetime. Estos supervivientes recibieron en la infancia diversas quimioterapias y radiación en el cerebro o en el tronco (tórax, abdomen, pelvis), y volvieron años después para controles de salud detallados y análisis de sangre. Los científicos se centraron en cinco problemas cardiometabólicos clave que aumentan el riesgo de enfermedad cardíaca y muerte prematura: obesidad, alteración del azúcar en sangre, triglicéridos altos, colesterol alto e hipertensión. Comparando supervivientes con y sin estas condiciones, buscaron en millones de posiciones del genoma diferencias en la metilación del ADN—pequeños interruptores químicos que ayudan a controlar cómo se activan o desactivan los genes.
Marcas químicas en el ADN como memoria del tratamiento
En todo el genoma, los investigadores identificaron casi 1.900 sitios de ADN donde los niveles de metilación se vincularon con al menos una de las cinco condiciones cardiometabólicas. La mayoría de estos sitios estaban asociados a un solo problema, pero un pequeño grupo parecía ser “hubs” conectados a varios. Cinco sitios clave, ubicados cerca de dos genes llamados CPT1A y LMNA, se asociaron simultáneamente con los cinco riesgos cardiometabólicos. Se sabe que estos genes influyen en cómo el cuerpo maneja las grasas y en el mantenimiento estructural de las células, lo que sugiere que el tratamiento puede alterar vías metabólicas y cardiovasculares compartidas. Muchas de las alteraciones en metilación coincidieron con señales observadas previamente en la población general, especialmente las relacionadas con la inflamación, pero otras parecieron ser exclusivas de los supervivientes de cáncer—lo que sugiere que el tratamiento deja una huella biológica distintiva.
Conectando terapia, cambios en el ADN y enfermedad
El siguiente paso fue probar si estos cambios en la metilación ayudan realmente a explicar cómo el tratamiento conduce a enfermedad posterior, en lugar de ser solo un marcador asociado. Los investigadores se centraron en problemas cardiometabólicos nuevos o empeorados que se desarrollaron únicamente después de la toma de la muestra de sangre, preservando la secuencia temporal: de tratamiento a cambio en el ADN a enfermedad. Mediante análisis estadísticos de mediación, identificaron 24 sitios de metilación que en conjunto explicaban hasta aproximadamente una cuarta parte del vínculo entre tratamientos específicos y problemas cardiometabólicos posteriores. La radiación en el cerebro y en el tronco mostró patrones particularmente fuertes: grupos de sitios de metilación en conjunto representaron aproximadamente entre el 10 y el 20% del impacto de estas radioterapias sobre la alteración del azúcar en sangre. Un sitio destacado, cercano a un gen llamado ANTXR2, pareció mediar cerca del 20% del efecto de la radiación en el tronco sobre problemas glucémicos posteriores.
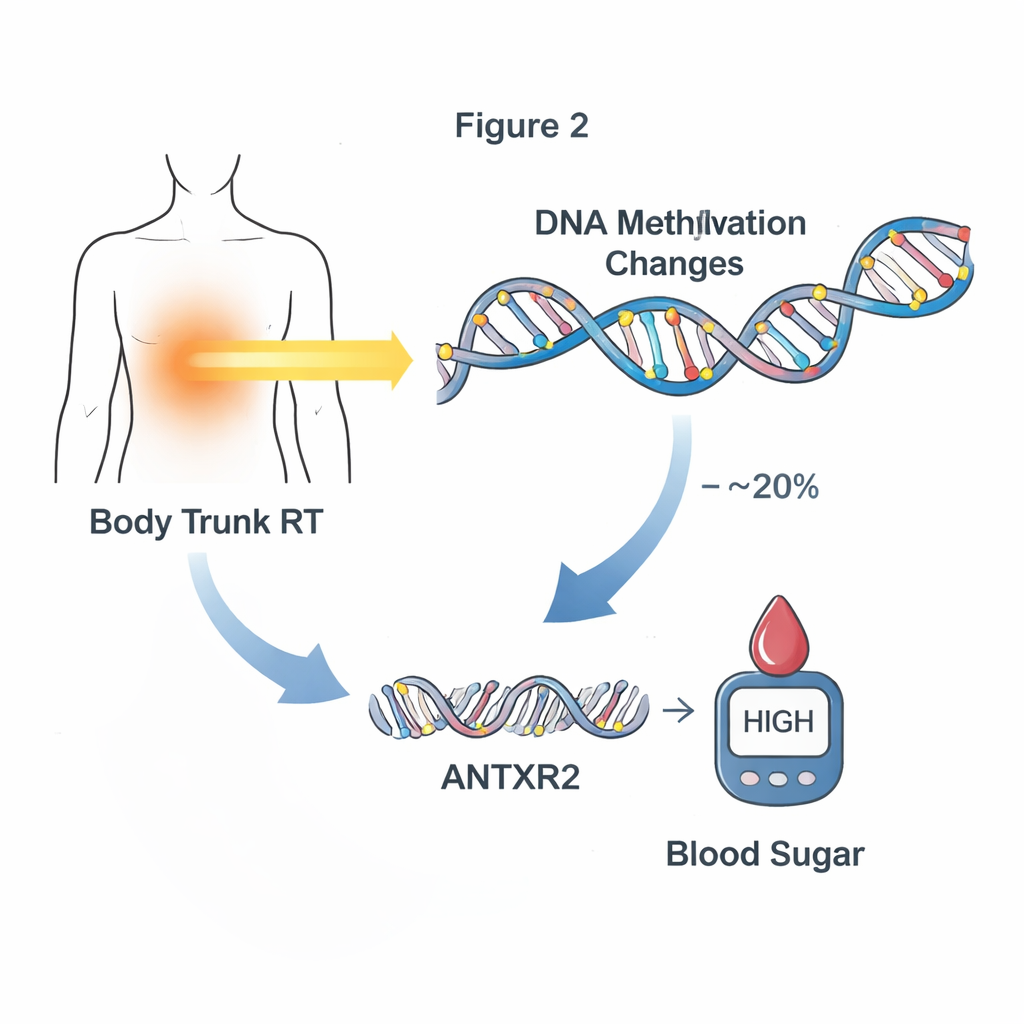
De las marcas del ADN a la actividad génica
Para entender cómo estas marcas de metilación podrían alterar la biología, el equipo examinó la actividad génica en un subconjunto de supervivientes con datos tanto de ADN como de ARN en sangre. Encontraron docenas de sitios de metilación donde niveles más altos o más bajos de metilación se vinculaban con cambios en la expresión de genes cercanos. Entre ellos estaba el sitio mediador clave cerca de ANTXR2, donde los niveles de metilación se asociaron fuertemente con cuánto se expresaba este gen, especialmente en supervivientes que habían recibido radiación en el tronco. ANTXR2 ayuda a regular los vasos sanguíneos y la estructura del tejido circundante—sistemas que influyen en cómo la glucosa y la insulina se distribuyen en el cuerpo. Este patrón sugiere una cadena de eventos en la que la radiación altera la metilación, lo que modifica la actividad génica y, a su vez, podría empujar al organismo hacia una alteración del azúcar en sangre.
Qué significa esto para los supervivientes y la atención futura
Para el público general, el mensaje clave es que los tratamientos contra el cáncer infantil no solo dañan los tejidos en el momento; también pueden dejar “notas” duraderas en el ADN que moldean la salud durante décadas. En este estudio, algunas de esas notas—cambios en la metilación del ADN—ayudan a explicar por qué ciertos supervivientes tienen más probabilidad de desarrollar obesidad, niveles altos de lípidos en sangre o problemas glucémicos relacionados con la diabetes y las enfermedades cardíacas. Aunque estas marcas químicas son solo una parte de la historia, podrían acabar sirviendo como biomarcadores en sangre para identificar a los supervivientes con mayor riesgo y para probar si cambios en el estilo de vida o nuevas terapias pueden reescribir de forma segura parte de esta historia epigenética. El trabajo acerca la atención de la supervivencia un paso más hacia la medicina de precisión: usar huellas moleculares de tratamientos pasados para guiar una prevención más temprana y personalizada de enfermedades cardiometabólicas.
Cita: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Palabras clave: supervivientes de cáncer infantil, metilación del ADN, riesgo cardiometabólico, radioterapia, epigenética