Clear Sky Science · es
Determinación cotraduccional de estructuras cuaternarias en fábricas de chaperonas
Cómo las “líneas de ensamblaje” celulares mantienen en forma a las grandes máquinas
Dentro de cada una de nuestras células, miles de piezas proteicas deben encajarse para formar complejas máquinas moleculares, desde los motores que copian el ADN hasta las fábricas que fabrican otros ARN. Este estudio plantea una pregunta aparentemente simple pero con grandes implicaciones: ¿cómo deciden las células, en tiempo real, qué proteínas ayudantes escoltarán cada nueva pieza mientras se construye, y cómo mantienen este proceso organizado en el fluido caótico de la célula?
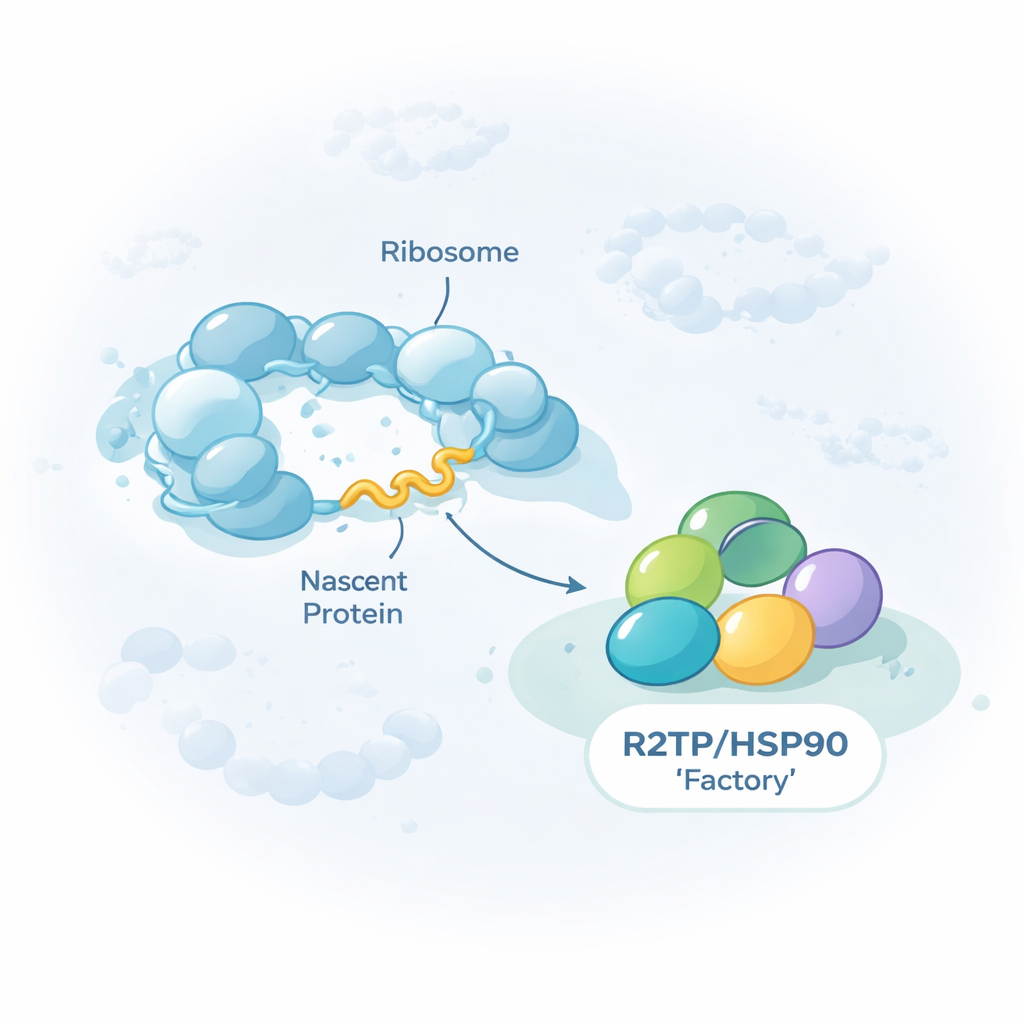
Un ayudante de uso general para mega-máquinas celulares
El trabajo se centra en un grupo de proteínas ayudantes, o chaperonas, conocidas como HSP90/R2TP. En lugar de plegar proteínas individuales, esta chaperona se especializa en ensamblar complejos gigantes de múltiples partes, incluidas las tres RNA polimerasas nucleares que transcriben ADN a ARN, ciertos ribonucleoproteínas y grandes máquinas remodeladoras que reorganizan el empaquetamiento del ADN. Los autores muestran que R2TP no solo encuentra a estos clientes una vez terminados. En cambio, a menudo se acopla mientras cada cliente aún se está fabricando en los ribosomas, las máquinas de hacer proteínas de la célula. Al purificar R2TP de células humanas y secuenciar los ARN que venían con él, hallaron alrededor de 150 ARNm cuyos productos proteicos son contactados por R2TP durante su propia traducción.
Ayudantes que acompañan a cadenas proteicas en crecimiento
Para comprobar si esta unión ocurre realmente durante la síntesis de proteínas, el equipo usó fármacos que congelan o perturban la traducción. Cuando emplearon compuestos que desprenden las cadenas proteicas nacientes de los ribosomas, la mayoría de los ARNm desapareció del agarre de R2TP. Pero cuando usaron un fármaco que simplemente pausa los ribosomas y deja las cadenas nacientes unidas, la unión de R2TP aumentó. ARN reportero diseñados confirmaron esto: si la traducción se detenía artificialmente temprano, la chaperona ya no se unía al mensaje. En conjunto, estos resultados apuntan a una regla clara de compromiso: R2TP reconoce a sus clientes principalmente a través de la cadena proteica emergente que sale del ribosoma, más que por la secuencia del ARN en sí.
“Fábricas” construidas por chaperonas que aglutinan mensajes específicos
Usando imágenes avanzadas de molécula única, los autores hicieron luego un descubrimiento sorprendente. En lugar de ver muchos mensajes distintos dispersos al azar, observaron que algunos mensajes clave—especialmente los que codifican subunidades principales de la RNA polimerasa II y un gran factor de empalme llamado PRPF8—con frecuencia se agrupaban en focos brillantes en el citoplasma. Estos focos estaban enriquecidos en R2TP y su socio HSP90, así como en componentes ribosómicos y las propias proteínas en producción, lo que muestra que son sitios de traducción activos. Cuando se bloqueó la traducción o la actividad ATPasa dependiente de energía de R2TP o HSP90, estos focos se disolvieron. Los autores llaman a estas estructuras “fábricas R2TP”: condensados especializados donde ciertos ARNm y chaperonas se concentran para favorecer el contacto oportuno y protector entre las cadenas proteicas emergentes y sus ayudantes de ensamblaje.
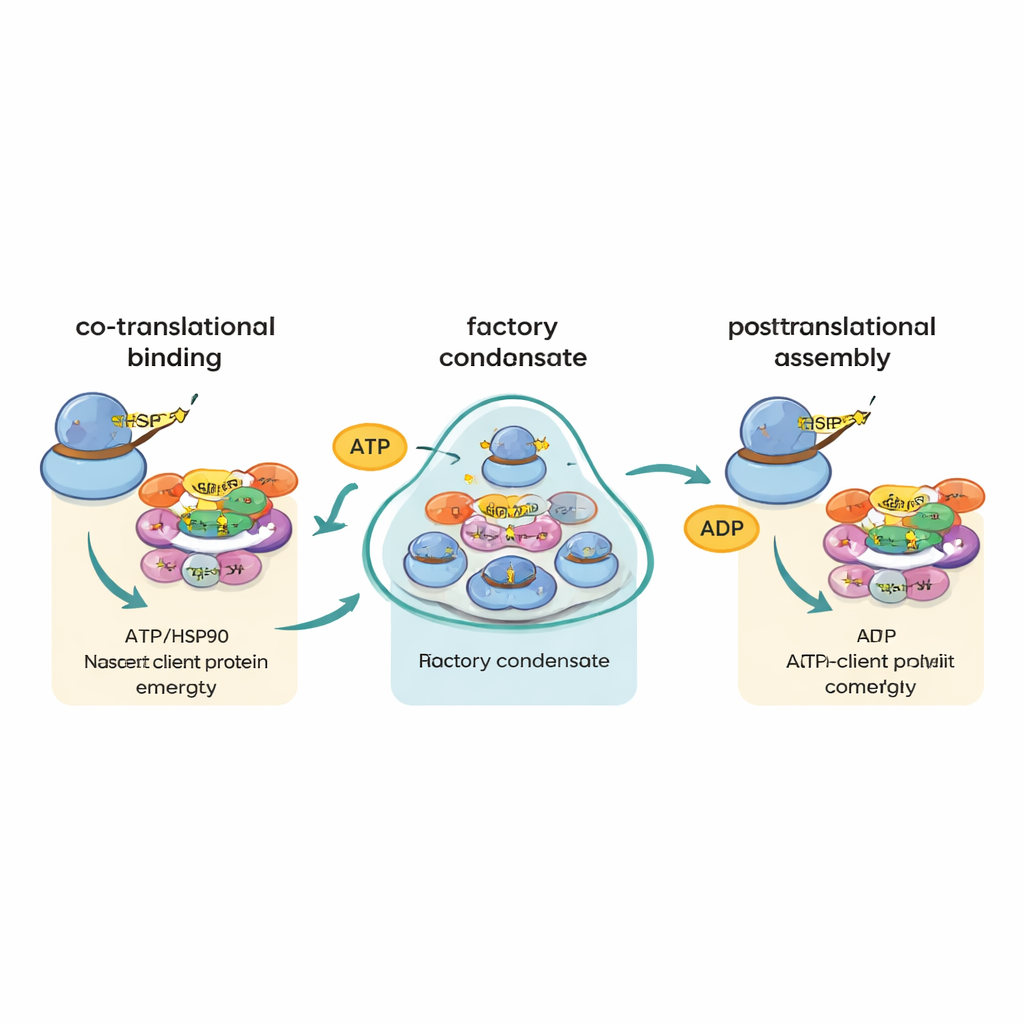
Enrutar piezas sin emparejar sus planos
Una idea previa sugería que los mensajes que codifican distintas piezas del mismo complejo podrían encontrarse y traducirse lado a lado, permitiendo que sus productos proteicos se ensamblen de inmediato. El nuevo trabajo descarta en gran medida este modelo de “planos co-localizados”. Incluso para pares de proteínas que se sabe que se unen en la misma máquina, sus ARNm raramente aparecían juntos. En cambio, los datos apoyan una estrategia diferente que los autores denominan “canalización chaperona cotraduccional”, o “cha-cha”. En este esquema, cuando cada proteína grande o propensa al ensamblaje empieza a emerger del ribosoma, R2TP y HSP90 se enganchan y determinan su destino, guiándola a través de pasos posteriores del ensamblaje. Las propias fábricas no actúan principalmente reuniendo mensajes coincidentes; más bien, aumentan las probabilidades de que las proteínas nuevas y vulnerables encuentren rápidamente la chaperona correcta.
Por qué esta organización oculta importa para la salud y la enfermedad
Al revelar que R2TP y HSP90 no solo protegen piezas proteicas frágiles sino que también definen dónde y cómo se traducen, este estudio expone una capa inesperada de organización intracelular. El mecanismo cha-cha ayuda a explicar cómo las células construyen de forma fiable enormes complejos moleculares aunque los mensajes de sus partes rara vez compartan la misma dirección. También sugiere por qué las defectos en chaperonas o en sus ciclos energéticos pueden desestabilizar máquinas vitales como la RNA polimerasa y factores de empalme, con consecuencias que van desde trastornos del desarrollo hasta cáncer. En esencia, el trabajo muestra que las células dependen de dinámicas “fábricas” de chaperonas para encauzar las piezas recién hechas hacia los ensamblajes correctos, manteniendo su maquinaria interna eficiente y ordenada.
Cita: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Palabras clave: chaperonas proteicas, ensamblaje cotraduccional, máquinas moleculares, RNA polimerasa, control de calidad celular