Clear Sky Science · es
ProteoAutoNet: análisis de proteínas co-eluidas de alto rendimiento con robótica y aprendizaje automático
Por qué importa entender las asociaciones entre proteínas
Dentro de cada célula, las proteínas rara vez actúan solas. Se asocian en alianzas cambiantes para construir estructuras, copiar el ADN, eliminar partes dañadas y alimentar el crecimiento. Muchos cánceres secuestran estas asociaciones, pero cartografiarlas en detalle ha sido un trabajo lento y laborioso. Este estudio presenta ProteoAutoNet, un sistema potenciado por robótica y aprendizaje automático que acelera considerablemente la forma en que los científicos descubren asociaciones entre proteínas en las células, y muestra cómo este enfoque puede revelar puntos débiles ocultos en los cánceres de tiroides.
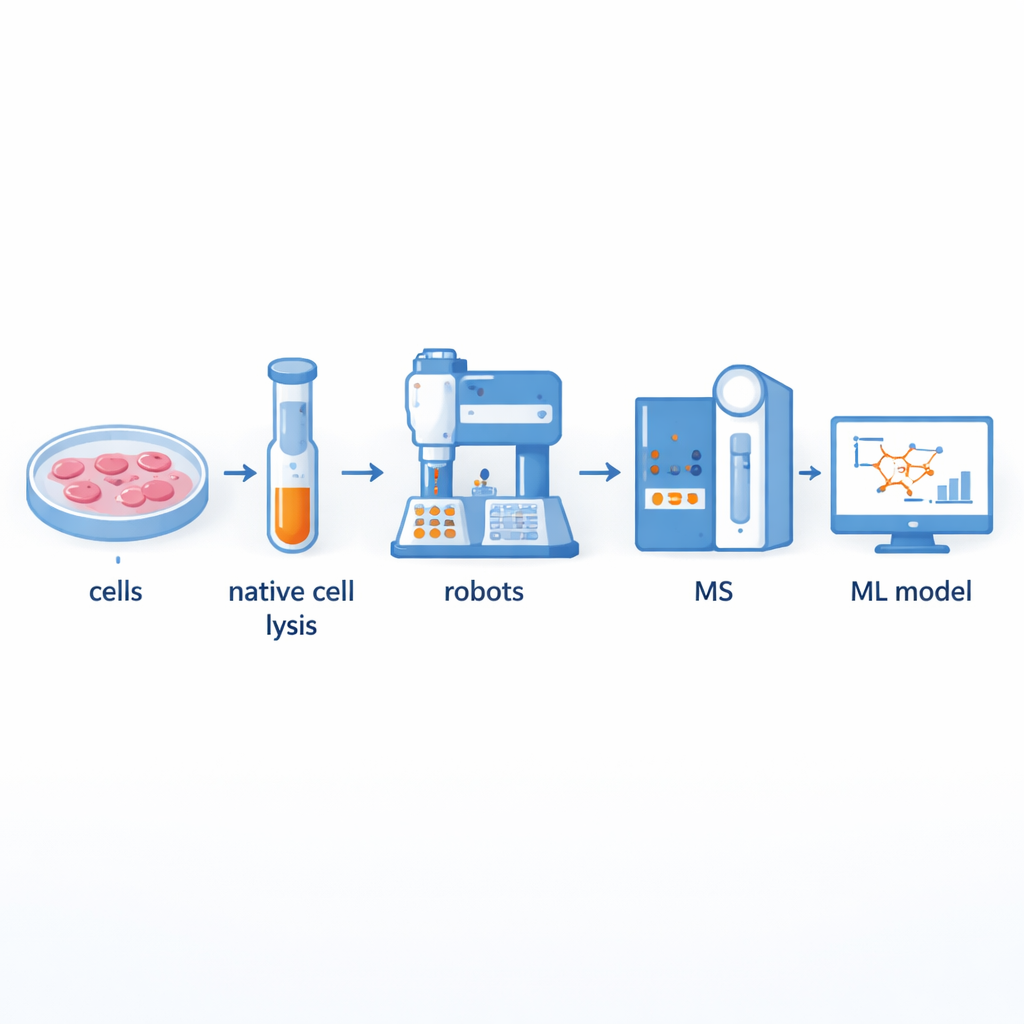
Construir una factoría de asociaciones proteicas más rápida
Tradicionalmente, los científicos usan un método llamado espectrometría de masas por co-fraccionamiento para separar complejos proteicos grandes y luego identificar sus componentes. Aunque potente, este enfoque es laborioso y de bajo rendimiento: preparar cientos de fracciones a mano puede llevar muchos días. Los autores construyeron una plataforma asistida por robótica que automatiza la mayor parte de este flujo de trabajo. El contenido celular se rompe suavemente para que los complejos proteicos naturales permanezcan intactos y luego se pasan por columnas que los separan por tamaño en docenas de fracciones. Robots manipuladores de fluidos y brazos robóticos se encargan después de añadir reactivos, digerir las proteínas en fragmentos más pequeños, limpiar las muestras y entregarlas a un espectrómetro de masas para su medición. Esta configuración puede procesar hasta 540 fracciones procedentes de múltiples líneas celulares tiroideas en solo dos o tres días, duplicando aproximadamente el rendimiento respecto a sistemas semi-automatizados previos.
Robots que no solo son más rápidos, sino más fiables
La velocidad por sí sola no basta si los resultados son ruidosos o inconsistentes. El equipo comprobó con rigor si la canalización robótica igualaba o superaba la calidad del procesamiento manual tradicional. Usando muestras de control de calidad, demostraron que el sistema automatizado identificó de forma repetida cerca de 3.000 proteínas por línea celular tiroidea con una gran superposición entre réplicas y una fuerte concordancia en las cantidades proteicas medidas. Cuando compararon directamente el procesamiento robótico y el manual de las mismas muestras, ambos enfoques detectaron números similares de proteínas, pero el método robótico produjo una variación ligeramente menor en los recuentos y mediciones de abundancia más estables. Esto significa que la nueva plataforma no solo ahorra tiempo y mano de obra, sino que también favorece experimentos más reproducibles, un requisito crucial para estudios a gran escala y aplicaciones clínicas.
Enseñar a las máquinas a reconocer conexiones significativas
Incluso con instrumentos rápidos, persiste un desafío central: decidir qué proteínas interactúan realmente y cuáles aparecen juntas por casualidad. Para abordarlo, los autores combinaron bases de datos curadas de complejos proteicos con un modelo de aprendizaje automático basado en el algoritmo XGBoost. Primero limpiaron y unificaron tres recursos principales de complejos proteicos, obteniendo 96.635 interacciones proteína–proteína conocidas. Luego usaron los perfiles de aparición de las proteínas a lo largo de las fracciones como características de entrada y etiquetaron pares como probables socios o no socios según las bases de datos. Dado que las asociaciones reales y de alta confianza son relativamente raras, emplearon una estrategia de aumento de datos dirigida: generaron muchas versiones ligeramente perturbadas de ejemplos positivos conocidos para enseñar al modelo a reconocer patrones robustos en lugar de memorizar trazas específicas. Entrenado con decenas de millones de ejemplos de este tipo procedentes de tres líneas celulares tiroideas, el modelo logró un rendimiento sólido, clasificando correctamente las interacciones verdaderas por encima del azar tanto en pruebas internas como en una línea de validación independiente.
Nuevas perspectivas sobre la maquinaria celular del cáncer
Con este flujo de trabajo, los investigadores trazaron redes de interacción en una línea celular tiroidea normal y en dos líneas cancerosas: una carcinoma papilar de tiroides y una carcinoma folicular que puede diseminarse a los pulmones. En estas células identificaron más de 25.000 interacciones proteicas probables y detectaron señales fuertes de máquinas celulares bien conocidas, como los ribosomas (que sintetizan proteínas) y los proteasomas (que las degradan), confirmando que el método recupera biología establecida. Al comparar las células tumorales con la línea normal, descubrieron redes sobreactivadas en la enfermedad. En las células de carcinoma folicular metastásico, tanto componentes del proteasoma como un complejo chaperón llamado prefoldina mostraron una conectividad y abundancia marcadamente mayores. Varios subunidades de prefoldina se habían vinculado previamente a otros cánceres, pero los estudios proteómicos globales habían pasado por alto su comportamiento coordinado en cáncer de tiroides, posiblemente porque estas proteínas están fuertemente reguladas por degradación. El enfoque de co-fraccionamiento puso de manifiesto sus cambios coordinados a nivel de complejo.
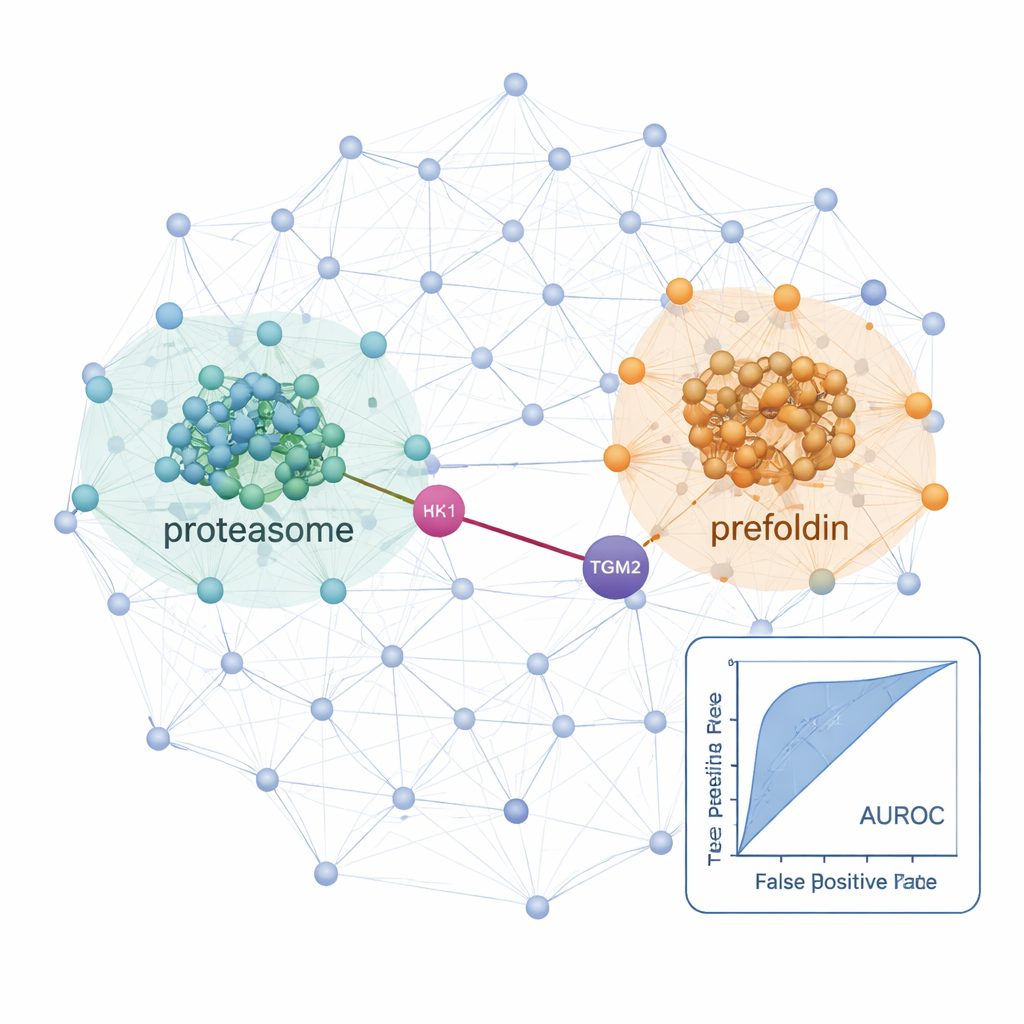
Vínculos ocultos que pueden orientar tratamientos futuros
El estudio también destacó interacciones específicas que podrían influir en cómo los cánceres de tiroides crecen y se diseminan. Un ejemplo es una asociación predicha entre HK1, una enzima que inicia la principal vía de consumo de azúcar de la célula, y TGM2, una proteína conocida por favorecer la invasión y la metástasis en tumores tiroideos. Esta conexión HK1–TGM2, ausente de las bases de datos de interacción existentes, recibió apoyo de modelado estructural y apareció particularmente activa en la línea de carcinoma papilar, lo que sugiere que la reprogramación metabólica y el comportamiento invasivo podrían estar vinculados físicamente. En conjunto, ProteoAutoNet muestra cómo la combinación de robótica y aprendizaje automático puede transformar el mapeo de redes proteicas, antes lento y reservado a expertos, en un proceso más escalable. Para el público no especializado, el mensaje clave es que esta tecnología puede descubrir tanto cambios amplios en la maquinaria celular como asociaciones proteicas inesperadas que, en el futuro, podrían ayudar a los médicos a predecir mejor qué cánceres de tiroides serán agresivos y a proponer nuevos objetivos terapéuticos.
Cita: Lyu, M., Hu, P., Zhang, G. et al. ProteoAutoNet: high-throughput co-eluted protein analysis with robotics and machine learning. Nat Commun 17, 1949 (2026). https://doi.org/10.1038/s41467-026-68686-9
Palabras clave: interacciones proteicas, espectrometría de masas, aprendizaje automático en biología, cáncer de tiroides, proteasoma y prefoldina