Clear Sky Science · es
Descubrimiento iterativo de potentes antibióticos poliméricos mediante aprendizaje multitarea y por fases frente a la resistencia antimicrobiana
Por qué importan los nuevos antibióticos para todos
Las infecciones resistentes a los medicamentos están aumentando en todo el mundo, lo que hace que enfermedades familiares sean más difíciles y, a veces, imposibles de tratar. Este estudio describe una nueva forma de descubrir rápidamente un tipo diferente de antibiótico: pequeños polímeros sintéticos que pueden tanto matar bacterias resistentes como ayudar a que fármacos antiguos, como la penicilina, vuelvan a ser eficaces. El trabajo combina inteligencia artificial avanzada con química y pruebas en animales para explorar un enorme espacio químico que sería imposible abarcar por ensayo y error.
Buscando nuevos defensores en un universo químico abarrotado
Los antibióticos tradicionales suelen dirigirse a proteínas bacterianas específicas, que las bacterias pueden evadir gradualmente. En contraste, los polímeros de este estudio imitan los péptidos defensivos propios del organismo, que dañan físicamente las membranas bacterianas y son menos propensos a generar resistencia. El reto es que existen decenas de miles de posibles estructuras poliméricas, y su comportamiento depende de un equilibrio sutil entre carga positiva, componentes hidrofílicos e hidrofóbicos. Probar manualmente suficientes candidatos para encontrar los seguros y potentes llevaría años. Los autores construyeron una biblioteca combinatoria de aproximadamente 100.000 polímeros relacionados llamados poli(β-amino ésteres), cada uno diseñado para autoensamblarse en partículas de tamaño nanométrico que pueden interactuar fuertemente con las superficies celulares bacterianas.
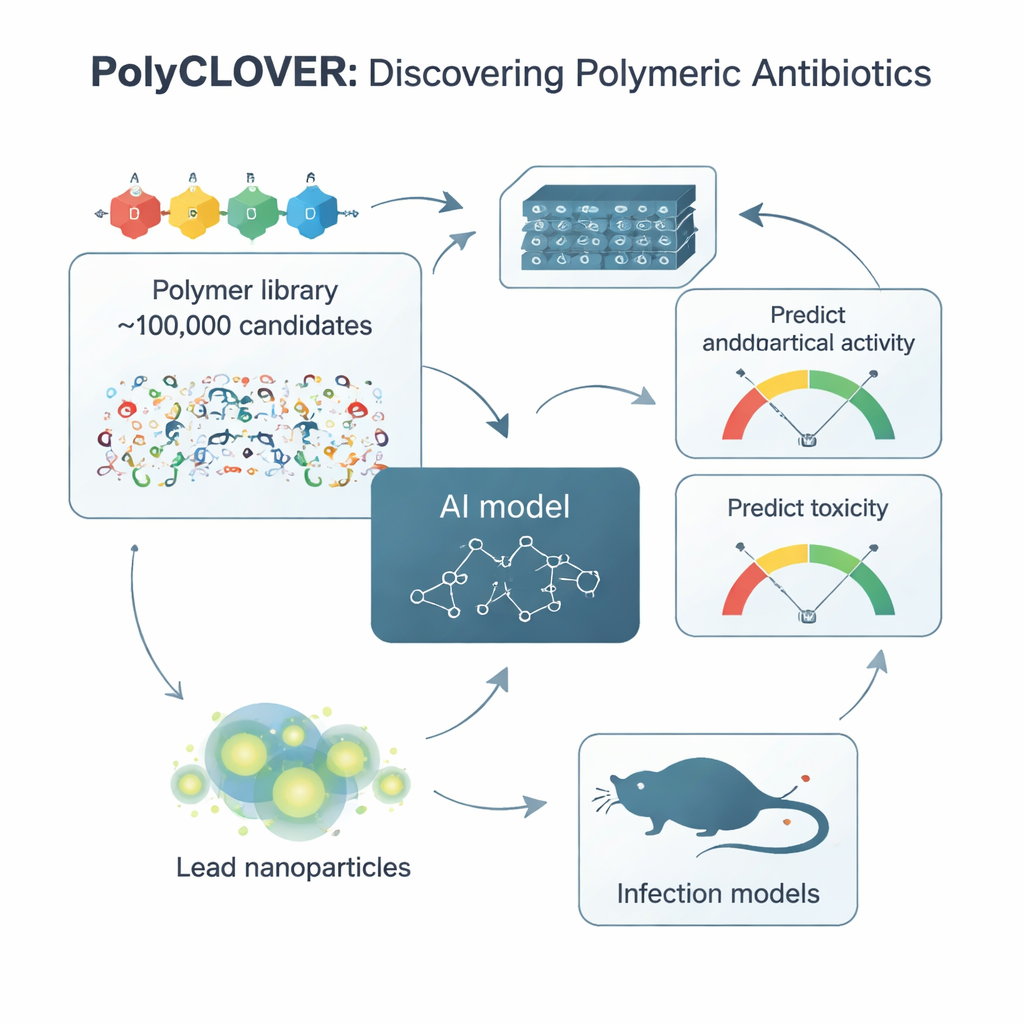
Enseñar a una IA a leer el “lenguaje corporal” de los polímeros
Para navegar esta biblioteca, el equipo creó un marco que denominan PolyCLOVER. En su núcleo hay una red neuronal basada en grafos que trata cada polímero como una red de átomos conectados, permitiendo al modelo captar diferencias estructurales sutiles. Debido a que había muy pocos ejemplos etiquetados sobre qué polímeros eran buenos o malos antibióticos, los investigadores emplearon una estrategia de aprendizaje auto-supervisado por fases. Primero, el modelo se entrenó con alrededor de un millón de estructuras poliméricas no etiquetadas para captar patrones químicos generales. Luego se entrenó adicionalmente con la biblioteca no etiquetada de 100.000 miembros y, finalmente, se ajustó con un pequeño conjunto de 220 polímeros que se habían sintetizado y probado por su potencia antibacteriana y su daño a los glóbulos rojos. Este aprendizaje por etapas mejoró drásticamente la capacidad del modelo para predecir qué nuevos polímeros serían a la vez potentes y seguros.
Dejar que experimentos y algoritmos aprendan entre sí
PolyCLOVER no se queda en una sola ronda de predicciones. Funciona en un bucle en el que la IA sugiere los candidatos más prometedores e informativos, los químicos los sintetizan y prueban en formato de alto rendimiento, y los nuevos resultados se retroalimentan para refinar el modelo. La fase de selección usa un enfoque de «cota superior de confianza» que equilibra la explotación (favorecer polímeros predichos como eficaces) con la exploración (sondear regiones inciertas donde el modelo puede aprender más). En unas cuatro rondas iterativas, los polímeros sugeridos mejoraron de forma sostenida: se hicieron más potentes frente a Staphylococcus aureus resistente a meticilina (MRSA) manteniendo una toxicidad aceptable hacia los glóbulos rojos. En solo 20 días de experimentación, el sistema convergió hacia un pequeño conjunto de actuaciones destacadas.
Pequeñas partículas autoensamblables que perforan las bacterias
Los tres polímeros líderes finales, denominados H1, H2 y H3, se autoensamblaron espontáneamente en nanopartículas con carga positiva de unos 100 nanómetros de diámetro. En pruebas de laboratorio, mataron MRSA con la misma eficacia que un antibiótico estándar, la estreptomicina, y lo hicieron mucho más rápido: redujeron el recuento bacteriano varios órdenes de magnitud en minutos a horas, incluso en suero rico en proteínas. Microscopía electrónica y sondas fluorescentes mostraron que estas partículas se adhieren rápidamente a la superficie bacteriana y alteran la integridad y el potencial eléctrico de la membrana, provocando la fuga del contenido celular. De forma importante, cuando MRSA se expuso a estos polímeros durante casi un mes, las bacterias desarrollaron muy poca resistencia, en marcado contraste con la estreptomicina, cuya dosis requerida aumentó dramáticamente en el mismo período.
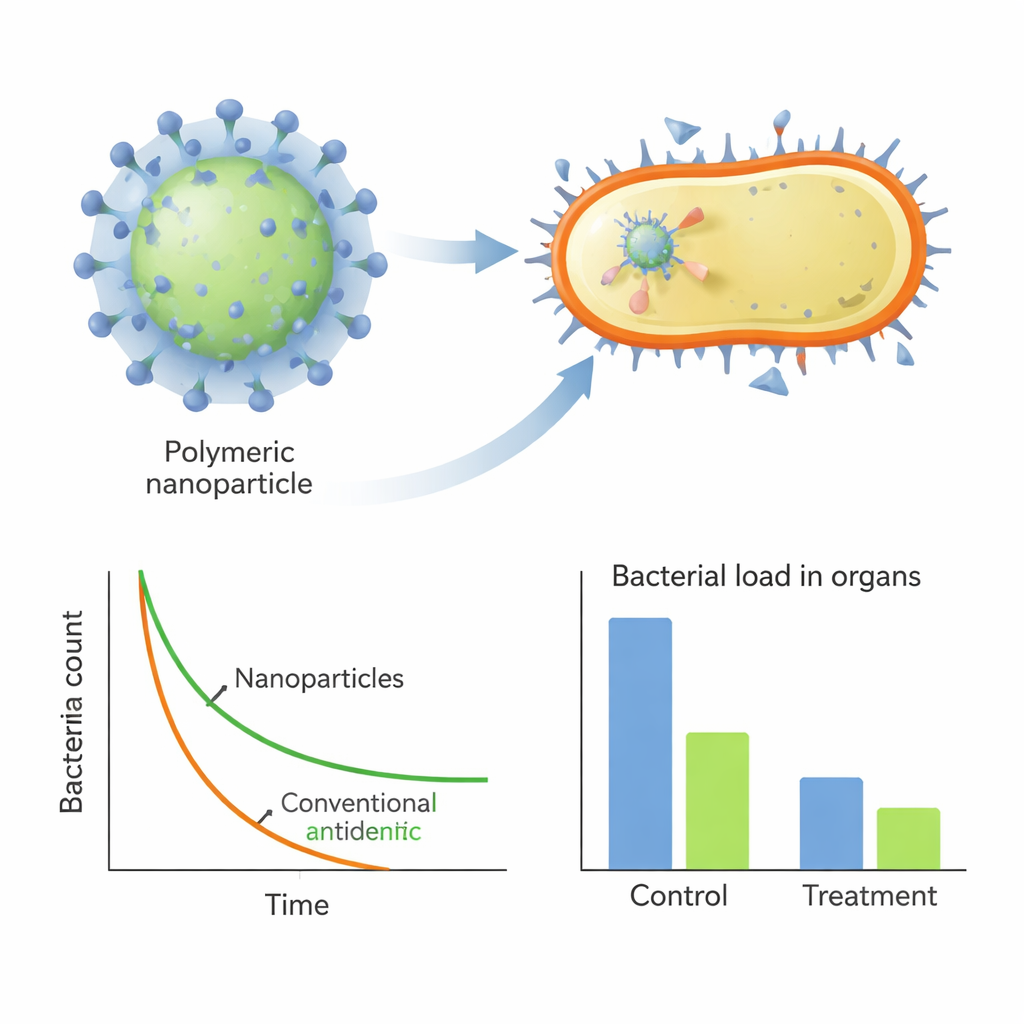
Reactivar antibióticos antiguos en infecciones animales
Además de actuar por sí solas, las nanopartículas también funcionaron como potentes auxiliares de fármacos tradicionales. Cuando se combinaron con penicilina G, frente a la cual MRSA es normalmente muy resistente, el mejor polímero (H2) formó nanocompuestos que atrapaban el antibiótico dentro de la partícula. Estos compuestos mostraron una fuerte sinergia en ensayos de laboratorio, reduciendo drásticamente la dosis de penicilina necesaria para detener MRSA. En modelos murinos de infección pulmonar y de una infección abdominal grave, el tratamiento con los polímeros líderes —ya sea solos o en combinación con penicilina— redujo marcadamente la carga bacteriana en órganos, disminuyó las señales inflamatorias en la sangre y limitó el daño tisular, todo ello sin toxicidad aparente.
Un nuevo manual para un descubrimiento de antibióticos más inteligente
Para no especialistas, la conclusión clave es que PolyCLOVER muestra cómo la IA y los experimentos automatizados pueden colaborar para descubrir tipos completamente nuevos de antibióticos mucho más rápido que antes. En lugar de depender únicamente del azar y del cribado lento, este enfoque aprende de cada tanda de resultados para centrarse en polímeros que atacan bacterias resistentes a fármacos y que además transportan antibióticos convencionales hacia ellas de forma más eficaz. Si bien se necesita trabajo adicional antes de que cualquiera de estos materiales llegue a la clínica, el estudio ofrece una vía prometedora para reponer nuestro menguante arsenal contra las infecciones resistentes y sugiere una estrategia general para diseñar muchos otros biomateriales inteligentes.
Cita: Wu, Y., Wang, C., Shen, X. et al. Iterative discovery of potent polymeric antibiotics via multi-stage and multi-task learning against antimicrobial resistance. Nat Commun 17, 1878 (2026). https://doi.org/10.1038/s41467-026-68682-z
Palabras clave: resistencia antimicrobiana, antibióticos poliméricos, nanopartículas, aprendizaje automático, bacterias resistentes a fármacos