Clear Sky Science · es
Disrupción diferencial de los lípidos de membrana por los antibióticos lipopeptídicos colistina y turnerciclamicinas
Por qué esto importa para los antibióticos del futuro
Se prevé que las infecciones resistentes a los fármacos causen decenas de millones de muertes cada año a mediados de siglo, y algunos de los agentes más letales son bacterias Gram-negativas que ya resisten muchos antibióticos. La colistina es uno de los pocos fármacos que aún pueden tratar estas infecciones, pero resulta dura para los pacientes y las bacterias están aprendiendo cada vez más a evadirla. Este estudio desentraña cómo actúa la colistina en comparación con una nueva familia de antibióticos naturales llamados turnerciclamicinas, revelando que pequeñas modificaciones químicas pueden generar maneras muy distintas de matar bacterias —y potencialmente medicinas más seguras.
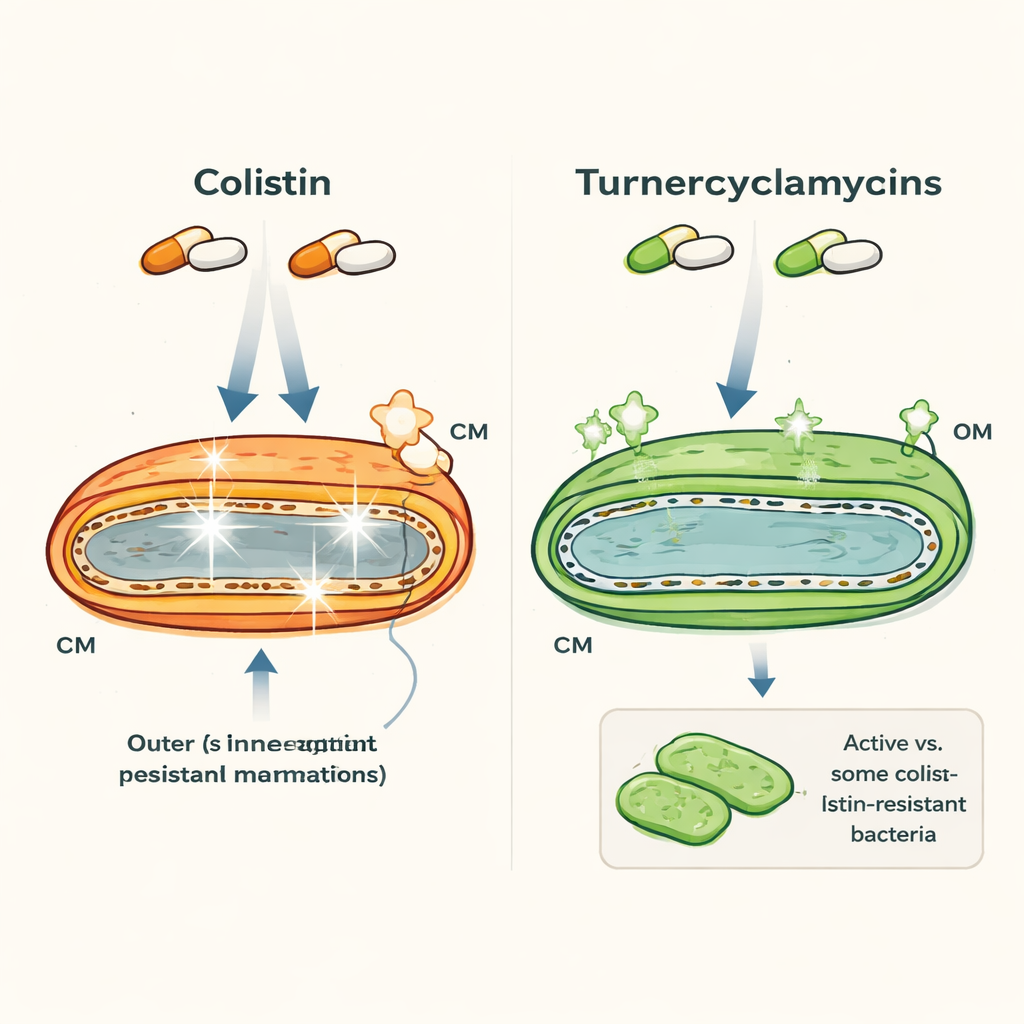
Dos fármacos de aspecto parecido con comportamientos muy distintos
La colistina y las turnerciclamicinas son ambos lipopeptídicos —moléculas que combinan una cola grasa con un anillo peptídico— y ambos se dirigen a bacterias Gram-negativas como Escherichia coli y Acinetobacter. A primera vista parecen similares, pero sus propiedades divergen notablemente. La colistina es un fármaco de último recurso que actúa rápido pero puede dañar los riñones y nervios humanos, y las bacterias llevan cada vez más genes de resistencia como mcr-1. Las turnerciclamicinas, descubiertas en bacterias asociadas a teredos (shipworms), pueden matar muchos de los mismos patógenos, incluidas algunas cepas resistentes a la colistina, pero muestran mucha menos toxicidad en ensayos de laboratorio. Intrigantemente, dos versiones que difieren únicamente por una pequeña extensión de la cola grasa ya muestran patrones de resistencia distintos, lo que sugiere que rasgos estructurales muy sutiles importan.
Cómo la colistina perfora y las turnerciclamicinas actúan con paciencia
Los autores emplearon tintes fluorescentes, experimentos de killing en el tiempo y microscopía electrónica para observar cómo estos fármacos afectan las membranas bacterianas a lo largo del tiempo. La colistina vuelve permeables de forma rápida tanto la membrana externa como la interna (citoplásmica), provocando la muerte celular en pocas horas. Las turnerciclamicinas, en cambio, matan más despacio —tardan de 6 a 10 horas en limpiar completamente los cultivos— y perturban principalmente la membrana externa. Los tintes que se iluminan cuando se rompe la membrana interna mostraron señales fuertes para la colistina pero solo señales modestamente retardadas para las turnerciclamicinas, y las imágenes de alta resolución confirmaron escasos daños visibles en la membrana interna incluso cuando las células morían. Esto indica que las turnerciclamicinas no matan por la vía clásica de “formación de poros” empleada por muchos antibióticos que atacan membranas.
Bloques constructores lipídicos como mandos ocultos
Ambas familias de fármacos dependen en último término de un componente bacteriano llamado lipopolisacárido (LPS), que se sintetiza en la membrana interna y normalmente se exporta a la superficie externa. Cuando los investigadores deshabilitaron pasos tempranos de la biosíntesis de LPS, tanto la colistina como las turnerciclamicinas perdieron actividad; pero cuando bloquearon la maquinaria de transporte que mueve el LPS hacia afuera, los fármacos siguieron funcionando. Esto significa que la existencia de precursores de LPS es esencial, pero su destino final no lo es. Surgió una diferencia clave al medir la unión directamente: la colistina se adhiere al LPS purificado con afinidad micromolar, mientras que las turnerciclamicinas no mostraron unión medible. En lugar de ello, las turnerciclamicinas se vieron fuertemente afectadas por otros lípidos de la membrana. Ciertos fosfolípidos, especialmente la fosfatidilglicerol, podían atenuar o modular su actividad, y los fármacos quedaron fácilmente capturados por vesículas de la membrana externa —pequeñas burbujas lipídicas que las bacterias desprenden.
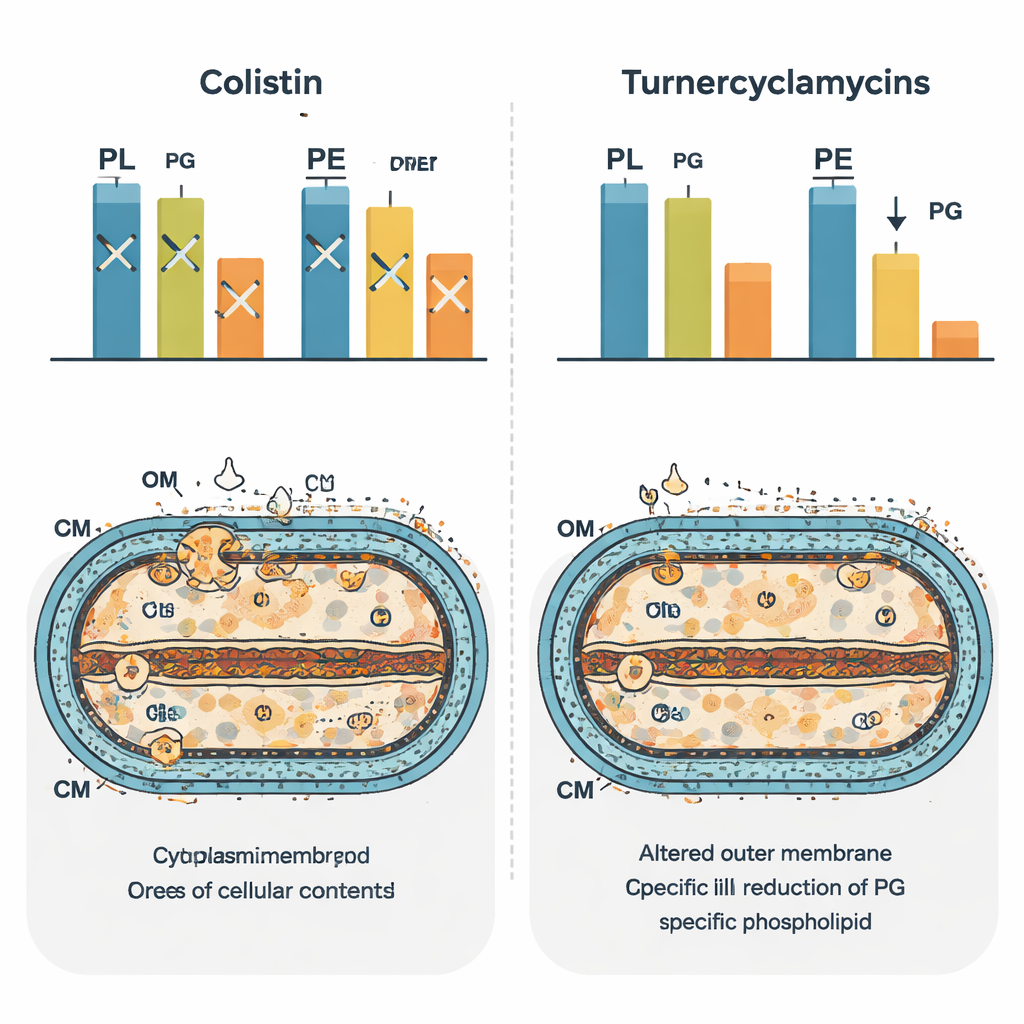
Reprogramar el paisaje lipídico bacteriano
Para ver el impacto más amplio en la célula, el equipo utilizó “fosfolipidómica” basada en espectrometría de masas para catalogar cientos de especies lipídicas después del tratamiento. La colistina produjo un patrón característico de cambios, reflejo de su amplia disrupción de la homeostasis de membrana. Las turnerciclamicinas generaron una firma distinta que se parecía mucho a la de bacterias carentes de una proteína transportadora de lípidos llamada MlaA. En estas células, ciertos lípidos diacil fueron disminuidos y las formas monoacil aumentaron, lo que sugiere que el ciclo y la remodelación normales de los fosfolípidos entre membranas se vieron desequilibrados. Cabe destacar que los niveles de fosfatidilglicerol cayeron en las células tratadas con turnerciclamicinas, lo que refuerza la idea de que este lípido está directamente ligado a su potencia. Los autores proponen que las turnerciclamicinas podrían actuar como imitadores moleculares que atascan las vías que conectan la síntesis o el transporte de ácidos grasos, LPS y fosfatidilglicerol.
Qué significa esto para diseñar mejores fármacos
En términos sencillos, el estudio muestra que la colistina mata rasgando rápidamente ambas capas protectoras de una bacteria Gram-negativa, ayudada por su unión estrecha al LPS, mientras que las turnerciclamicinas actúan más como saboteadores de la cadena de suministro lipídica de la célula. Se infiltran en la membrana externa, perturban gradualmente cómo se producen y reciclan lípidos específicos, y finalmente provocan el fallo del envoltorio celular —sin dañar en exceso la membrana interna. Como este mecanismo más suave y selectivo se vincula a menor toxicidad y a un perfil de resistencia distinto, comprenderlo ofrece una hoja de ruta para diseñar lipopeptídicos de nueva generación. Ajustando finamente características como la longitud y la saturación de la cola grasa, los químicos podrían construir fármacos que preserven tejidos humanos, conserven actividad frente a cepas resistentes a la colistina y se mantengan un paso por delante en la carrera armamentista con las bacterias resistentes a antibióticos.
Cita: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
Palabras clave: resistencia a los antibióticos, bacterias Gram-negativas, colistina, antibióticos lipopeptídicos, lípidos de membrana