Clear Sky Science · es
Base estructural de las conformaciones dinámicas de AP-4 y su asociación con ARF1
Cómo las células clasifican y envían su carga
Cada célula es un almacén bullicioso que clasifica y envía constantemente miles de “paquetes” proteicos a los destinos correctos. Cuando este sistema de reparto falla en las neuronas, el resultado puede ser grave, provocando trastornos del movimiento y del desarrollo cerebral. Este estudio revela cómo una máquina de envío clave, llamada AP-4, cambia de forma y se asocia con una proteína reguladora, ARF1, para cargar mercancía en pequeñas burbujas de transporte y por qué esa flexibilidad es tan importante para la salud neuronal.
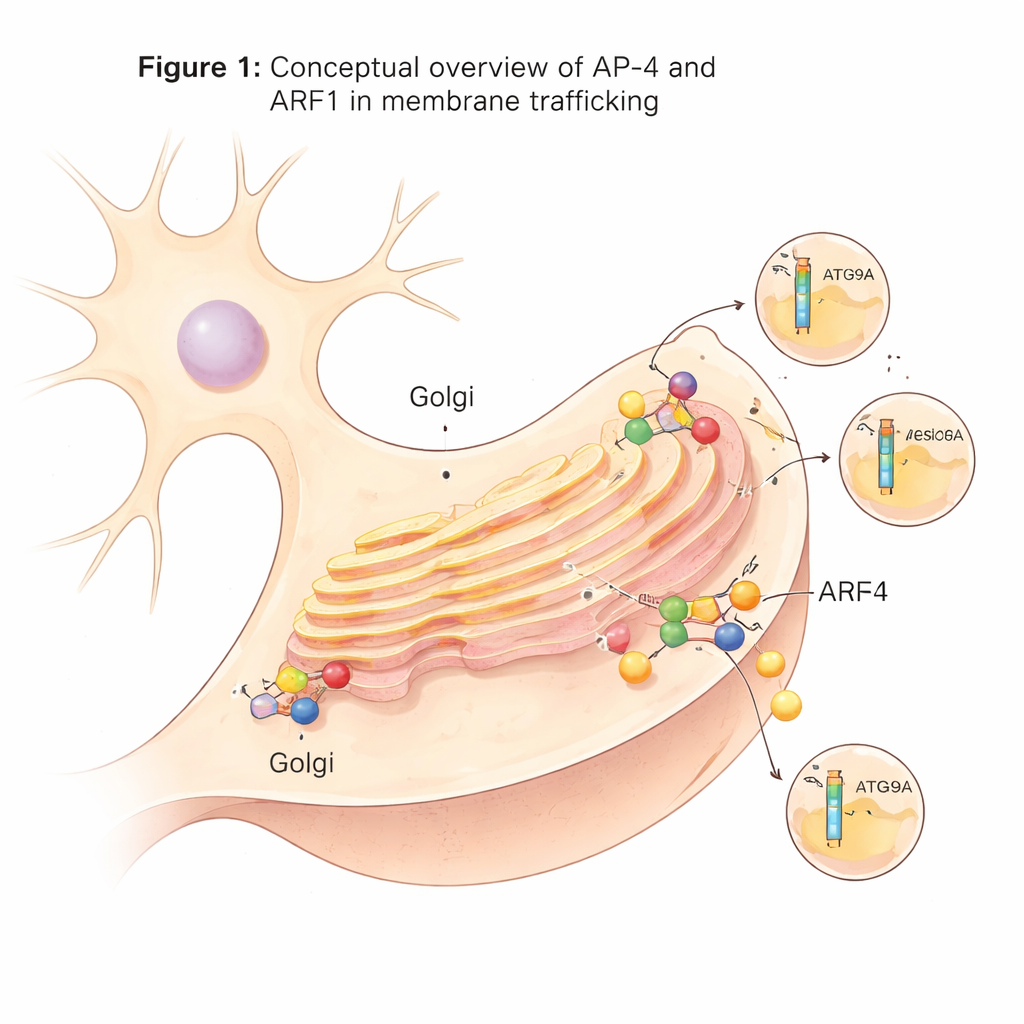
Una máquina de envío especializada en las neuronas
Dentro de las células, muchas vesículas de transporte brotan de una estación central de clasificación conocida como la red trans-Golgi. Estas vesículas dependen de complejos de proteínas adaptadoras, o complejos AP, que actúan como muelles de carga: reconocen proteínas de carga y ayudan a formar vesículas recubiertas a su alrededor. AP-4 es uno de estos adaptadores y es inusual porque, a diferencia de muchos otros, no usa la proteína andamiaje común clatrina. Aunque AP-4 se expresa en muchos tejidos, desempeña un papel especialmente importante en las neuronas. Cuando AP-4 falta o está defectuoso en humanos, cargas cruciales como la proteína relacionada con la autofagia ATG9A y ciertos receptores de glutamato no se desplazan correctamente, provocando una condición grave del neurodesarrollo conocida como síndrome por deficiencia de AP-4.
Un complejo que cambia de forma en reposo
Los autores utilizaron crio–microscopía electrónica, un potente método de imagen capaz de visualizar ensamblajes proteicos grandes, para determinar la estructura tridimensional del complejo “núcleo” de AP-4 en solución. AP-4 está formado por cuatro subunidades que juntas conforman una estructura en forma de cuenco. Descubrieron que AP-4 no permanece en una única forma rígida. En lugar de ello, cambia de forma de manera natural entre una conformación “cerrada”, en la que una subunidad (el dominio C-terminal de la subunidad mediana) queda recogida en el centro del cuenco, y una conformación “abierta”, en la que esa pieza se desplaza hacia fuera y se vuelve muy flexible. Experimentos adicionales de fluorescencia a nivel de una sola molécula mostraron que esta subunidad muestrea al menos tres posiciones —cerrada, parcialmente abierta y totalmente abierta— lo que revela que AP-4 es intrínsecamente dinámico incluso antes de unirse a membranas.
El papel de ARF1: reclutador, no interruptor maestro
Muchos complejos adaptadores emparentados cambian de una forma inactiva a una activa al unirse a pequeñas proteínas reguladoras llamadas ARF. Para ver cómo ocurre esto en AP-4, los investigadores resolvieron estructuras de AP-4 unido a ARF1, una pequeña proteína GTPasa que se ancla a las membranas. Hallaron que ARF1 se adhiere principalmente a una de las subunidades grandes de AP-4 cerca de su extremo N-terminal, de forma similar a otros complejos AP. Sorprendentemente, la unión de ARF1 no desencadena una reordenación estructural drástica en AP-4. Las formas cerrada y abierta siguen coexistiendo y la arquitectura global del complejo permanece en gran medida sin cambios. Ensayos bioquímicos confirmaron que puntos de contacto específicos entre ARF1 y AP-4 son esenciales para el reclutamiento a membranas, pero ARF1 por sí solo no fija a AP-4 en un único estado activo.
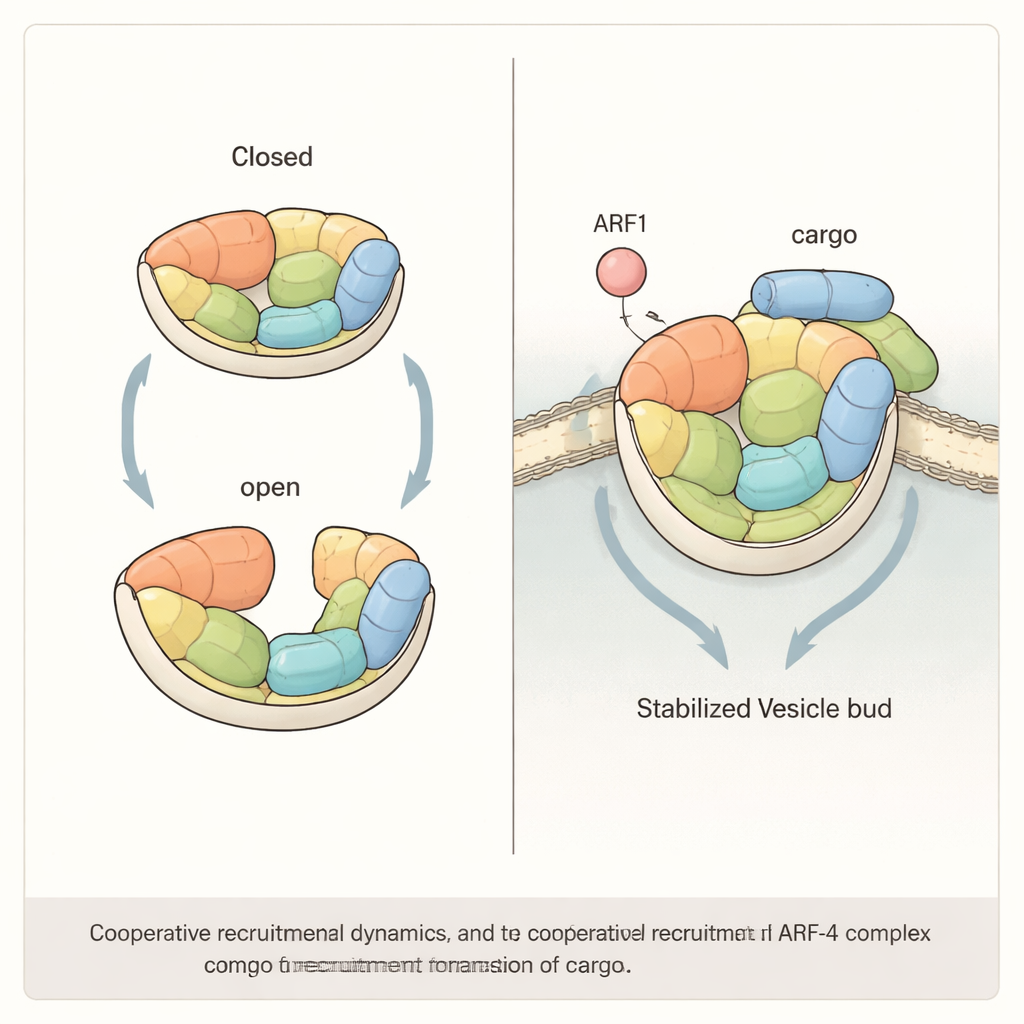
Trabajo conjunto entre regulador y carga
El estudio continúa mostrando que el reclutamiento eficaz de AP-4 a las membranas probablemente requiere la cooperación entre ARF1 y las propias proteínas de carga. Al reconstituir el sistema sobre perlas artificiales y liposomas, los autores observaron que tanto ARF1 como una cola corta de la carga ATG9A pueden atraer AP-4, pero cuando ambos están presentes aumentan la captación de AP-4 mucho más de lo esperado por la suma de sus efectos individuales. Cuando los investigadores introdujeron mutaciones que rigidizaban la estructura de AP-4 —reduciendo su capacidad para alternar entre estados abiertos y cerrados— este efecto sinérgico se perdió. En células humanas que carecían de una subunidad clave de AP-4, restaurar solo versiones “rígidas” mutantes del complejo no consiguió rescatar el tráfico normal de ATG9A desde el Golgi, subrayando que la flexibilidad de AP-4 no es una curiosidad sino un requisito funcional.
Por qué la flexibilidad importa para la salud cerebral
En conjunto, el trabajo presenta a AP-4 como un adaptador que cambia de forma y que muestrea múltiples conformaciones en solución y sobre membranas. En vez de actuar como un interruptor de encendido/apagado, ARF1 sirve como reclutador anclado a membranas que trabaja junto con las proteínas de carga para estabilizar a AP-4 en configuraciones productivas para la formación de vesículas. Alterar este equilibrio —ya sea debilitando la unión de ARF1 o de la carga, o congelando a AP-4 en una sola conformación— perjudica la exportación de carga desde el Golgi y puede contribuir a enfermedades del neurodesarrollo. Al revelar la base estructural del comportamiento dinámico de AP-4, este estudio ofrece un marco para entender los trastornos relacionados con AP-4 y sugiere posibles estrategias futuras para restaurar el tráfico adecuado en neuronas afectadas.
Cita: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Palabras clave: transporte de membrana, complejo adaptador AP-4, ARF1, formación de vesículas, trastorno del neurodesarrollo