Clear Sky Science · es
Las células NK ZNF683+ determinan la sensibilidad a la quimioterapia en carcinoma avanzado de la hipofaringe mediante la remodelación del microambiente inmunitario
Por qué algunos tratamientos quimioterápicos funcionan mejor en ciertos cánceres de garganta
Las personas con carcinoma avanzado de la hipofaringe —un tumor oculto en lo profundo de la garganta— a menudo afrontan quimioterapias agresivas con resultados inciertos. Algunos tumores se reducen notablemente, mientras que otros apenas responden. Este estudio plantea una pregunta simple pero crucial: ¿qué difiere en los tumores que responden bien? Al examinar las células inmunitarias una por una, los investigadores identifican un tipo particular de “célula guardiana” que puede inclinar la balanza entre el éxito y el fracaso de la quimioterapia estándar.
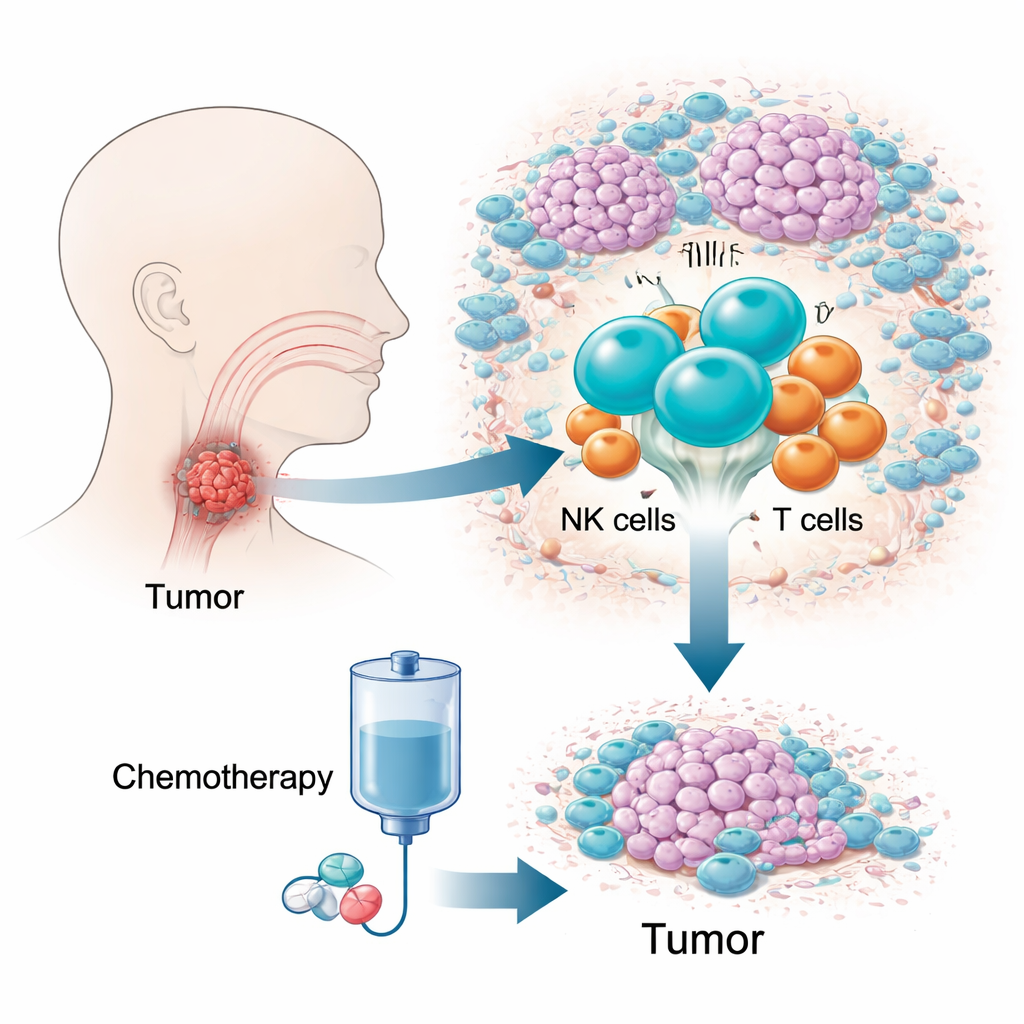
El reto de un cáncer oculto y de difícil tratamiento
El carcinoma escamoso de la hipofaringe es uno de los cánceres de cabeza y cuello más letales, en parte porque crece en una zona estrecha y de difícil exploración y provoca pocos síntomas en etapas tempranas. Muchos pacientes se diagnostican tarde, cuando las opciones son limitadas y la supervivencia a cinco años es baja. Una combinación de fármacos conocida como quimioterapia TPF se usa ampliamente porque puede controlar la enfermedad preservando la laringe. Sin embargo, entre el 10 y el 20 por ciento de los pacientes muestran poca o nula respuesta, perdiendo un tiempo valioso. Las pruebas genéticas tradicionales, que promedian señales de millones de células, han tenido dificultades para explicar esta diferencia, lo que llevó a los autores a centrarse en cambio en el ecosistema vivo de células inmunitarias del tumor.
Leer el paisaje inmunitario del tumor célula a célula
Los investigadores siguieron a 12 pacientes a lo largo del tiempo, recogiendo muestras tumorales antes y después de dos ciclos de quimioterapia TPF y perfilando más de 150.000 células inmunitarias a resolución de célula única. También examinaron a 41 pacientes adicionales para confirmar hallazgos clave mediante imagen y citometría de flujo. Al mapear la actividad génica y el tipo de cada célula, construyeron un atlas detallado del microambiente tumoral: células T, células B, macrófagos, células dendríticas, mastocitos, neutrófilos y células asesinas naturales (NK). Entre todos estos actores destacó un patrón. Antes del tratamiento, los tumores que luego se redujeron tenían muchas más células NK que los que resistieron la terapia, y cuanto mayor era la fracción de células NK, mayor fue la reducción tumoral eventual.
Un subconjunto especial de NK prepara el terreno para las células T
Profundizando, el equipo dividió las células NK en tres grupos según sus características moleculares. Solo uno de ellos, marcado por el factor de transcripción ZNF683 y situado en gran medida en el tejido que rodea los nidos tumorales, se correlacionó fuertemente con una buena respuesta a la quimioterapia. Los pacientes cuyos tumores contenían más de estas células NK ZNF683+ en la línea de base tenían muchas más probabilidades de beneficiarse de TPF. En experimentos con ratones, la eliminación de las NK casi borró por completo el beneficio de la quimioterapia, confirmando que la actividad de las NK no es solo un marcador sino un requisito para un tratamiento eficaz. De manera intrigante, estas NK no actuaban simplemente como asesinas directas del cáncer; sus programas génicos estaban enriquecidos en funciones para guiar y activar a las células T.
Cómo las NK autorizan a las células T con gran capacidad citotóxica
Para entender qué células T eran las más relevantes, los científicos siguieron clones individuales del receptor de células T antes y después del tratamiento. Encontraron que en los respondedores un grupo específico de células T CD8 de tipo “memoria efectora”, enriquecidas en la molécula GZMK, se expandió de forma dramática tras la quimioterapia. Estas células T producían altos niveles de las citocinas tóxicas TNF e interferón gamma sin mostrar un agotamiento profundo, lo que las convierte en asesinas potentes y duraderas. La imagen espacial reveló que, tras el tratamiento, estas células CD8 GZMK+ se agruparon intensamente en los tumores de los respondedores pero no en los de los no respondedores. En ensayos de cocultivo con células humanas, el contacto directo con NK ZNF683+ promovió el crecimiento de este subconjunto CD8 GZMK+, efecto que desapareció cuando las células se separaron por una barrera.
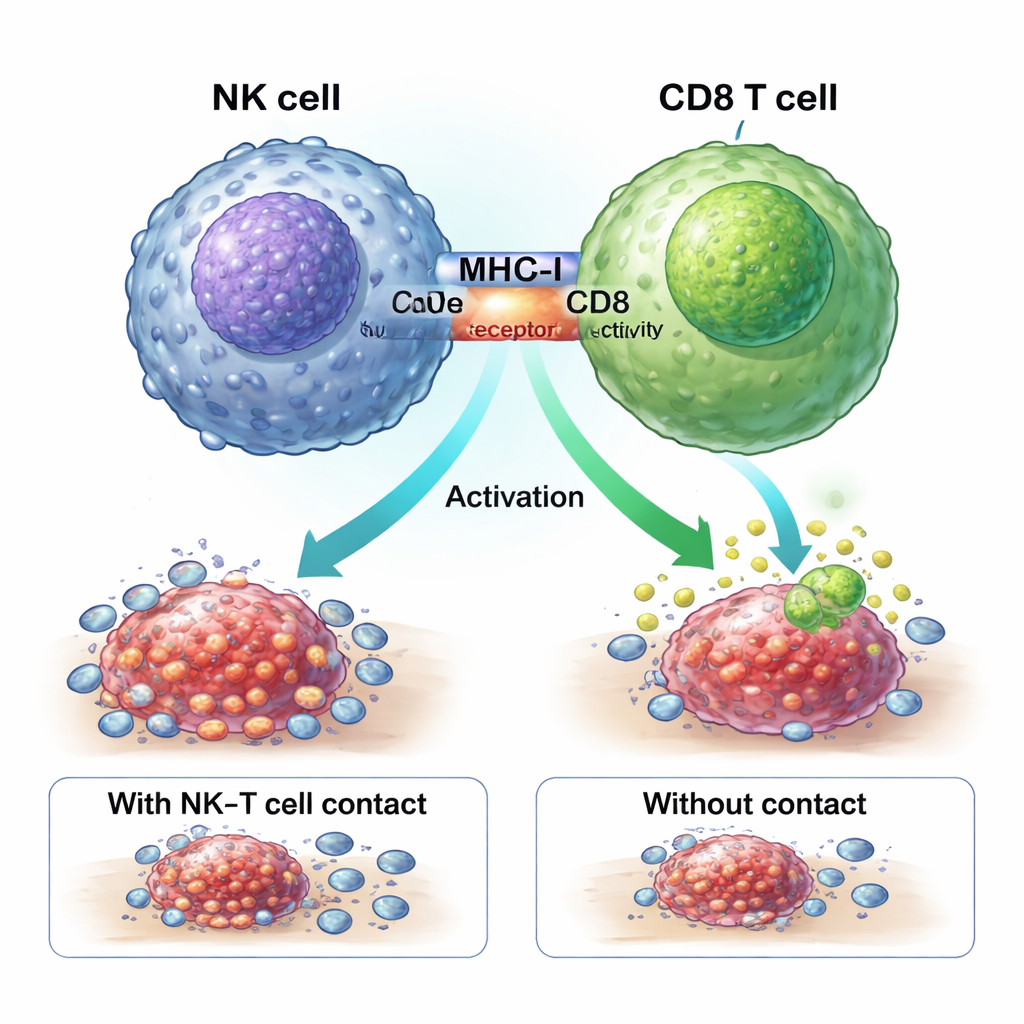
Un apretón físico de manos que activa a los combatientes tumorales
El estudio muestra que las NK ZNF683+ aumentan la respuesta a la quimioterapia mediante un “apretón de manos” físico con las células T CD8. Moléculas llamadas MHC-I en la superficie de las NK interaccionan con receptores CD8 en las T en una zona de contacto estrecho, o sinapsis inmunitaria. Bloquear MHC-I impidió que las NK generaran las potentes células CD8 GZMK+. En ratones especialmente diseñados para carecer de ZNF683 solo en las NK, estas células expresaron menos MHC-I y fueron mucho peores activando a las CD8, reforzando la idea de que ZNF683 programa a las NK para convertirse en entrenadoras efectivas de las células T más que en simples ejecutoras.
Qué significa esto para los pacientes
Para lectores no especializados, el mensaje clave es que no todas las células inmunitarias en un tumor son iguales. Este trabajo identifica un subconjunto particular de células NK como exploradoras avanzadas que preparan el campo de batalla antes de que comience la quimioterapia. Los tumores ricos en estas células están listos para desatar oleadas de potentes células T CD8 cuando los fármacos actúan, lo que conduce a una reducción tumoral mucho mayor. Medir la abundancia de este eje NK–T antes del tratamiento podría ayudar a los médicos a predecir quién se beneficiará de la quimioterapia TPF y quién podría necesitar terapias alternativas o adicionales. En el futuro, tratamientos que aumenten o imiten a estas NK ZNF683+ podrían convertir cánceres de hipofaringe resistentes en otros mucho más sensibles a la quimioterapia estándar.
Cita: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
Palabras clave: cáncer de hipofaringe, resistencia a la quimioterapia, células asesinas naturales, microambiente tumoral inmunitario, células T CD8