Clear Sky Science · es
Construcción selectiva de enlaces N‑N inducida por fotoexcitación mediante la liberación y transferencia de nitrenos
Iluminando una nueva manera de unir átomos de nitrógeno
Los átomos de nitrógeno están en el corazón de muchos fármacos, agentes de protección de cultivos y materiales avanzados. Los químicos son muy hábiles para unir nitrógeno con carbono, pero conectar directamente dos átomos de nitrógeno es mucho más difícil. Este estudio presenta un método alimentado por luz y sin metales para enlazar átomos de nitrógeno de forma controlada, abriendo una vía más simple hacia una amplia gama de moléculas útiles.
Por qué es difícil unir nitrógeno con nitrógeno
Muchos productos naturales y fármacos contienen pares de átomos de nitrógeno unidos entre sí, un motivo que puede ajustar cómo se comporta una molécula en el cuerpo o en materiales. Las vías existentes para construir estas unidades N–N suelen partir de fragmentos de nitrógeno–nitrógeno ya preparados, como hidrazinas o compuestos de diazo, y luego modificarlos paso a paso. Forjar directamente el enlace N–N desde aminas simples es atractivo pero complicado: el nitrógeno es bastante electronegativo, por lo que dos átomos de nitrógeno no forman de forma natural un enlace estable y no polar. Los éxitos previos han dependido en gran medida de catalizadores de metales de transición y a menudo funcionan solo para familias estrechas de moléculas, lo que limita su utilidad en la química de descubrimiento.
Usar luz para domar a un intermediario reactivo
Los autores recurrieron a los nitrenos, especies de nitrógeno altamente reactivas y de vida corta que, en principio, pueden insertarse en otros enlaces. La química tradicional de nitrenos suele necesitar catalizadores metálicos y puede sufrir reacciones secundarias porque los nitrenos son muy energéticos. El equipo se preguntó si podrían generar nitrenos con luz de una forma más suave y controlada, sin metales, y luego usarlos para enlazar aminas simples en productos que contengan N–N. Su idea clave fue emplear sulfiliminas, una familia de moléculas fáciles de modificar y que absorben en el ultravioleta y en el visible cercano. Al iluminarse, estas sulfiliminas pueden fragmentarse liberando un fragmento de nitreno mientras se recupera un subproducto benigno que contiene azufre.
Una receta amplia y libre de metales para pares de nitrógeno
Tras pruebas sistemáticas, los investigadores identificaron una sulfilimina concreta que, bajo luz de 365 nanómetros en cloroformo, reacciona eficientemente con muchas aminas para dar productos hidrazida —moléculas que presentan un enlace N–N recién formado junto a un grupo carbonilo. Optimizaron factores como la estructura de la sulfilimina, el solvente y la intensidad de la luz para favorecer el producto deseado frente a subproductos comunes como las ureas. En estas condiciones suaves, una amplia variedad de aminas, incluidas tipos aromáticos y alifáticos y variantes cíclicas, se acoplaron con éxito. También demostraron que muchas sulfiliminas diferentes, que portan grupos acilo aromáticos y alifáticos y grupos sulfónico, participan bien, produciendo docenas de productos distintos con enlace N–N. Es importante que el método pueda aplicarse en etapas tardías de una síntesis para modificar moléculas complejas y biológicamente activas, como fármacos antiinflamatorios comunes y bloques de construcción quirales, demostrando su practicidad para la química medicinal y de materiales.
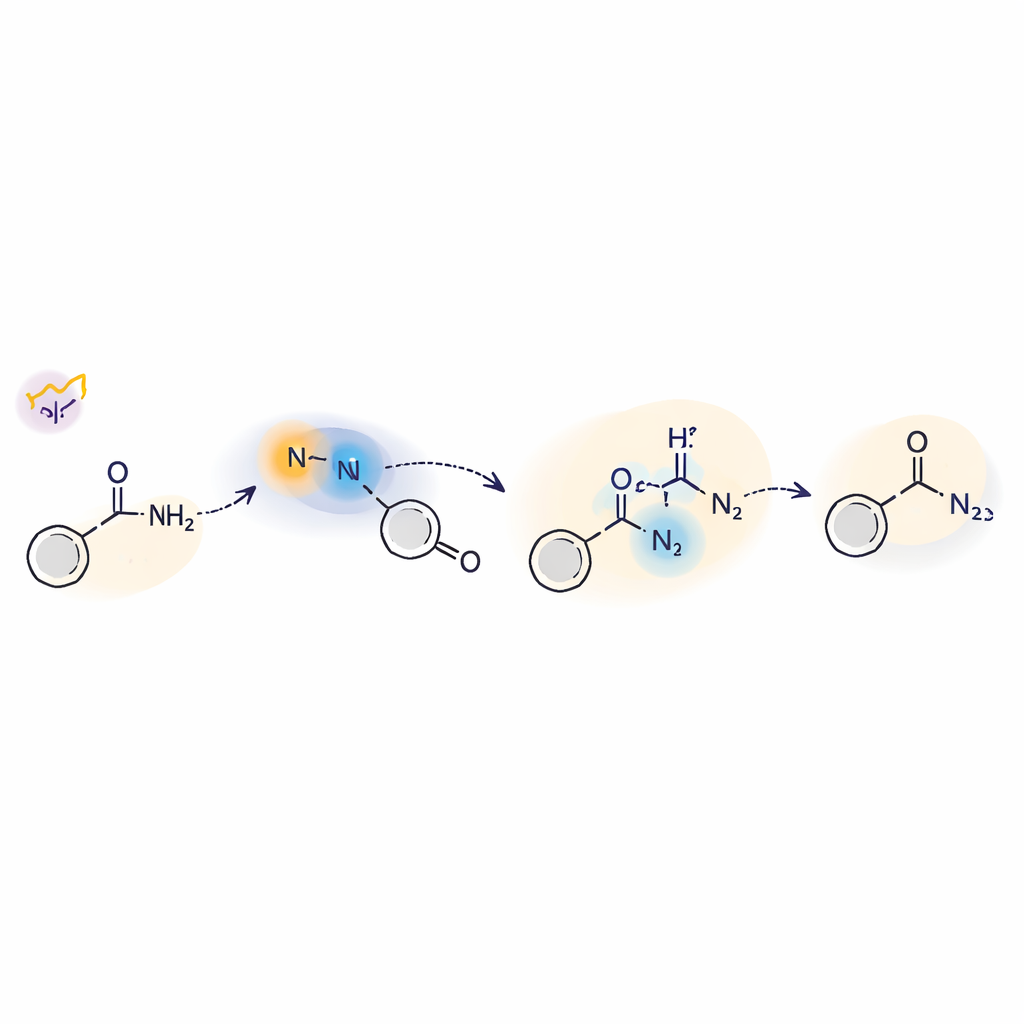
Escrutando el mecanismo del paso impulsado por la luz
Para entender cómo funciona esta química activada por luz, el equipo combinó experimentos y teoría. Usaron trampas radiculares, etiquetado isotópico y resonancia paramagnética electrónica para mostrar que intermedios de nitreno libre y radicales centrados en nitrógeno aparecen durante la reacción. La espectroscopía láser resuelta en el tiempo reveló dos formas clave del nitreno: un estado triple de vida corta y un estado singlete de vida más larga. La forma singlete reacciona directamente con las aminas mediante una especie de ataque nucleofílico, mientras que el triplete puede participar en pasos de transferencia de átomos de hidrógeno. Cálculos computacionales apoyaron un mecanismo en el que la luz excita la sulfilimina, su enlace azufre–nitrógeno se rompe y el nitreno resultante interactúa con la amina a través de rutas singlete y triplete antes de asentarse en la estructura final de la hidrazida.
Qué significa esto para moléculas futuras
Este trabajo muestra que sulfiliminas cuidadosamente diseñadas pueden actuar como “depósitos de nitreno” que liberan unidades reactivas de nitrógeno bajo demanda con luz, sin la ayuda de metales. Aprovechando tanto las personalidades singlete como triplete de los nitrenos y manteniendo su concentración baja, el método logra la formación selectiva de enlaces N–N en una amplia gama de bloques de construcción. Para los no especialistas, la conclusión es que los químicos disponen ahora de una forma más simple, limpia y flexible de coser átomos de nitrógeno, lo que podría acelerar la creación de nuevos fármacos, agroquímicos y materiales ricos en nitrógeno.
Cita: Yu, M., Feng, J., Wang, X. et al. Photo-induced selective N-N bond construction via harnessing nitrene release and transfer. Nat Commun 17, 2084 (2026). https://doi.org/10.1038/s41467-026-68674-z
Palabras clave: química de nitrenos, reacciones fotoinducidas, formación de enlaces N–N, sulfiliminas, hidrazidas