Clear Sky Science · es
Fotosíntesis de glicina mediante acoplamiento C−N de plástico residual y nitrato sobre un catalizador diatómico Pd−B
Convertir la basura en bloques básicos de la vida
Botellas de plástico, envases de comida y ropa de poliéster están por todas partes, y lo mismo ocurre con los residuos que generan. Al mismo tiempo, muchas fábricas vierten aguas residuales cargadas de nitratos que pueden contaminar ríos y mares. Este estudio muestra cómo abordar ambos problemas a la vez: utilizando la luz solar y un catalizador especialmente diseñado para convertir plástico desechado y nitrato en glicina, un aminoácido simple ampliamente usado en alimentación, medicina y agricultura.
Por qué importan la glicina y los residuos
La glicina es uno de los bloques básicos de las proteínas y se produce en escalas de cientos de miles de toneladas al año. Los métodos industriales convencionales, especialmente el proceso clásico de Strecker, dependen de compuestos tóxicos como el cianuro y de condiciones de reacción severas, lo que plantea problemas de seguridad y medioambientales. Mientras tanto, la producción global de PET—empleado en botellas, textiles y embalajes—supera los 100 millones de toneladas anuales, y más del 80 % acaba en vertederos o en el medio ambiente. Cuando el PET se descompone químicamente, uno de los productos es el etilenglicol, un líquido de bajo valor que resulta caro de purificar. Los autores plantean una pregunta simple: en lugar de tratar el etilenglicol y el nitrato como residuos, ¿podrían convertirse en materias primas para producir glicina valiosa usando solo la luz solar?
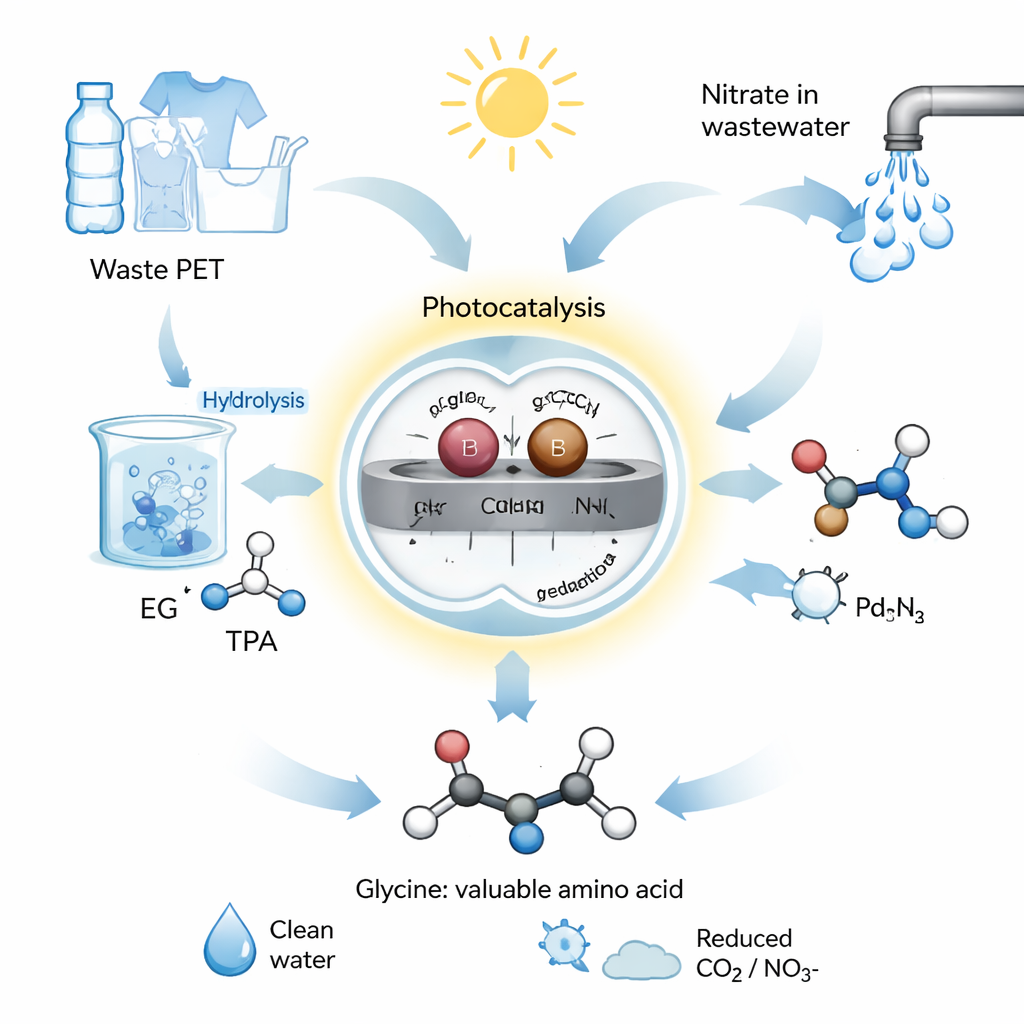
Un atajo químico impulsado por el sol
El equipo diseñó un sistema fotocatalítico, es decir, que utiliza luz para impulsar reacciones químicas. Construyeron un catalizador a partir de nitruro de carbono gráfico, un semiconductor, y anclaron pares de átomos individuales de paladio (Pd) y boro (B) en su superficie. Estos átomos emparejados actúan como un equipo microscópico de dos personas, cada uno manejando una mitad diferente de la química. En su proceso, los residuos de PET se hidrolizan primero—se separan en agua alcalina—para liberar etilenglicol. Este etilenglicol y el nitrato procedente de aguas residuales se colocan luego en agua con el catalizador Pd–B y se exponen a luz solar simulada o natural. Bajo estas condiciones suaves, el sistema convierte la mezcla en glicina con un rendimiento alto y una selectividad superior al 92 %, lo que significa que se forman muy pocos subproductos no deseados.
Cómo funciona el dúo atómico
El éxito del catalizador depende de cómo gestiona los intermedios de reacción de corta duración. Los sitios de boro en la superficie son "ricos en huecos" (hole‑rich), lo que significa que aceptan con facilidad carga positiva cuando el material absorbe luz. En estos sitios de B, el etilenglicol se oxida de forma suave—se le quitan hidrógenos—para formar glicolaldehído, una molécula inestable que normalmente tiende a sobreoxidarse hasta ácidos o incluso dióxido de carbono. Los sitios de paladio, en contraste, son "ricos en electrones". Utilizan los electrones generados por la luz para reducir el nitrato paso a paso hasta amonio o amoníaco. El paso clave es un acoplamiento carbono–nitrógeno entre el glicolaldehído y estas especies nitrogenadas para formar etanolamina, que luego se oxida más, de nuevo principalmente en los sitios de B, dando como resultado la glicina. Al estabilizar el glicolaldehído el tiempo justo para que reaccione y al mantener separados espacialmente electrones y huecos, el par Pd–B dirige la química lejos de reacciones laterales ineficientes y hacia el aminoácido deseado.
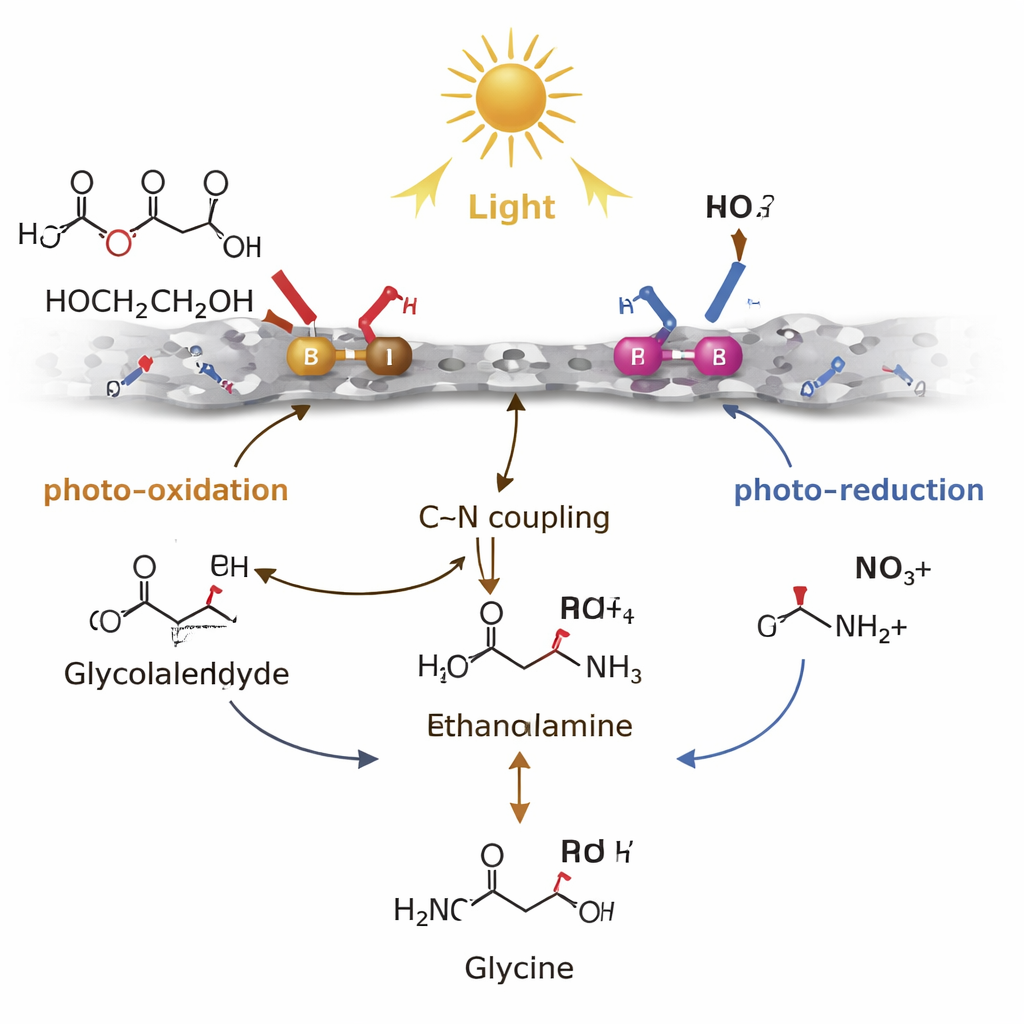
Del mecanismo de laboratorio a residuos del mundo real
Los investigadores confirmaron cada parte de esta vía con un conjunto de técnicas, rastreando radicales, intermedios y productos nitrogenados en tiempo real. Compararon distintos materiales y metales catalíticos y encontraron que los soportes de g‑C3N4 con pares aislados Pd–B ofrecían el mejor rendimiento, alcanzando tasas de producción de glicina de 2,9 milimoles por gramo de catalizador por hora. El catalizador permaneció activo tras ciclos repetidos y su estructura se mantuvo estable. De forma importante, el equipo fue más allá de los reactivos de laboratorio puros: demostraron la producción de glicina a escala de gramos partiendo de PET posconsumo real—polvo, botellas, ropa, bolsas y más—combinado con soluciones de nitrato e incluso aguas residuales complejas. También mostraron que alcoholes relacionados procedentes de biomasa, como el glicerol, pueden servir como fuentes alternativas de carbono, ampliando la relevancia del enfoque.
Una vía ventajosa para residuos y clima
Para acercar el concepto a la práctica, los autores probaron su proceso bajo luz solar natural concentrada mediante una sencilla lente de Fresnel. El sistema produjo consistentemente glicina con alta selectividad, y los modelos sugieren que su ampliación podría evitar emisiones sustanciales de dióxido de carbono y prevenir la descarga de nitratos al medio ambiente. En términos simples, este trabajo describe una forma de convertir montones de plástico usado y agua contaminada en un aminoácido útil, usando solo luz y un catalizador afinado a nivel atómico. Aunque quedan desafíos de ingeniería antes de su despliegue industrial, el estudio subraya cómo el diseño de catalizadores a escala atómica puede convertir dos grandes corrientes de residuos en un único producto químico valioso.
Cita: Ya, Z., Li, M., Fu, D. et al. Glycine photosynthesis via C−N coupling of waste plastic and nitrate over diatomic Pd−B catalyst. Nat Commun 17, 1887 (2026). https://doi.org/10.1038/s41467-026-68666-z
Palabras clave: glicina, reciclaje de plástico, fotocatálisis, aguas residuales con nitrato, catalizadores monoatómicos