Clear Sky Science · es
Regulación del ensamblaje del adaptador AP1 por la chaperona ambidiestra MEA1
Por qué importa este ayudante celular oculto
Dentro de cada célula humana, miles de pequeños paquetes transportan proteínas hasta donde se necesitan o hacia el “centro de reciclaje” celular para su degradación. Este tráfico mantiene nuestras células sanas y controla nuestras defensas inmunitarias. El artículo resumido aquí revela una proteína previamente enigmática, llamada MEA1, que resulta esencial para construir una de las máquinas clave de clasificación que cargan esos paquetes. Entender cómo funciona MEA1 ayuda a explicar cómo las células controlan cargas importantes, incluidas moléculas que activan o desactivan respuestas antivirales.
Control del tráfico en el centro de envíos de la célula
Gran parte de la actividad de envío de la célula pasa por una estructura llamada el aparato de Golgi, una pila de sacos aplanados que actúa como una oficina central de correos. Desde el Golgi, las cargas pueden enviarse a la superficie celular para su uso o redirigirse a compartimentos internos para su degradación. Un complejo proteico conocido como AP1 ocupa el centro de esta ruta. AP1 reconoce etiquetas en las proteínas cargadas, ayuda a curvar la membrana y recluta una cubierta externa de clatrina para formar pequeñas vesículas de transporte. Sin un AP1 correctamente ensamblado, cargas cruciales se acumulan en lugares incorrectos y las rutas de señalización normales, incluidas las vinculadas a la inmunidad, pueden verse alteradas. 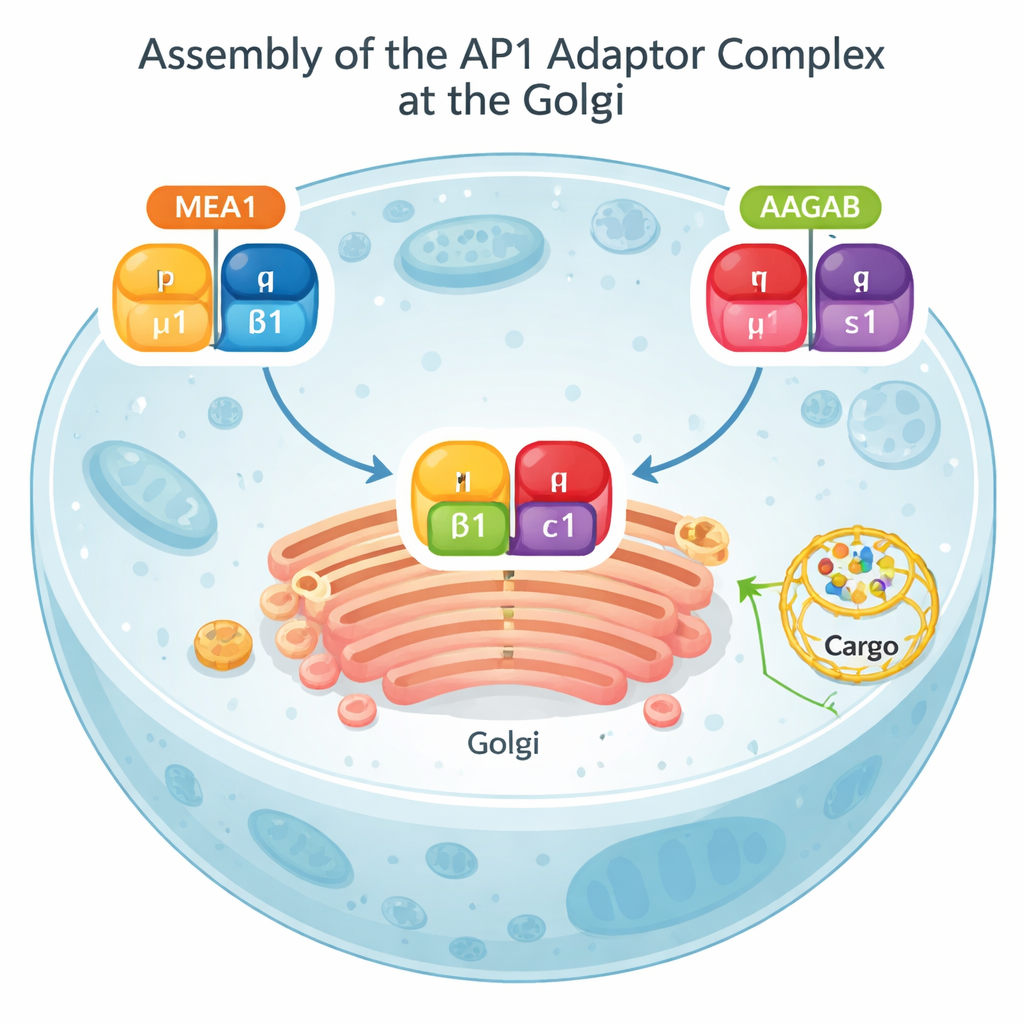
Encontrar a un trabajador ensamblador perdido
Los autores se propusieron identificar proteínas que se asocian físicamente con AP1 y que podrían ayudar en su ensamblaje. Buscaron en una gran base de datos de interacciones proteicas, descartaron candidatos poco probables y luego usaron una herramienta de inteligencia artificial, AlphaFold, para predecir cómo las proteínas restantes podrían contactar las distintas partes de AP1. Esta búsqueda destacó a MEA1, una proteína pequeña y previamente no caracterizada presente en muchos tejidos. Experimentos posteriores en células humanas confirmaron que MEA1 se une a dos subunidades específicas de AP1, conocidas como μ1 y β1, tanto cuando se prueban por separado como en sus formas naturales y no modificadas.
MEA1 mantiene AP1 intacto y el tráfico celular en movimiento
Para investigar qué hace realmente MEA1, los investigadores eliminaron el gen MEA1 en líneas celulares humanas. Cuando faltaba MEA1, las cuatro piezas de AP1 se vieron drásticamente reducidas y los puntos característicos de AP1 cerca del Golgi casi desaparecieron. Esta pérdida tuvo consecuencias funcionales claras. Una carga de AP1, el receptor de folato FOLR1, se acumuló en la superficie celular en lugar de ser enviada hacia el interior, una señal de clasificación defectuosa por AP1. Otra carga, la proteína de señalización inmune STING, ya no se empaquetó de forma eficiente en vesículas dirigidas a los lisosomas, los centros de reciclaje de la célula. Como resultado, STING activado y su quinasa asociada TBK1 permanecieron a niveles elevados, lo que indica que el “interruptor de apagado” de esta vía antiviral no funcionaba correctamente. Reintroducir MEA1 restauró los niveles de AP1 y corrigió estos defectos de tráfico.
Una chaperona con dos manos y un proceso de ensamblaje por colisión
Pruebas bioquímicas y modelos de AlphaFold revelaron que MEA1 actúa como una chaperona de ensamblaje “ambidiestra”: su porción frontal sujeta la subunidad μ1, mientras que su porción trasera sujeta β1. Por sí solas, μ1 y β1 son inestables y tienden a agregarse o a ser destruidas; al unirse a MEA1, se vuelven solubles y están listas para ensamblarse. Otra chaperona conocida, AAGAB, realiza un trabajo paralelo para las otras dos subunidades de AP1, γ y σ1. Cuando los complejos MEA1–μ1–β1 y AAGAB–γ–σ1 se encuentran, sus subunidades se combinan en un adaptador AP1 completo de cuatro partes. En ese punto, ambas chaperonas se desprenden y regresan al fluido celular, mientras que el AP1 recién formado se dirige a las membranas para realizar su función de clasificación. Este mecanismo de “colisión de chaperonas duales” muestra que el ensamblaje de AP1 está cuidadosamente orquestado y no dejado al azar.
Lecciones más amplias sobre el control de calidad celular
Más allá de AP1, el estudio sugiere una estrategia más general que las células podrían usar para construir muchas máquinas proteicas grandes. MEA1 también puede ayudar de forma débil a otro complejo adaptador llamado AP2, y junto con AAGAB y una tercera chaperona llamada CCDC32, ilustra una vía más amplia que los autores denominan “Ensamblaje de Proteínas Adaptadoras asistido por Chaperonas”. En este esquema, chaperonas especializadas estabilizan subunidades frágiles, acercan los pares correctos y bloquean temporalmente los sitios de unión de cargas hasta que el complejo está completamente formado y es seguro desplegarlo. 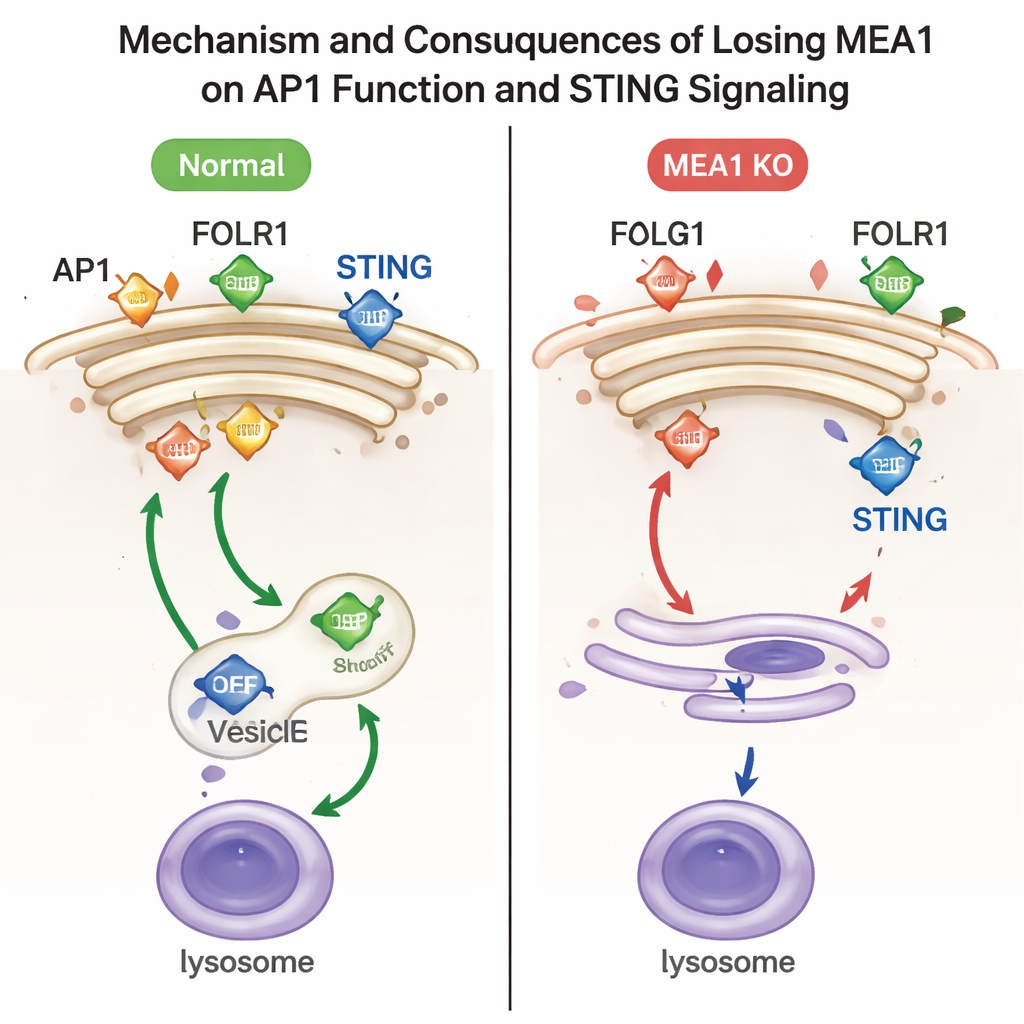
Qué significa esto para la salud y la enfermedad
Para el público no especializado, la conclusión principal es que MEA1 es un trabajador crucial entre bambalinas que ayuda a ensamblar AP1, una máquina de clasificación central en nuestras células. Cuando MEA1 está ausente, AP1 se desintegra, se forman atascos de tráfico y reguladores importantes como STING no se apagan correctamente. Esta nueva comprensión podría, en última instancia, ayudar a explicar ciertos trastornos inmunitarios u otras enfermedades vinculadas al tráfico proteico defectuoso, y revela un principio general sobre cómo las células construyen de forma segura máquinas moleculares complejas a partir de piezas inestables.
Cita: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
Palabras clave: transporte de proteínas, proteína adaptadora AP1, chaperonas moleculares, señalización STING, biología celular