Clear Sky Science · es
Reconocimiento molecular de la tiroglobulina por sortilina
Cómo las células tiroideas deciden cuándo liberar hormona
Las hormonas tiroideas ayudan a ajustar nuestro “termostato” metabólico, influyendo en todo, desde la frecuencia cardíaca hasta la temperatura corporal. Estas hormonas se sintetizan y almacenan dentro de una proteína gigante llamada tiroglobulina. Este estudio revela cómo otra proteína, la sortilina, ayuda a las células tiroideas a elegir qué forma de tiroglobulina internalizar para que la hormona pueda liberarse al torrente sanguíneo, una decisión que en última instancia determina la cantidad de hormona tiroidea disponible para el organismo.
Una proteína de almacenamiento a la espera de ser procesada
La tiroglobulina es una proteína enorme con forma de Y, producida y secretada por las células tiroideas dentro de una masa gelatinosa llamada coloide. Allí actúa tanto como materia prima como almacén para la hormona tiroidea: determinados bloques de construcción (aminoácidos) dentro de la tiroglobulina se modifican químicamente con yodo para convertirse en hormonas tiroideas, aún integrados en la proteína mayor. Para liberar realmente estas hormonas, la tiroglobulina debe ser recuperada por la célula, fragmentada dentro de compartimentos de reciclaje denominados lisosomas, y sus porciones hormonales transportadas hacia la sangre.
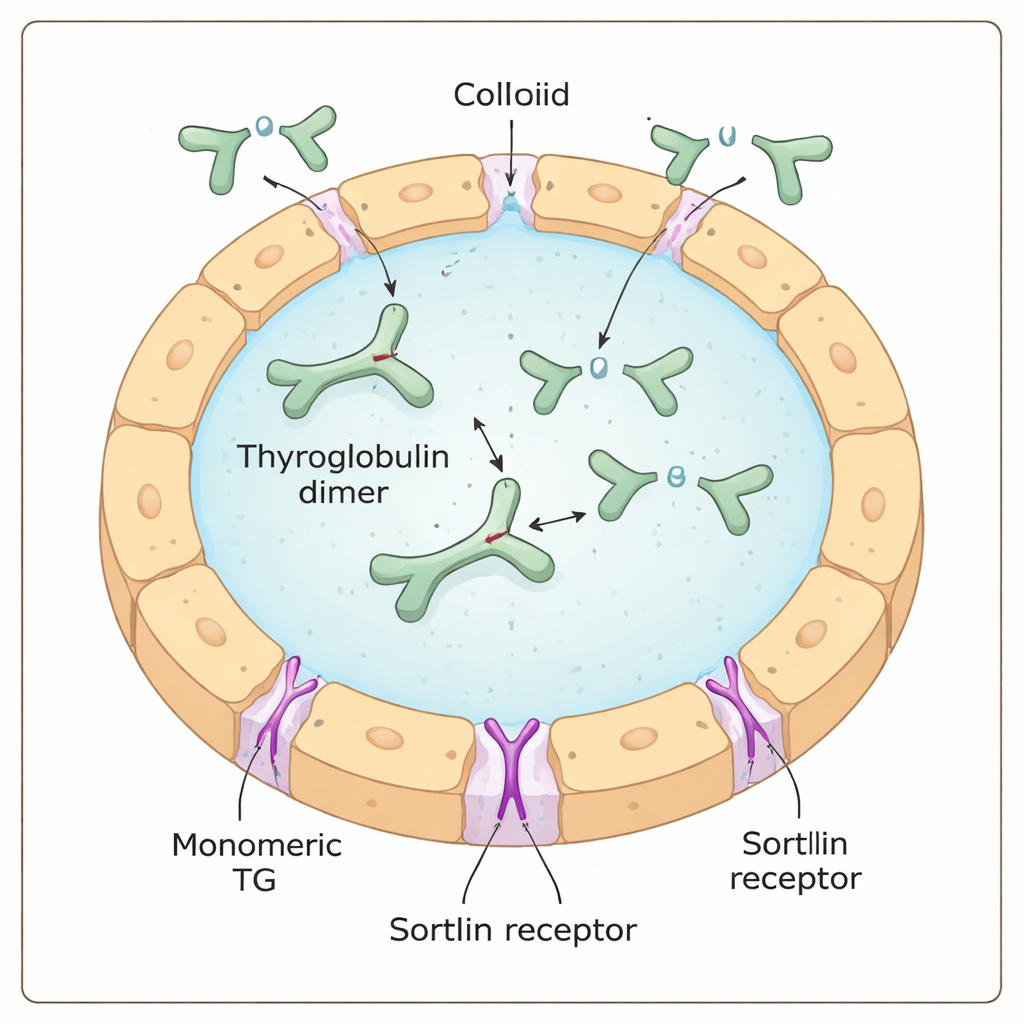
Un portero celular con una preferencia oculta
Se ha propuesto a la sortilina como uno de los “porteros” que se unen a la tiroglobulina en la superficie celular y la guían hacia el interior. Trabajos previos sugerían que la sortilina prefería la tiroglobulina altamente iodada, insinuando que el receptor podía percibir directamente el contenido de yodo. Usando una combinación de pruebas bioquímicas, medidas de masa de moléculas únicas y experimentos de captación en células, los autores encontraron en cambio que la sortilina prefiere con fuerza la forma monomérica (de unidad simple) de la tiroglobulina frente a su forma más común apareada, la dimérica. Cuanto más monómero había en una muestra, con más eficiencia formaba complejos con sortilina y era internalizada por las células tiroideas, independientemente de la cantidad de yodo que contuviera.
Acercándose al punto de contacto
Para entender esta preferencia a nivel atómico, el equipo recurrió a microscopía crioelectrónica de alta resolución y espectrometría de masas tras entrecruzamiento. Estos métodos mostraron que la sortilina reconoce una cola corta y flexible en el extremo C-terminal (un extremo) de la tiroglobulina monomérica. Esta cola se introduce en una cavidad central de la sortilina con forma de hélice de diez palas, acoplándose en dos pequeños “puntos calientes” en su interior. De manera llamativa, en la forma dimérica de la tiroglobulina, parte de la región alrededor de esa cola queda enterrada y la sortilina no puede acceder a ella, lo que explica por qué el dímero es un mal socio. Los datos sugieren que el recorte o aflojamiento extracelular de la tiroglobulina —mediante la degradación proteica natural— ayuda a convertir dímeros en monómeros que la sortilina puede captar.
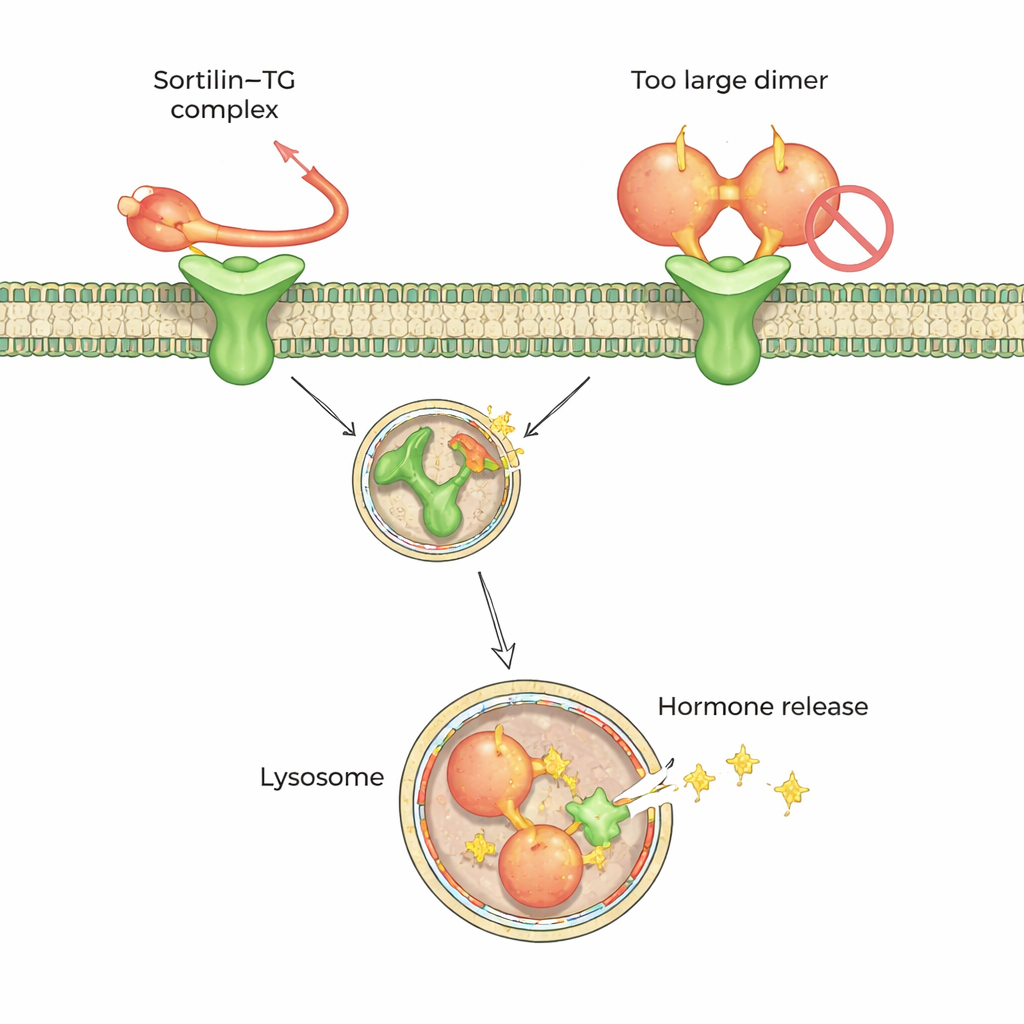
Un código de acoplamiento compartido por muchas proteínas cargadas
La sortilina no es solo una proteína tiroidea; participa en el transporte de muchas moléculas diferentes por el organismo, incluidos factores relacionados con enfermedades cardíacas y trastornos cerebrales. Combinando su trabajo estructural con herramientas avanzadas de predicción de estructuras como AlphaFold y AlphaPulldown, los investigadores compararon cómo docenas de socios conocidos de la sortilina podrían unirse a su cavidad en forma de hélice. Encontraron un patrón recurrente: muchos cargos presentan un segmento peptídico no estructurado de unas veinte aminoácidos que encaja en el mismo bolsillo que la cola de la tiroglobulina, a veces en la misma dirección que un péptido cerebral conocido llamado neurotensina y a veces en la dirección opuesta. A pesar de la orientación invertida, estos péptidos comparten rasgos similares: un grupo ácido o con carga negativa en un extremo, un residuo aromático voluminoso en el otro y un tramo flexible, a menudo rico en prolina, entre ambos.
Por qué el yodo importa menos que la forma
Puesto que el contacto clave entre sortilina y tiroglobulina es esa cola flexible, los autores probaron si añadir yodo extra a una tirosina formadora de hormona en la cola alteraría la unión. No fue así: un péptido sintético que llevaba una hormona tiroidea ya formada se comportó casi idénticamente al no modificado. El modelado mostró que el anillo iodinado sobresale hacia el solvente sin crear nuevos contactos estrechos. Junto con los experimentos de captación, esto respalda una visión revisada: la sortilina no “cuenta” átomos de yodo en la tiroglobulina. En su lugar, percibe si la proteína se ha relajado o se ha degradado parcialmente lo suficiente como para exponer su forma monomérica y la cola de la manera adecuada.
Qué significa esto para la salud tiroidea
Para el no especialista, el mensaje central es que la liberación de hormona tiroidea está controlada menos por un sensor interno de yodo y más por un control mecánico sobre la forma y la flexibilidad de la proteína. La sortilina actúa como un escáner en la superficie celular, buscando moléculas de tiroglobulina que se hayan aflojado o recortado en monómeros, y luego las atrae hacia el interior para la liberación final de la hormona y el reciclado del yodo. Este trabajo aclara un paso clave en la biología de la hormona tiroidea y sugiere que fármacos diseñados para bloquear la sortilina —ahora explorados para otras enfermedades— podrían alterar de forma involuntaria el manejo de la hormona tiroidea al perturbar este paso de reconocimiento.
Cita: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Palabras clave: hormona tiroidea, tiroglobulina, sortilina, transporte de proteínas, endocitosis