Clear Sky Science · es
El helicio puente de Cas12a es un regulador alostérico de la formación del R-loop y de la activación de RuvC
Por qué importa esto para la edición génica
Muchas herramientas poderosas de edición génica, incluidas las que sustentan terapias emergentes y pruebas diagnósticas rápidas, dependen de proteínas CRISPR que cortan el ADN en sitios seleccionados. Pero si estas tijeras moleculares cortan en el lugar equivocado, pueden provocar efectos secundarios dañinos. Este estudio diseca una pequeña pieza móvil dentro del editor Cas12a, llamada helicio puente, y muestra cómo sus cambios de forma actúan como un interruptor interno de seguridad que enlaza el reconocimiento correcto del objetivo con el corte del ADN. Comprender este interruptor ofrece una hoja de ruta para diseñar herramientas CRISPR que sean a la vez precisas y más seguras para aplicaciones médicas y biotecnológicas.
Una pinza molecular con piezas móviles
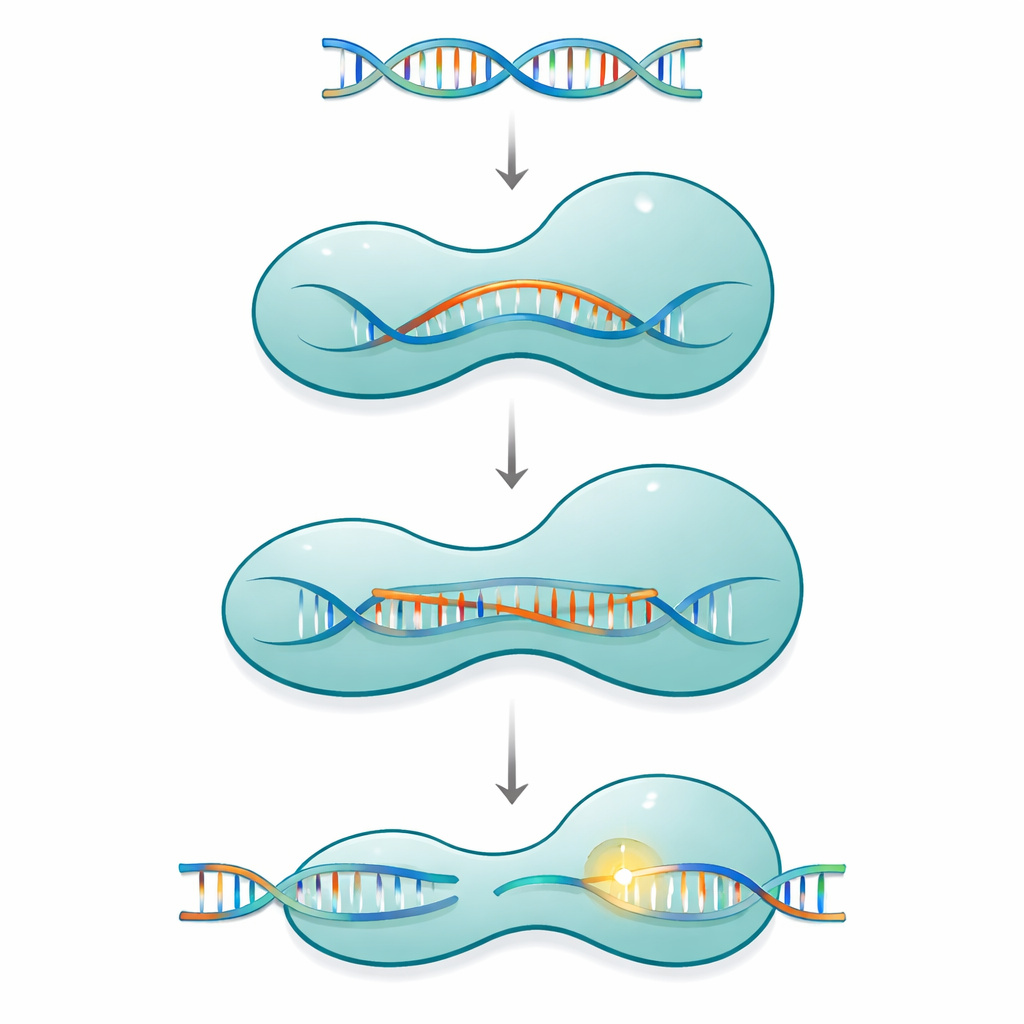
Cas12a pertenece a una familia de sistemas CRISPR de proteína única que usan una corta ARN guía para localizar y cortar ADN coincidente en virus o en el genoma de una célula. La proteína tiene la forma de una pinza de dos brazos: un lado de reconocimiento que comprueba la secuencia, y un lado de corte que aloja la maquinaria química. Estas dos mitades están conectadas por un segmento delgado y cargado positivamente llamado helicio puente. Cuando Cas12a se une a su ARN guía y luego a su ADN objetivo, la proteína no actúa como una herramienta rígida. En su lugar, atraviesa una serie de cambios conformacionales grandes y pequeños que se cierran gradualmente alrededor de una estructura híbrida ARN–ADN en crecimiento conocida como R-loop, activando completamente el sitio de corte solo cuando se ha formado un tramo suficientemente largo de apareamiento correcto de bases.
Explorando el interruptor de seguridad incorporado
Los investigadores se centraron en un Cas12a de la bacteria Francisella novicida y en una versión previamente diseñada en la que dos aminoácidos en el helicio puente fueron reemplazados por prolina, un cambio conocido por endurecer o interrumpir hélices. Esta variante, llamada FnoCas12aKD2P, corta el ADN de manera más selectiva pero más lenta que la proteína natural. Usando crio-microscopía electrónica, capturaron cinco instantáneas estructurales distintas de esta variante unida a su ARN guía y a un fragmento de ADN objetivo. Estas instantáneas muestran la proteína en diferentes etapas de su vía de activación, desde el reconocimiento inicial temprano del ADN hasta estados posteriores donde parte del híbrido ARN–ADN está formada pero aún no se ha alcanzado la plena preparación para el corte.
Cómo los cambios de forma impulsan un corte preciso
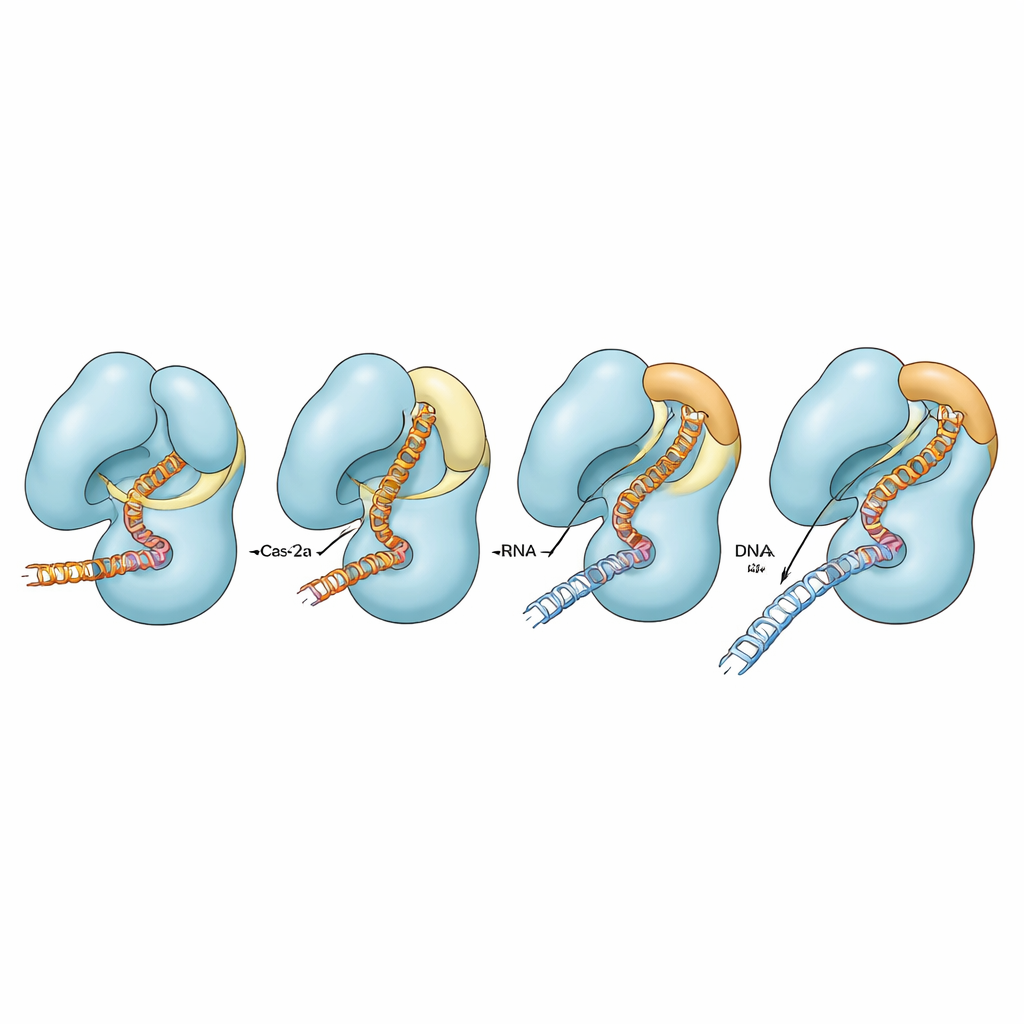
Comparar la variante con estructuras previamente determinadas de Cas12a normal reveló un patrón claro. En la proteína natural, un segmento del helicio puente se convierte de un lazo suelto en una hélice más larga y recta y se inclina hacia el híbrido ARN–ADN en crecimiento, entrando en contacto cercano con él. Al mismo tiempo, una hélice vecina en el dominio de corte se afloja, y una pequeña región llamada la “tapa”, que normalmente bloquea el sitio activo, pasa de un lazo a una hélice y se abre. Juntos, estos movimientos coordinados abren un bolsillo que permite que entre una sola cadena de ADN y sea cortada. En la variante que contiene prolina, el helicio puente no puede completar esta transición de lazo a hélice ni doblarse correctamente. Como resultado, el híbrido ARN–ADN permanece distorsionado y más alejado, la tapa permanece en un estado cerrado similar a un lazo, y el complejo rara vez alcanza una conformación totalmente precatalítica. Este cuello de botella mecánico ralentiza el corte en el objetivo y dificulta que el ADN con desajustes supere los puntos de control internos.
Ajustar la fidelidad afinando contactos
Para probar cómo contribuyen los distintos contactos alrededor de la tapa y del helicio puente a la actividad, los autores modificaron residuos cargados específicos que enlazan estas regiones. En el Cas12a normal, romper esos contactos tuvo efectos solo modestos sobre el corte de ADN perfectamente emparejado, aunque en algunas condiciones afectó la eficiencia con la que se clivaba la segunda hebra de ADN cuando había desajustes. En el contexto del helicio puente deteriorado, sin embargo, las mismas sustituciones redujeron drásticamente o casi eliminaron el corte de ambas hebras, especialmente cuando la guía y el ADN no concordaban perfectamente. Simulaciones por computadora apoyaron estos hallazgos, mostrando que solo cuando el helicio puente puede adoptar plenamente su forma helicoidal se mueven de manera fuertemente coordinada el puente, la hélice adyacente, la tapa y los ácidos nucleicos. Cuando la hélice está dañada, estos movimientos se desacoplan parcial o totalmente, y la enzima tiene dificultades para completar su ciclo catalítico.
Una guía de diseño para herramientas CRISPR de nueva generación
En conjunto, el trabajo revela al helicio puente como una palanca de control interna que vincula la longitud y la calidad del híbrido ARN–ADN con la apertura del bolsillo de corte en Cas12a. Al obligar a la proteína a completar una secuencia específica de cambios conformacionales antes de cleavar el ADN, este mecanismo refuerza de forma natural la discriminación frente a desajustes. Los hallazgos ayudan a explicar por qué cambios dirigidos en esta pequeña región pueden generar variantes de Cas12a con reducción del corte fuera de objetivo y actividad colateral disminuida, propiedades deseables para una edición genómica y diagnósticos más seguros. Más ampliamente, el estudio destaca cómo desplazamientos sutiles en hélices cortas pueden coordinar la comunicación a larga distancia en grandes máquinas moleculares, ofreciendo principios generales para diseñar enzimas de procesamiento de ácidos nucleicos de alta fidelidad.
Cita: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
Palabras clave: CRISPR-Cas12a, fidelidad de la edición génica, helicio puente, formación del R-loop, regulación alostérica