Clear Sky Science · es
RoboA refuerza el destino de las células madre en planarias a través de FoxA y Anosmin1a
Cómo los gusanos regeneran sus órganos
Algunos platelmintos pueden volver a crecer casi cualquier parte del cuerpo que falta, desde su tubo de alimentación hasta el cerebro. Esta notable capacidad depende de células madre adultas que pueden convertirse en muchos tipos celulares diferentes según la demanda. Pero con tanta libertad, ¿cómo evitan estas células formar tejido equivocado en el lugar equivocado—por ejemplo, producir células del estómago en la cabeza en lugar de neuronas? Este estudio utiliza la planaria para desentrañar cómo un pequeño conjunto de señales mantiene a las células madre altamente flexibles en la vía correcta durante la regeneración.
El gusano regenerante y su potencial oculto
La planaria Schmidtea mediterranea es un modelo favorito para estudiar la regeneración porque una gran población de células madre está distribuida por todo su cuerpo. Un órgano clave es la faringe, un tubo muscular de alimentación que se sitúa en el centro del gusano y se conecta con el exterior cuando el animal se alimenta. Trabajos anteriores mostraron que un gen llamado foxA es crucial para reconstruir esta faringe tras una lesión, y que solo ciertas células madre cercanas a la faringe suelen activar foxA. El nuevo estudio plantea una pregunta aparentemente simple: ¿qué impide que las células madre en otras regiones—especialmente la cabeza y el cerebro—también adopten una identidad faríngea?
Cuando falta la orientación
Los investigadores se centraron en una proteína receptora llamada RoboA, presente a niveles bajos en muchos tipos celulares, incluidas las células madre. Cuando redujeron la actividad de RoboA mediante interferencia por ARN, los animales con frecuencia desarrollaron faringes extras y mal ubicadas tras ser seccionados. Una inspección más detallada reveló algo más sutil: incluso en gusanos no lesionados, bajar RoboA provocó la aparición de neuronas y músculos con aspecto faríngeo dentro de la región cerebral. Estas “neuronas faríngeas ectópicas” se comportaban como células faríngeas normales en cuanto a expresión génica, pero ahora estaban en el lugar equivocado. Es importante señalar que el plano corporal general y la arquitectura cerebral se mantuvieron mayormente intactos, lo que sugiere que RoboA no remodelaba todo el animal, sino que afinaba en qué se convertían las células madre cercanas.
Un interruptor de tres actores para el destino celular
Para entender cómo funciona RoboA, el equipo buscó socios fuera de la célula. Aunque las proteínas Robo son mejor conocidas por unirse a un ligando llamado Slit, silenciar Slit no reprodujo la aparición de células faríngeas mal ubicadas. Un amplio cribado por RNAi de proteínas secretadas y de membrana señaló en cambio a Anosmin1a (Anos1a), una proteína secretada relacionada con un factor humano implicado en el síndrome de Kallmann. Reducir Anos1a causó neuronas faríngeas adicionales similares, y las inactivaciones combinadas de RoboA y Anos1a se comportaron como si actuaran en la misma vía. Al mismo tiempo, el perfil molecular mostró que el factor de transcripción FoxA está en el centro de la decisión: cuando RoboA está presente, mantiene a FoxA apagado en las células madre de la cabeza; cuando se elimina la señalización de RoboA, FoxA se enciende y esas mismas células madre pueden elegir un destino de neurona faríngea incluso estando en el cerebro.
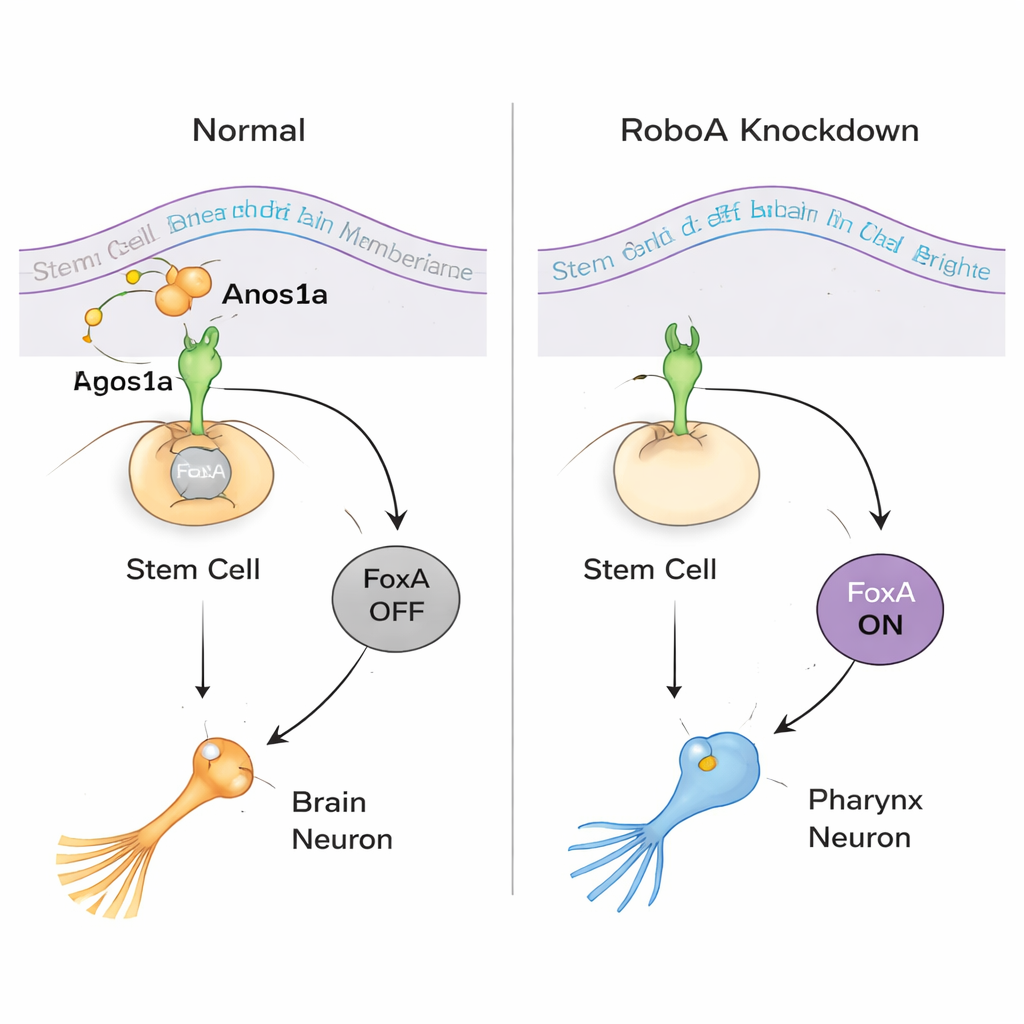
Revelando una elección bidireccional en las células madre
El equipo se preguntó entonces si esta flexibilidad funciona en ambas direcciones. En animales normales, las células madre alrededor de la faringe dependen de FoxA para convertirse en neuronas faríngeas y células epiteliales, mientras que los músculos faríngeos siguen una vía diferente. Cuando FoxA fue silenciado durante periodos prolongados, los gusanos perdieron sus faringes por completo y desarrollaron crecimientos anormales en el centro del cuerpo. La secuenciación de ARN de células individuales y el análisis con marcadores revelaron que estos crecimientos contenían muchos tipos celulares normalmente restringidos a la cabeza, incluidas células oculares y neuronas específicas del cerebro. En otras palabras, cuando falta FoxA en el lugar donde debería formarse la faringe, las células madre locales derivan por defecto hacia un destino similar al cerebral. Este hallazgo muestra que las mismas células madre pueden ser empujadas hacia identidades de “faringe” o de “cerebro” según las señales que reciban.
Afinando la regeneración, no redibujando el mapa
Poniendo todas las evidencias juntos, los autores proponen que la regeneración en planarias se guía en dos capas. Señales amplias de “control posicional”, como Wnt y otras moléculas de patrón, establecen el mapa aproximado de cabeza, tronco y cola. Sobre eso, genes locales “reforzadores de destino” como RoboA y Anos1a actúan como controles de seguridad, bloqueando opciones inapropiadas. En la cabeza, la señalización RoboA–Anos1a mantiene a FoxA apagado para que las células madre produzcan neuronas cerebrales en lugar de células faríngeas; cerca de la faringe, se permite que FoxA se active y promueva destinos específicos de la faringe. Este control por capas permite que las células madre de la planaria permanezcan extraordinariamente plásticas a la vez que reconstruyen órganos en el lugar correcto, ofreciendo un plano de cómo una regeneración robusta puede coexistir con un orden anatómico estricto.
Cita: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
Palabras clave: regeneración de planarias, plasticidad de las células madre, patronización de órganos, señalización RoboA, factor de transcripción FoxA