Clear Sky Science · es
NeoPrecis: mejorando la predicción de respuesta a la inmunoterapia mediante la integración de paisajes de neoantígenos cualificados y conscientes de la clonalidad
Por qué algunos cánceres responden a la inmunoterapia y otros no
La inmunoterapia ha transformado el tratamiento del cáncer, pero muchos pacientes siguen sin beneficiarse y algunos sufren efectos secundarios graves. Una gran pregunta es por qué algunos tumores son detectados y destruidos por el sistema inmune mientras que otros pasan desapercibidos. Este estudio presenta NeoPrecis, un método computacional que examina con más detalle las “señales” que los tumores muestran al sistema inmune —llamadas neoantígenos— y usa esa información para predecir mejor qué pacientes tienen más probabilidades de responder a las inmunoterapias modernas.
Nuevas señales en las células cancerosas
Las células cancerosas acumulan mutaciones en el ADN que pueden alterar las proteínas que producen. Pequeños fragmentos de estas proteínas alteradas, conocidos como neoantígenos, pueden mostrarse en la superficie celular y ser reconocidos como extraños por los linfocitos T, los asesinos del sistema inmune. Durante años, médicos e investigadores han recurrido a medidas toscas como la carga mutacional tumoral —el número total de mutaciones— para estimar la probabilidad de que un cáncer responda a inhibidores del punto de control inmune. Pero esto es una herramienta poco precisa: no toda mutación crea un objetivo visible o atractivo para los linfocitos T, y los tumores pueden ser un mosaico de muchos subtipos celulares distintos. NeoPrecis fue diseñado para ir más allá de simplemente contar mutaciones y, en su lugar, evaluar cuántas de ellas son realmente objetivos prometedores en todo el tumor.
Analizando tres ingredientes clave a la vez
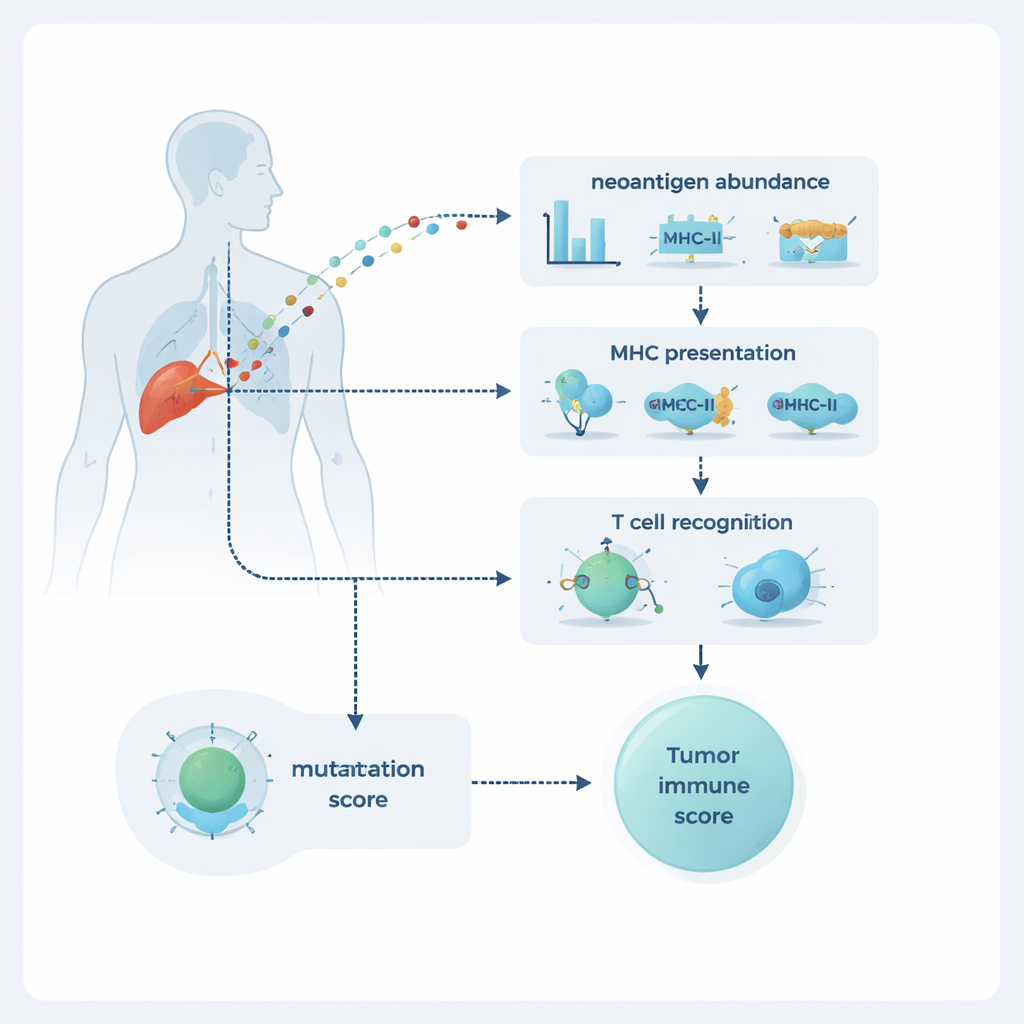
NeoPrecis evalúa cada mutación en tres dimensiones: cuánto abunda en el tumor, si es probable que se presente en la superficie celular y qué probabilidad hay de que la detecten los linfocitos T. La abundancia se estima a partir de secuenciación de ADN y ARN, que revelan con qué frecuencia aparece la mutación y cuán fuertemente se expresa. La presentación se modela mediante la unión a moléculas llamadas MHC de clase I y clase II, que actúan como paneles publicitarios que muestran fragmentos proteicos a los linfocitos T. La parte más novedosa es el componente de reconocimiento por linfocitos T, NeoPrecis-Immuno. Este modelo aprende a partir de grandes bases de datos de interacciones conocidas entre linfocitos T y péptidos para calibrar cuánto difiere un fragmento mutado de su contraparte normal en una forma relevante para el reconocimiento por T, a la vez que tiene en cuenta las variantes específicas de MHC que porta cada persona.
Enseñar a una computadora lo que “ven” los linfocitos T
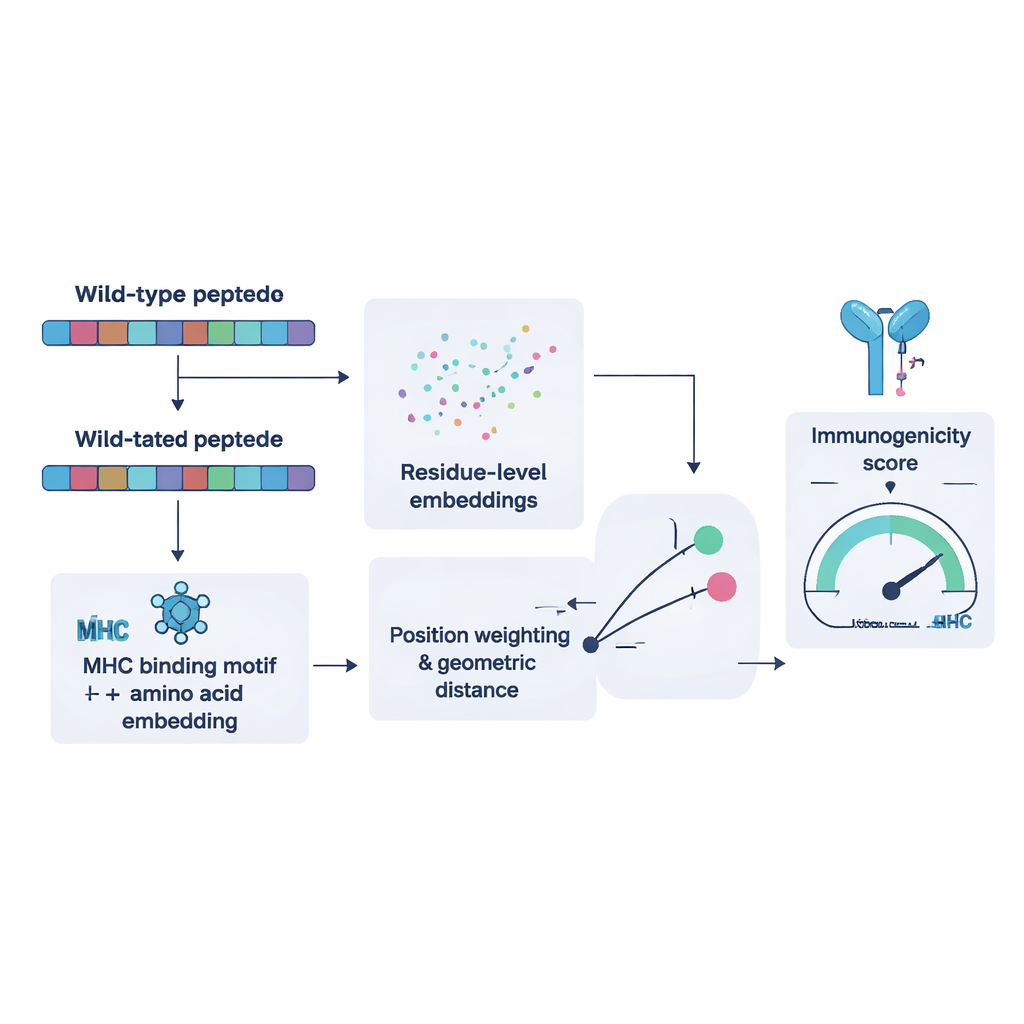
Para entrenar NeoPrecis-Immuno, los investigadores reunieron primero miles de ejemplos en los que el mismo linfocito T reconoce múltiples péptidos similares y otros que no reconoce. Usaron estos ejemplos para enseñarle al modelo que los fragmentos mutados que se parecen mucho a los normales tienen menos probabilidades de desencadenar un ataque inmune, porque los objetivos que se parecen al propio organismo suelen eliminarse durante el desarrollo de los linfocitos T. El modelo representa cada péptido como un punto en un espacio matemático conformado por su secuencia de aminoácidos y las preferencias de unión de las moléculas MHC de la persona. Luego mide qué tan lejos queda el péptido mutado respecto al original. Distancias mayores, informadas por motivos específicos, se corresponden con una mayor probabilidad de ser inmunogénico. Al compararlo con herramientas existentes en conjuntos de datos de cáncer independientes, NeoPrecis-Immuno igualó o superó su rendimiento, especialmente al trabajar con MHC de clase II, que presenta péptidos a los linfocitos T colaboradores que apoyan y sostienen las respuestas antitumorales.
De mutaciones individuales al tumor completo
Las mutaciones individuales son solo una parte de la historia; también importa cómo se distribuyen dentro del tumor. Algunas mutaciones son “clonales”, presentes en casi todas las células cancerosas, mientras que otras son “subclonales”, solo presentes en ciertos focos. NeoPrecis construye un “paisaje de neoantígenos” sumando sus puntuaciones de inmunogenicidad a través de las mutaciones e incorporando información sobre a qué subclones pertenecen y qué tan frecuentes son esos subclones. Esto produce puntuaciones a nivel tumoral que resaltan los cánceres ricos en neoantígenos fuertes y ampliamente compartidos —especialmente aquellos que pueden presentarse tanto en MHC de clase I como de clase II y que potencialmente desencadenan respuestas coordinadas de linfocitos T colaboradores y citotóxicos. En cohortes de pacientes con melanoma y cáncer de pulmón no microcítico tratados con inhibidores del punto de control, estas puntuaciones basadas en NeoPrecis separaron con mayor precisión a respondedores y no respondedores que los recuentos estándar de mutaciones, y fueron particularmente útiles en tumores pulmonares complejos y heterogéneos.
Qué significa esto para los pacientes
Para los pacientes, la promesa de NeoPrecis es emparejar con mayor precisión las inmunoterapias con quienes tengan más probabilidades de beneficiarse y comprender mejor por qué algunos tumores resisten el tratamiento. Al centrarse en la calidad y la distribución de los neoantígenos —no solo en su cantidad—, el marco ayuda a explicar por qué tumores con cargas mutacionales similares pueden comportarse muy diferente. En el futuro, mapas tan detallados del paisaje visible por el sistema inmune de un tumor podrían guiar no solo el uso de inhibidores del punto de control, sino también el diseño de vacunas personales contra el cáncer que prioricen los objetivos más potentes y ampliamente compartidos en el tumor de cada persona.
Cita: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
Palabras clave: inmunoterapia del cáncer, neoantígenos, heterogeneidad tumoral, inhibidores de puntos de control, oncología computacional