Clear Sky Science · es
Stenotrophomonas promueve la progresión de tumores gastrointestinales mediante la degradación de STING en células tumorales y la atenuación de la respuesta inmune
Gérmenes ocultos dentro de los tumores
La mayoría sabe que los microbios en nuestro intestino pueden afectar la digestión e incluso el estado de ánimo, pero pocos se imaginan que bacterias vivas pueden establecerse dentro de las propias células cancerosas. Este estudio revela cómo una bacteria ambiental común, Stenotrophomonas, se oculta en tumores gastrointestinales y los ayuda a crecer de forma silenciosa, al tiempo que embota las defensas inmunitarias del organismo y reduce la eficacia de las inmunoterapias modernas.
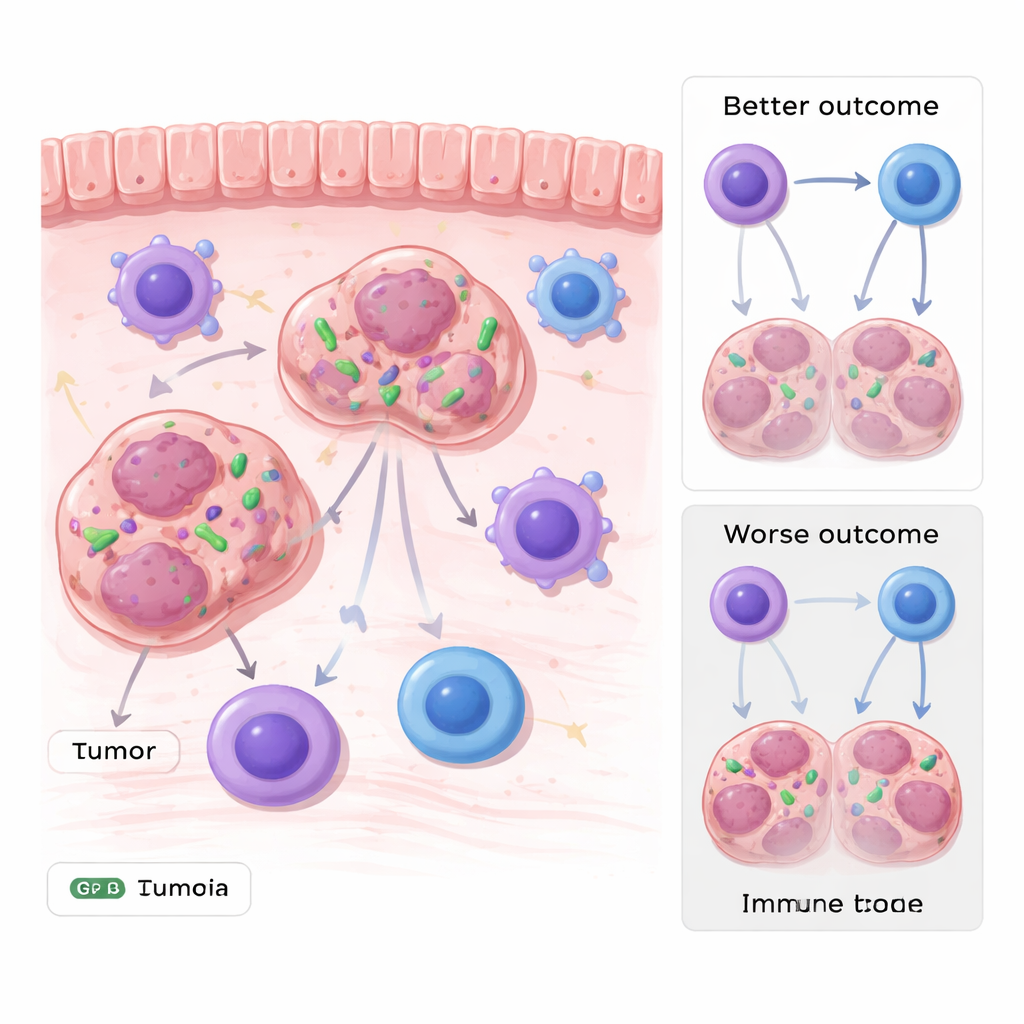
Bacterias que viven en células cancerosas
Los tumores gastrointestinales, como los cánceres de estómago y colorrectal, se desarrollan en contacto permanente con las ricas comunidades bacterianas del tracto digestivo. Al analizar múltiples conjuntos de datos genéticos de pacientes y validar después sus hallazgos en muestras tumorales, los investigadores encontraron que el ADN de Stenotrophomonas estaba inusualmente abundante en varios tipos de tumores gastrointestinales. De forma importante, su presencia no fue solo contaminación de la superficie: métodos de imagen, incluidos sondas fluorescentes y microscopía electrónica, revelaron bacterias enteras en el citoplasma de células tumorales. Los pacientes cuyos tumores contenían niveles más altos de esta bacteria tendieron a tener peor evolución con el tiempo, vinculando al microbio con un peor pronóstico.
Cómo un microbio desequilibra la respuesta inmune
El equipo se preguntó si estas bacterias ocultas simplemente coexistían con tumores agresivos o si activamente impulsaban la enfermedad. En modelos de ratón, infectaron células tumorales con Stenotrophomonas marcadas con fluorescencia antes de implantarlas en los animales. Los tumores que portaban la bacteria crecieron más rápido y fueron mayores que los que no la tenían, en varios tipos celulares cancerosos. Al examinar el paisaje inmunitario circundante, observaron que el número total de células inmunes, incluidas células T y macrófagos, era similar. La diferencia crítica residía en un subconjunto especializado de macrófagos que expresan una molécula llamada MHC-II, que les ayuda a presentar fragmentos tumorales a las células T citotóxicas. En los tumores que alojaban Stenotrophomonas, estos macrófagos MHC-II positivos estaban marcadamente reducidos y las células T mostraban una actividad citotóxica más débil.
Interrumpiendo un sistema de alarma celular
Para entender el mecanismo, los investigadores se centraron en una vía de alarma clave dentro de las células conocida como STING, que normalmente detecta ADN extraño y desencadena la liberación de señales antivirales “de peligro” llamadas interferones de tipo I. En experimentos de laboratorio, las células tumorales infectadas con Stenotrophomonas produjeron mucho menos interferón beta, y los genes que normalmente se activan por esta vía estaban apagados. El estudio mostró que la bacteria induce estrés en la fábrica de plegado de proteínas de la célula, el retículo endoplásmico, y después secuestra una ruta de control de calidad llamada degradación asociada al RE (ER-associated degradation). A través de una proteína auxiliar llamada SEL1L, esta vía etiqueta la proteína STING para su destrucción en el proteasoma, el “triturador” de la célula. Con los niveles de STING disminuidos, la célula tumoral emite una alarma más débil, lo que conduce a menos interferón y, en consecuencia, a una activación atenuada de los macrófagos MHC-II positivos.
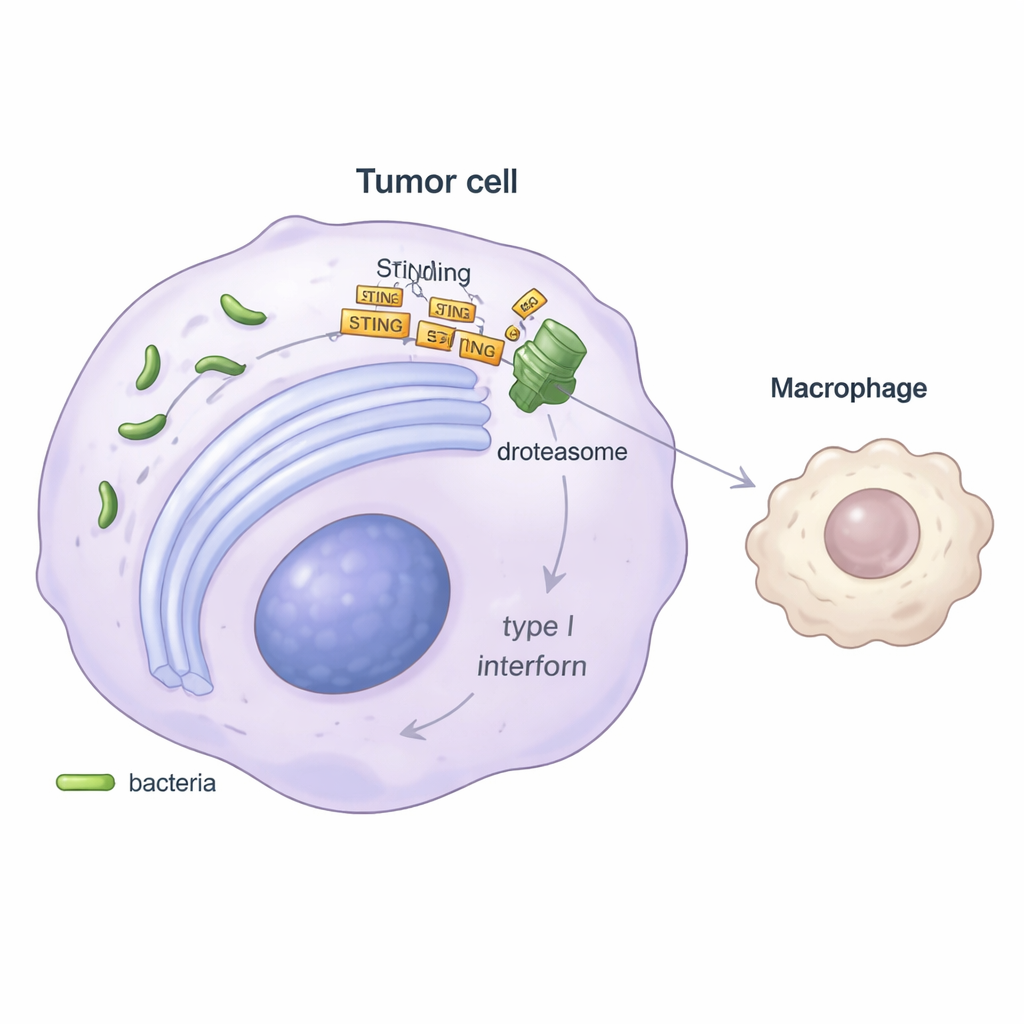
Socavando la inmunoterapia — y una posible solución
Dado que las inmunoterapias modernas como los anticuerpos anti–PD-1 dependen de respuestas vigorosas de células T, el equipo probó cómo Stenotrophomonas intracelular afectaba el tratamiento. En ratones, los tumores que portaban la bacteria respondieron mal al anti–PD-1 en comparación con tumores libres de bacterias, incluso cuando se combinó con quimioterapia. Las células T en estos tumores mostraron marcadores reducidos de actividad y proliferación, consistente con una pobre estimulación inmune. De forma llamativa, cuando los investigadores trataron a los animales con el antibiótico levofloxacino, que mata eficazmente a Stenotrophomonas, el crecimiento tumoral se ralentizó y la respuesta al anti–PD-1 mejoró. Restaurar la señalización del interferón con un fármaco clínico de interferón también pudo rescatar la población de macrófagos MHC-II positivos y reavivar la citotoxicidad de las células T en algunos contextos, subrayando el papel central de esta vía.
Qué significa esto para los pacientes
Para el lector no especializado, el mensaje clave es que algunos cánceres gastrointestinales pueden contar con su propio microbioma interno que les ayuda a evadir el ataque inmune. Stenotrophomonas, al degradar el sistema de alarma STING dentro de las células tumorales, atenúa las señales inmunitarias que normalmente movilizarían macrófagos y células T citotóxicas. Esto no solo acelera el crecimiento tumoral, sino que también puede ayudar a explicar por qué ciertos pacientes no se benefician de potentes inmunoterapias. Aunque se necesita más trabajo antes de que esto cambie la práctica clínica, los hallazgos plantean la posibilidad de que analizar los tumores en busca de dichas bacterias —y tratarlas selectivamente con antibióticos dirigidos o fármacos que estabilicen STING— podría algún día mejorar los resultados en personas con cáncer de estómago y colorrectal.
Cita: Feng, H., Chen, K., Xi, Z. et al. Stenotrophomonas promotes gastrointestinal tumor progression via STING degradation in tumour cells and mitigated immune response. Nat Commun 17, 2042 (2026). https://doi.org/10.1038/s41467-026-68649-0
Palabras clave: microbioma tumoral, cáncer gastrointestinal, Stenotrophomonas, vía STING, inmunoterapia contra el cáncer