Clear Sky Science · es
NR6A1 es esencial para la especificación, formación y supervivencia de las células de la cresta neural
Cómo las decisiones celulares tempranas moldean la cara y el cuerpo
Antes de nacer, un grupo especial de células llamadas células de la cresta neural viaja por el embrión para ayudar a construir la cara, el corazón, los nervios y otros tejidos. Cuando estas células fallan, los bebés pueden nacer con defectos congénitos graves. Este estudio descubre un interruptor molecular anteriormente poco reconocido, una proteína llamada NR6A1, que contribuye a decidir cuándo y dónde se forman las células de la cresta neural en embriones de mamífero y qué ocurre cuando ese interruptor falla.
Los constructores nómadas del embrión
Las células de la cresta neural aparecen muy temprano en el desarrollo a lo largo del borde del tejido en formación del cerebro y la médula espinal. Tras separarse de ese tejido, migran largas distancias para crear muchas estructuras diferentes, desde huesos y cartílagos faciales hasta partes del sistema nervioso periférico y células pigmentarias de la piel. Debido a que contribuyen a tantos órganos, incluso pequeñas alteraciones en su formación pueden provocar afecciones de amplio alcance conocidas como neurocristopatías, incluidas síndromes craneofaciales como el de Treacher Collins. Comprender cómo aparecen estas células es, por tanto, esencial para explicar tanto el desarrollo normal como los defectos congénitos.
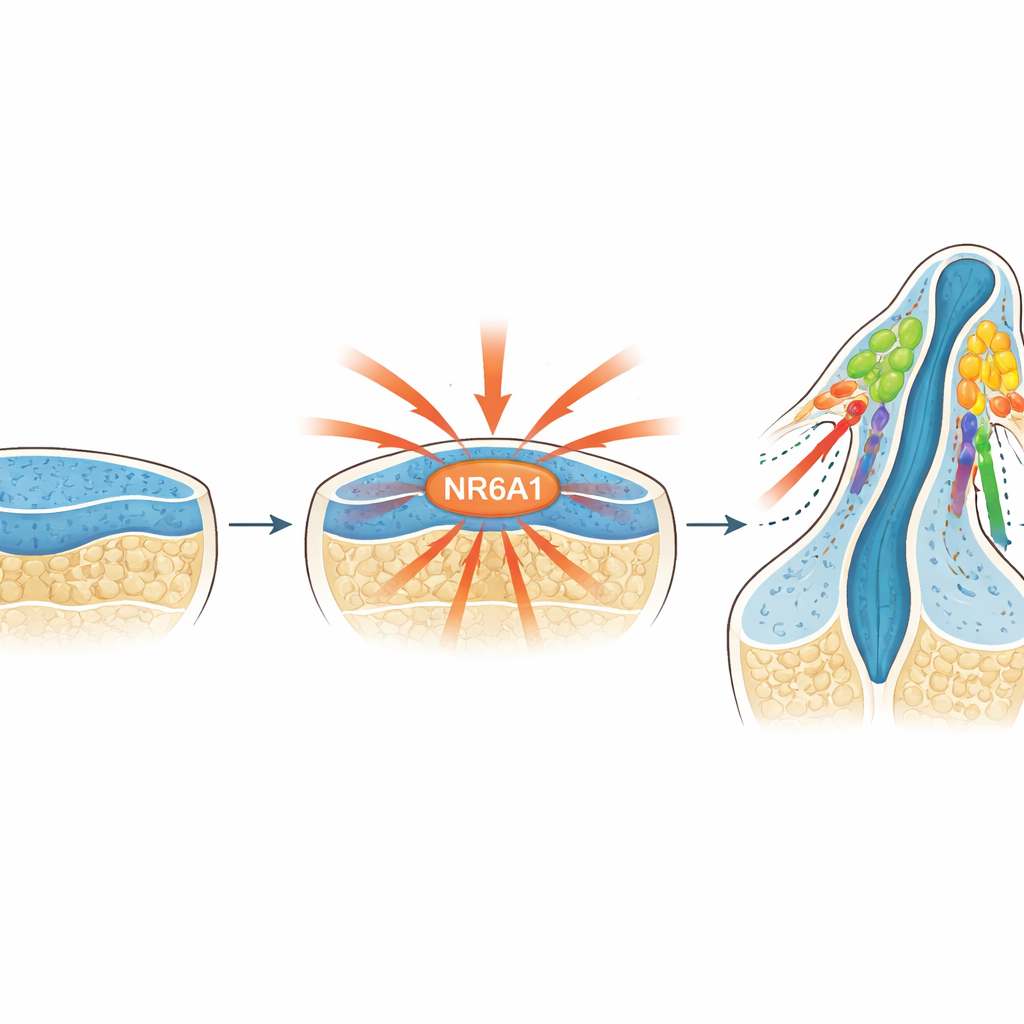
Un interruptor maestro reconocido ahora
Los investigadores se centraron en NR6A1, un miembro de la familia de receptores nucleares de proteínas que controlan la actividad génica. Trabajos previos sugerían que NR6A1 podría estar implicado en defectos craneofaciales, pero su papel en las células de la cresta neural era desconocido. Al seguir NR6A1 en embriones de ratón desde poco después de la implantación en adelante, el equipo halló que su presencia coincidía estrechamente con el lugar y el momento en que normalmente nacen las células de la cresta neural: aparece en el tejido neural temprano, se concentra a lo largo del lado dorsal del cerebro y la médula espinal en desarrollo, y también se observa en las células justo cuando se separan de ese tejido para comenzar a migrar.
Qué ocurre cuando falta el interruptor
Los ratones completamente carentes de NR6A1 mueren temprano en el desarrollo, por lo que el equipo examinó embriones justo antes de ese punto. Observaron una escasez grave de células de la cresta neural, particularmente detrás del primer arco que formará partes de la mandíbula y el cuello, donde las células de la cresta en migración estaban casi totalmente ausentes. Los programas génicos clave que normalmente marcan la identidad de la cresta neural y permiten que las células se desprendan y se muevan estaban fuertemente reducidos. Al mismo tiempo, los genes que mantienen a las células en un estado parecido a la célula madre y altamente proliferativo permanecían activos, y muchas células con rasgos de cresta neural que sí se formaron murieron pronto. Estos hallazgos indican que, sin NR6A1, las células neurales madre no logran la transición adecuada hacia células de la cresta neural migratorias y no pueden sobrevivir.
Apagar la pluripotencia y encender el movimiento
Para entender cómo ejerce NR6A1 este control, los autores combinaron varias técnicas moleculares potentes, incluyendo secuenciación de ARN de célula única, mapeo de accesibilidad de la cromatina y ensayos dirigidos de unión ADN–proteína en células de cresta neural derivadas de células madre de ratón y humana. Encontraron que NR6A1 se une físicamente a motivos de ADN específicos cercanos a genes que gobiernan dos programas opuestos: uno que mantiene la pluripotencia (la capacidad de convertirse en muchos tipos celulares) y otro que impulsa la identidad de la cresta neural y el movimiento celular. Cuando NR6A1 está presente, la cromatina que rodea genes de pluripotencia como Oct4 y Nanog se vuelve menos accesible y esos genes se silencian, mientras que regiones cercanas a genes de cresta neural y de transición epitelio-mesénquima se abren y activan. La sobreexpresión de Oct4 durante la ventana crítica de formación de la cresta neural imitó la pérdida de NR6A1, mostrando además que la pluripotencia debe silenciarse para que emerjan las células de la cresta neural.
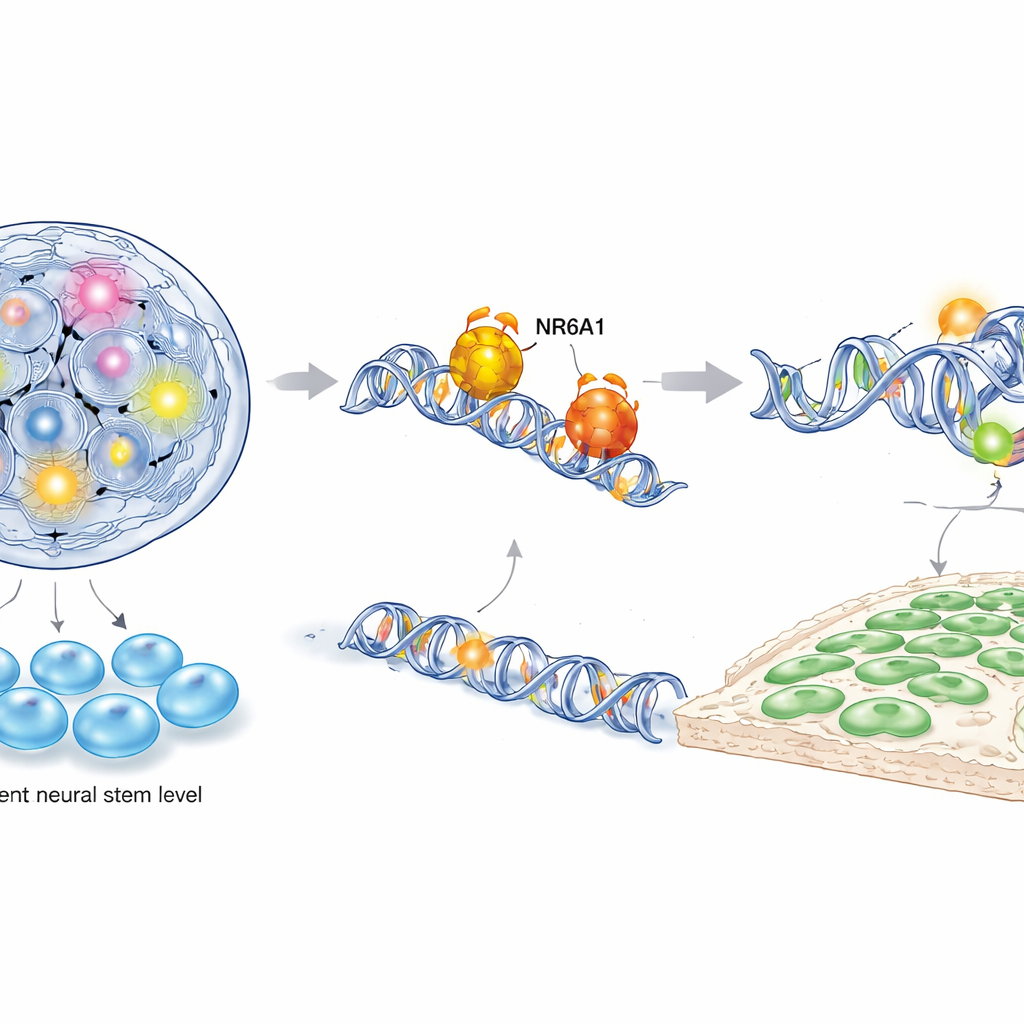
Reescribiendo el calendario del desarrollo temprano
El estudio también revisa el calendario de cuándo comienzan a especificarse las células de la cresta neural en los mamíferos. Usando un sistema genético inductible para eliminar NR6A1 en distintos momentos, el equipo mostró que eliminarlo hacia la mitad de la gastrulación—una etapa anterior a la que se pensaba tradicionalmente—era suficiente para bloquear la activación de los genes de la cresta neural. En contraste, eliminar NR6A1 más tarde, incluso con una línea conductora específica de la cresta neural ampliamente utilizada, no produjo defectos evidentes. Esto significa que las decisiones cruciales sobre el destino de la cresta neural se toman antes de que esas herramientas estándar incluso comiencen a funcionar, lo que explica por qué algunos estudios previos en ratón pudieron haber pasado por alto requisitos tempranos.
Por qué importa para los defectos congénitos y la enfermedad
En conjunto, el trabajo revela a NR6A1 como un coordinador central que ayuda a que las células neurales madre "maduren" en células de la cresta neural al apagar simultáneamente los programas de pluripotencia y permitir los programas de migración y supervivencia. Esta doble acción parece comenzar durante la mitad de la gastrulación, más temprano de lo reconocido previamente en mamíferos, y acerca el desarrollo del ratón al de otros vertebrados. Al aclarar cuándo y cómo opera este interruptor, el estudio ofrece un marco para reinterpretar experimentos genéticos anteriores, identificar mejores herramientas para estudiar la biología de la cresta neural y, en última instancia, comprender y potencialmente prevenir las neurocristopatías que surgen cuando esta decisión temprana del desarrollo falla.
Cita: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
Palabras clave: células de la cresta neural, NR6A1, desarrollo embrionario, cambio de pluripotencia, neurocristopatía