Clear Sky Science · es
Ingeniería del sistema MmeFz2-ωRNA para una edición genómica eficiente mediante un marco integrado computacional-experimental
Tijeras genéticas más pequeñas para grandes problemas médicos
La edición genética ya ha cambiado la forma en que los científicos estudian las enfermedades, pero convertirla en una medicina segura y práctica sigue siendo un reto importante. Un gran obstáculo es que las “tijeras” de ADN más potentes hoy en día, como CRISPR-Cas9, son físicamente grandes y difíciles de empaquetar en los diminutos vehículos de entrega usados en pacientes. Este estudio presenta una nueva herramienta de edición genética compacta, construida a partir de una familia de enzimas poco conocida llamada Fanzor2, y muestra cómo la inteligencia artificial puede rediseñarla rápidamente hasta convertirla en una candidata sólida para futuras terapias genéticas.
Una nueva clase de editores genéticos compactos
La mayoría de los editores genómicos actuales, como Cas9 y Cas12a, son proteínas voluminosas formadas por más de mil bloques constructivos. Ese tamaño dificulta su inclusión en los virus adenoasociados (AAV), el sistema de entrega líder para terapias génicas. En contraste, las proteínas Fanzor2 son mucho más pequeñas y se encuentran de forma natural en eucariotas, la rama de la vida que incluye animales y humanos. Los autores se centraron en un miembro de esta familia, MmeFz2, que utiliza una molécula corta de ARN llamada ωRNA para localizar y cortar secuencias de ADN específicas. En teoría, MmeFz2 parecía ideal para terapia: compacto y programable. En la práctica, sin embargo, su actividad en células humanas era pésima, editando menos del uno por ciento de los sitios objetivo. El equipo se propuso transformar esta enzima insuficiente en una herramienta práctica.
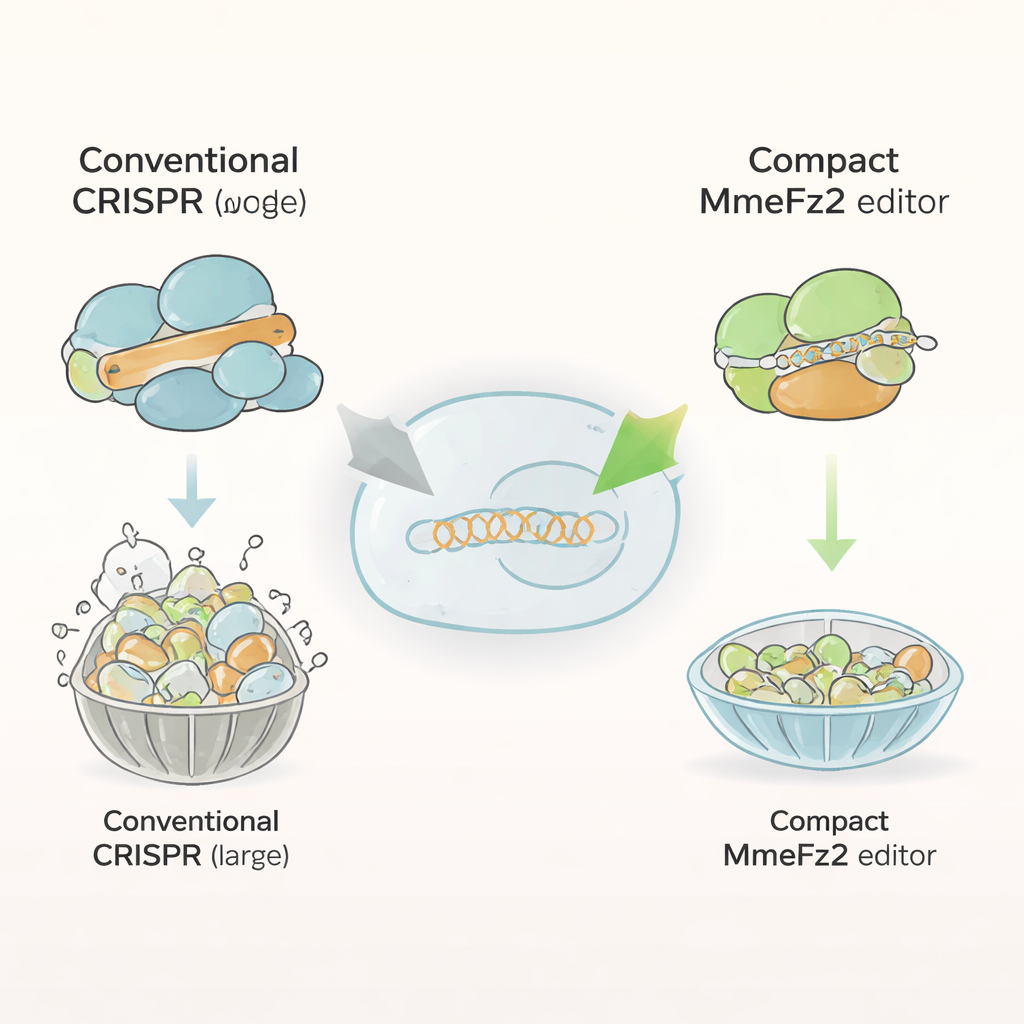
Usar IA para rediseñar la molécula guía
El primer objetivo fue el ωRNA, la guía que indica a MmeFz2 dónde cortar. Usando AlphaFold3, un programa de vanguardia que predice estructuras tridimensionales de complejos proteína–ARN–ADN, los investigadores construyeron un modelo de MmeFz2 unido a su ωRNA y a un objetivo de ADN. Esta estructura virtual reveló que partes del ωRNA eran flexibles, estaban mal apareadas y apenas tocaban la proteína. Guiados por esta información, el equipo reemplazó sistemáticamente enlaces inestables en el ARN y eliminó cadenas de uridinas que pueden interferir con la transcripción. Luego probaron docenas de variantes en células humanas. Al combinar las mejoras más eficaces y recortar una región de tallo innecesaria, crearon un ωRNA acortado un 30% pero que ofrecía cerca de 20 veces más eficiencia de edición en muchos sitios de ADN.
Ajustar finamente la proteína con aprendizaje automático
A continuación, el equipo afinó la propia proteína. Nuevamente emplearon AlphaFold3 para mapear dónde MmeFz2 contactaba el ARN y el ADN, y diseñaron más de cien cambios de un solo aminoácido destinados a fortalecer esos contactos o mejorar la flexibilidad. Tras evaluar estas variantes en células, incorporaron los datos de rendimiento en EVOLVEpro, un sistema de aprendizaje automático basado en modelos de lenguaje de proteínas entrenados con millones de secuencias naturales. Esta herramienta aprendió qué características tendían a aumentar la actividad y sugirió nuevas combinaciones de mutaciones con predicción de mejor rendimiento. Mediante unas pocas rondas de este ciclo computacional–experimental, los científicos obtuvieron dos variantes enzimáticas optimizadas que, combinadas con el ωRNA mejorado, elevaron la actividad de edición más de 60 veces respecto al sistema inicial.
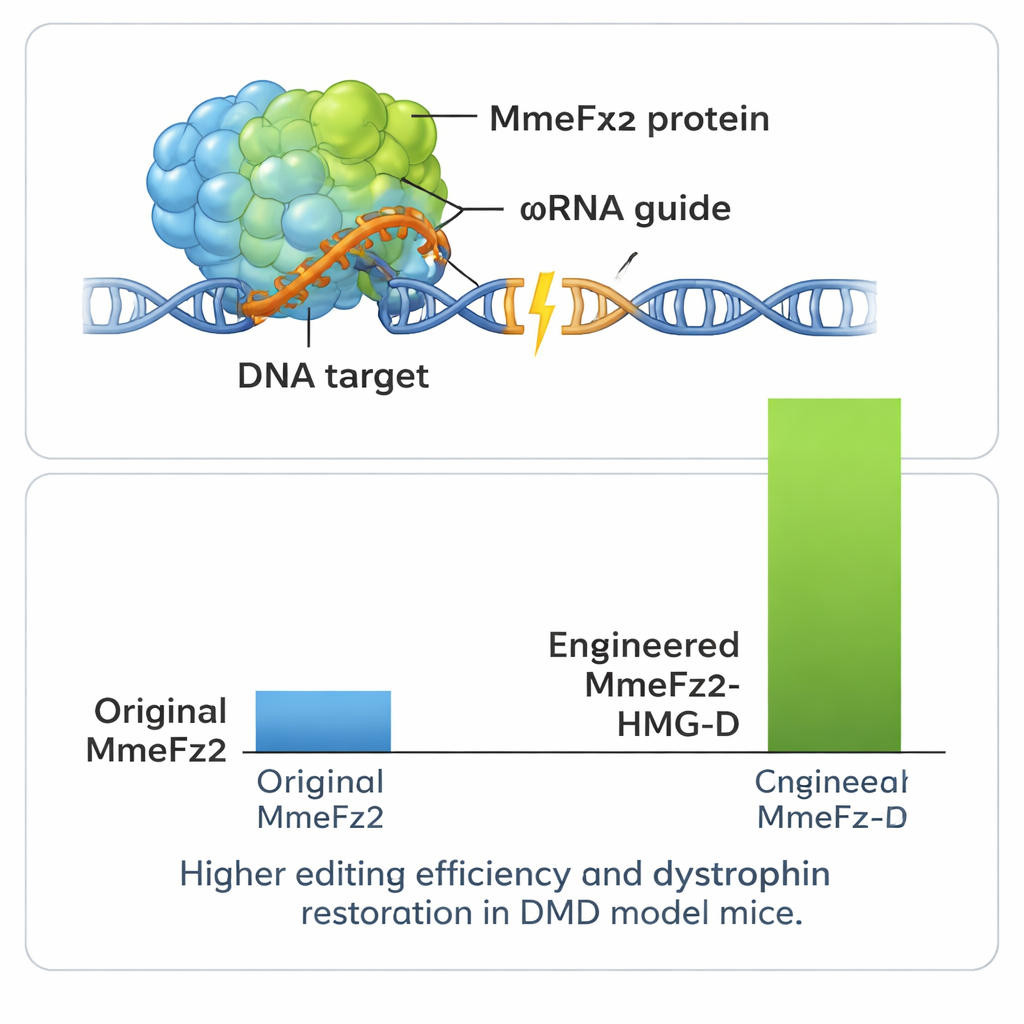
Aumentar la potencia y probar en un modelo de enfermedad
Para exprimir aún más el rendimiento del sistema, los autores fusionaron MmeFz2 con pequeños dominios de unión al ADN que ayudan a las proteínas a agarrarse al material genético. Uno de ellos, llamado HMG-D, resultó especialmente eficaz cuando se añadió al extremo de la enzima diseñada, produciendo niveles de edición superiores al 80% en algunos sitios. Es importante destacar que las pruebas en ubicaciones genómicas predichas como fuera de objetivo mostraron que este aumento de potencia no supuso una pérdida importante de precisión. Debido a que el editor genético completo —incluyendo proteína y ARN guía— es tan compacto, cabe cómodamente en un único vector AAV, algo que no es posible para la mayoría de los sistemas CRISPR. El equipo aprovechó esta ventaja en un modelo murino de la distrofia muscular de Duchenne, una enfermedad letal de desgaste muscular causada por errores en el gen de la distrofina. Una inyección única del editor entregado por AAV en el músculo de la pierna condujo a correcciones detectables en el ARN del gen y restauró la proteína distrofina en una fracción sustancial de las fibras musculares.
Qué significa esto para futuras terapias génicas
Para el público general, el mensaje clave es que los autores han convertido una enzima cortadora de genes débil y oscura en un editor compacto y de alto rendimiento que puede entregarse en un único paquete viral y reparar una enfermedad genética grave en un modelo animal realista. Igual de importante es cómo lo lograron: al combinar estrechamente predicción estructural basada en IA y aprendizaje automático con pruebas de laboratorio focalizadas, mejoraron tanto la proteína como su ARN guía con mucha más eficiencia que los enfoques tradicionales de prueba y error. Esta estrategia integrada podría acelerar la creación de muchas generaciones futuras de editores genómicos, acercando terapias génicas más precisas y seguras a pacientes con distrofia muscular y otras enfermedades hereditarias.
Cita: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Palabras clave: edición genética, alternativas a CRISPR, distrofia muscular de Duchenne, terapia génica viral, inteligencia artificial en biología