Clear Sky Science · es
La eliminación dependiente de C1q de la alfa-sinucleína permite a los macrófagos limitar de forma transitoria la sinucleinopatía entérica en ratones machos
Por qué el intestino importa en las enfermedades cerebrales
La enfermedad de Parkinson es más conocida por los temblores y los problemas de movimiento, pero muchas personas sufren años de estreñimiento intenso y otros trastornos intestinales antes de que aparezcan los síntomas motores. Este estudio explora lo que ocurre en el “segundo cerebro” del cuerpo —la red neuronal del intestino— cuando una proteína vinculada al Parkinson se pliega mal allí, y cómo las células inmunitarias locales primero ayudan y luego flaquean. Entender esta batalla temprana en el intestino podría abrir nuevas vías para aliviar los síntomas y, posiblemente, ralentizar la progresión de la enfermedad mucho antes de que el cerebro esté gravemente dañado.
Una proteína problemática en el segundo cerebro del cuerpo
En la enfermedad de Parkinson y trastornos relacionados, una proteína llamada alfa-sinucleína puede plegarse de forma anómala y agregarse en cúmulos tóxicos. Estos agregados se encuentran no solo en el cerebro, sino también en todo el sistema nervioso entérico, la red de neuronas que controla el movimiento intestinal. Muchos investigadores sospechan que, al menos en algunos pacientes, la alfa-sinucleína mal plegada podría establecerse primero en el intestino y luego propagarse hacia el cerebro a lo largo de las vías nerviosas. Los autores utilizaron un modelo de ratón en el que se inyectan fibrillas preformadas de alfa-sinucleína en el estómago y el intestino delgado proximal. Durante los siguientes dos meses, observaron un aumento sostenido de alfa-sinucleína anómala marcada químicamente dentro de las neuronas intestinales. Esta acumulación coincidió con un tránsito intestinal más lento y una reducción en la cantidad de heces, reflejando el estreñimiento observado en muchas personas con Parkinson.
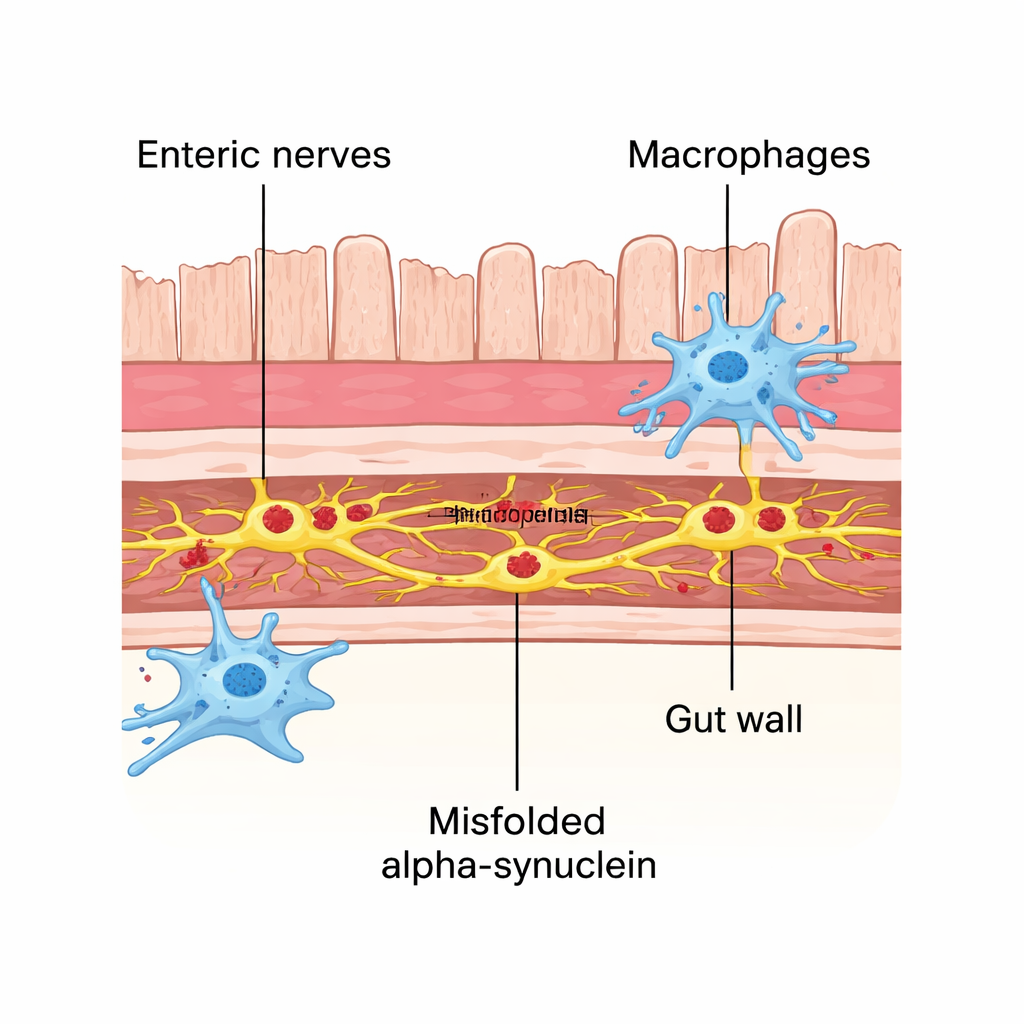
Las células inmunitarias intestinales actúan como primeras respondedores
La pared intestinal contiene células inmunitarias residentes llamadas macrófagos que se comunican constantemente con las neuronas vecinas y ayudan a mantener la salud del tejido. En este modelo, estos macrófagos hicieron más que reaccionar ante el daño: contactaron físicamente con los cúmulos nerviosos afectados con mayor frecuencia y albergaban pequeños puntos de la proteína mal plegada en su interior. Cuando los investigadores agotaron estos macrófagos mediante un tratamiento con anticuerpos, la patología por alfa-sinucleína en las neuronas entéricas aumentó significativamente. Esto sugiere que los macrófagos intestinales desempeñan un papel protector temprano, actuando como limpiadores celulares que engullen y eliminan la proteína tóxica de las neuronas cercanas antes de que pueda propagarse.
Una etiqueta molecular que ayuda—y perjudica
Para entender cómo estas células inmunitarias reconocen lo que deben eliminar, el equipo recurrió a la secuenciación de ARN de célula única, perfilando miles de células inmunitarias intestinales individuales. Identificaron subtipos específicos de macrófagos en las capas musculares del intestino que activaron genes vinculados con la fagocitosis y la degradación de proteínas, en particular componentes del sistema del complemento —una vía de etiquetado molecular más conocida por su papel en la sangre. Un actor clave, C1q, estaba altamente activo en estos macrófagos intestinales. Bajo el microscopio, C1q cubría las neuronas entéricas afectadas, y los macrófagos contenían puntitos positivos tanto para C1q como para la alfa-sinucleína mal plegada, lo que indica que C1q ayuda a marcar la proteína tóxica para su eliminación. Cuando los científicos usaron ratones genéticamente carecientes de C1q, la patología neuronal por alfa-sinucleína empeoró y los macrófagos internalizaron menos cúmulos proteicos. Sin embargo, sorprendentemente, estos ratones deficientes en C1q mostraron una motilidad intestinal algo mejor que la de los ratones normales expuestos a las mismas fibrillas, lo que sugiere que el propio proceso que elimina la proteína tóxica también puede perturbar la función intestinal —probablemente al recortar o debilitar las conexiones nerviosas que controlan el movimiento.
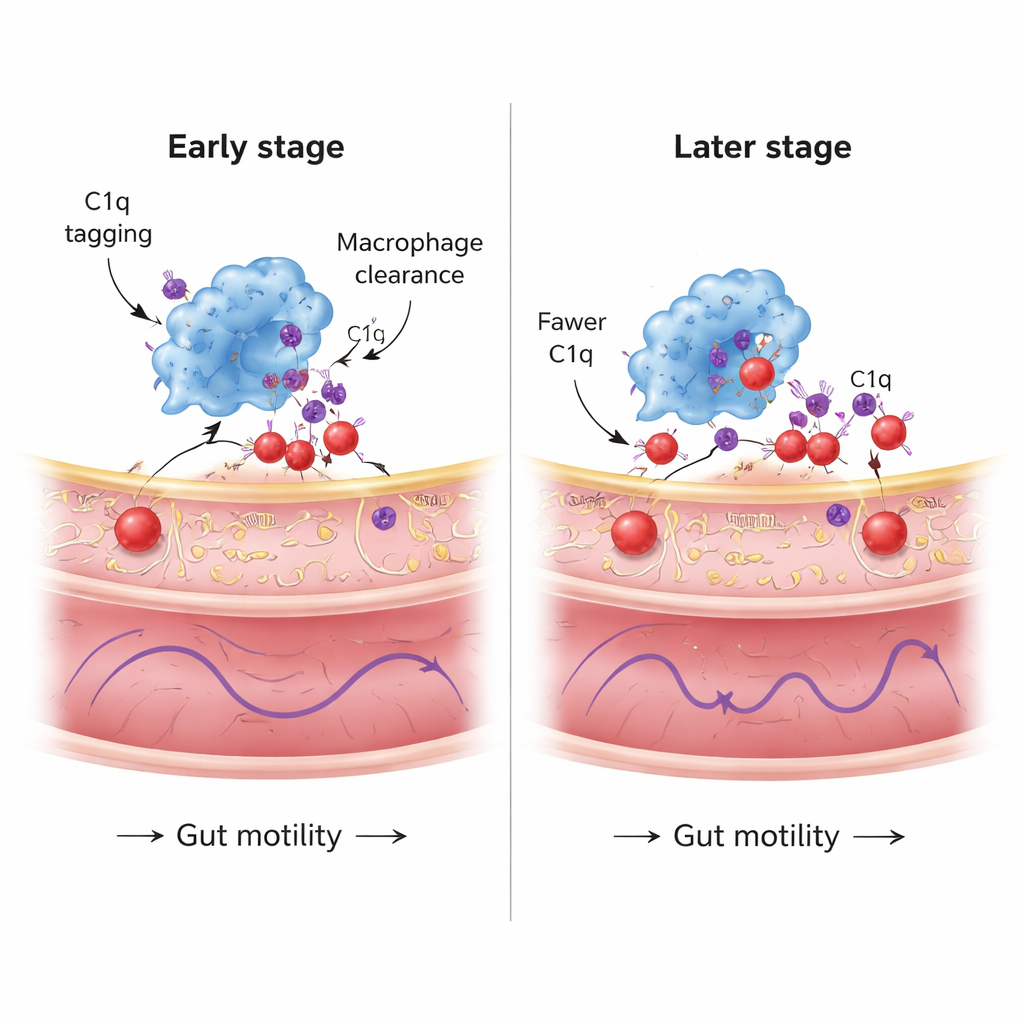
Un sistema protector que se debilita con el tiempo
El estudio también siguió esta respuesta de limpieza durante un periodo más largo. Alrededor de un mes después de la introducción de la alfa-sinucleína, los macrófagos mostraron una expresión robusta de C1q y muchos puntos de proteína etiquetada con C1q dentro de sus cuerpos celulares, y C1q decoraba ampliamente las neuronas entéricas. Sin embargo, a los dos meses, aunque los niveles globales de C1q en los macrófagos se mantenían, el número de puntitos internalizados de C1q/alfa-sinucleína y la cantidad de C1q depositada sobre las neuronas había disminuido. Al mismo tiempo, la patología neuronal en el intestino continuó aumentando. Los análisis genéticos sugirieron que la captación sostenida de proteína mal plegada sobrecarga la maquinaria de manejo de proteínas de los macrófagos, activando vías de estrés relacionadas con proteínas mal plegadas, lisosomas e incluso muerte celular. En otras palabras, la capacidad protectora de los macrófagos parece ser finita: inicialmente contienen la patología, pero a medida que se acumula el estrés, su habilidad para eliminar la alfa-sinucleína disminuye.
Lo que esto significa para el Parkinson y el intestino
El trabajo dibuja un panorama matizado de cómo las células inmunitarias intestinales moldean los cambios tempranos similares al Parkinson en el intestino. Al principio, los macrófagos residentes ayudan utilizando C1q para etiquetar y engullir la alfa-sinucleína mal plegada de las neuronas entéricas, limitando su propagación. Pero este mismo recorte impulsado por el complemento puede perjudicar la señalización nerviosa y enlentecer el intestino, contribuyendo al estreñimiento. Con el tiempo, el sistema de eliminación de los macrófagos, cargado de estrés, se debilita, permitiendo que se acumule más patología incluso cuando la función intestinal y la afectación cerebral divergen. Para los pacientes, esto sugiere que dirigir la actividad de los macrófagos o la señalización del complemento en el intestino —con el objetivo de mejorar la eliminación segura evitando la pérdida excesiva de sinapsis— podría algún día ser una estrategia para tratar o prevenir los síntomas intestinales relacionados con el Parkinson y quizás influir en el curso más amplio de la enfermedad.
Cita: Mackie, P.M., Koshy, J.M., Bhogade, M.H. et al. C1q-dependent clearance of alpha-synuclein allows macrophages to transiently limit enteric synucleinopathy in male mice. Nat Commun 17, 1877 (2026). https://doi.org/10.1038/s41467-026-68641-8
Palabras clave: Enfermedad de Parkinson, sistema nervioso entérico, alfa-sinucleína, células inmunitarias intestinales, complemento C1q