Clear Sky Science · es
Nanorobots camuflados apuntan y regulan los patrones de comunicación entre orgánulos subcelulares de macrófagos para promover la regeneración neural
Por qué importan los pequeños ayudantes “encubiertos” en las lesiones medulares
La lesión de la médula espinal a menudo conlleva parálisis de por vida porque el tejido nervioso dañado es extremadamente difícil de reparar. Una razón principal es que el sitio de la lesión se convierte en una zona hostil llena de inflamación y estrés celular que bloquea la curación. Este estudio describe un nuevo tipo de nanorobot camuflado que viaja por el torrente sanguíneo, evade las defensas del organismo y reprograma a las células inmunitarias en el lugar de la lesión para que cambien del modo agresivo al modo reparador, ayudando a que los nervios vuelvan a crecer en animales con daño medular.
El problema: una inflamación que no se apaga
Tras una lesión medular, la primera oleada de daño proviene del trauma físico en sí. Pero una segunda oleada, más lenta, está impulsada por la inflamación, por moléculas tóxicas llamadas especies reactivas de oxígeno y por una muerte celular generalizada. Células inmunitarias conocidas como macrófagos acuden a limpiar los restos. Al principio, adoptan un estado agresivo “M1” que elimina patógenos y células dañadas, pero también libera señales inflamatorias intensas. Para que comience una verdadera reparación, estas mismas células deben después cambiar a un estado calmante “M2” que favorezca la reparación tisular, el crecimiento de vasos sanguíneos y la regeneración nerviosa. Desgraciadamente, el estrés intenso dentro del tejido lesionado puede atrapar a los macrófagos en el nocivo estado M1, atrapando el tejido en un ciclo de inflamación crónica que impide la recuperación funcional.
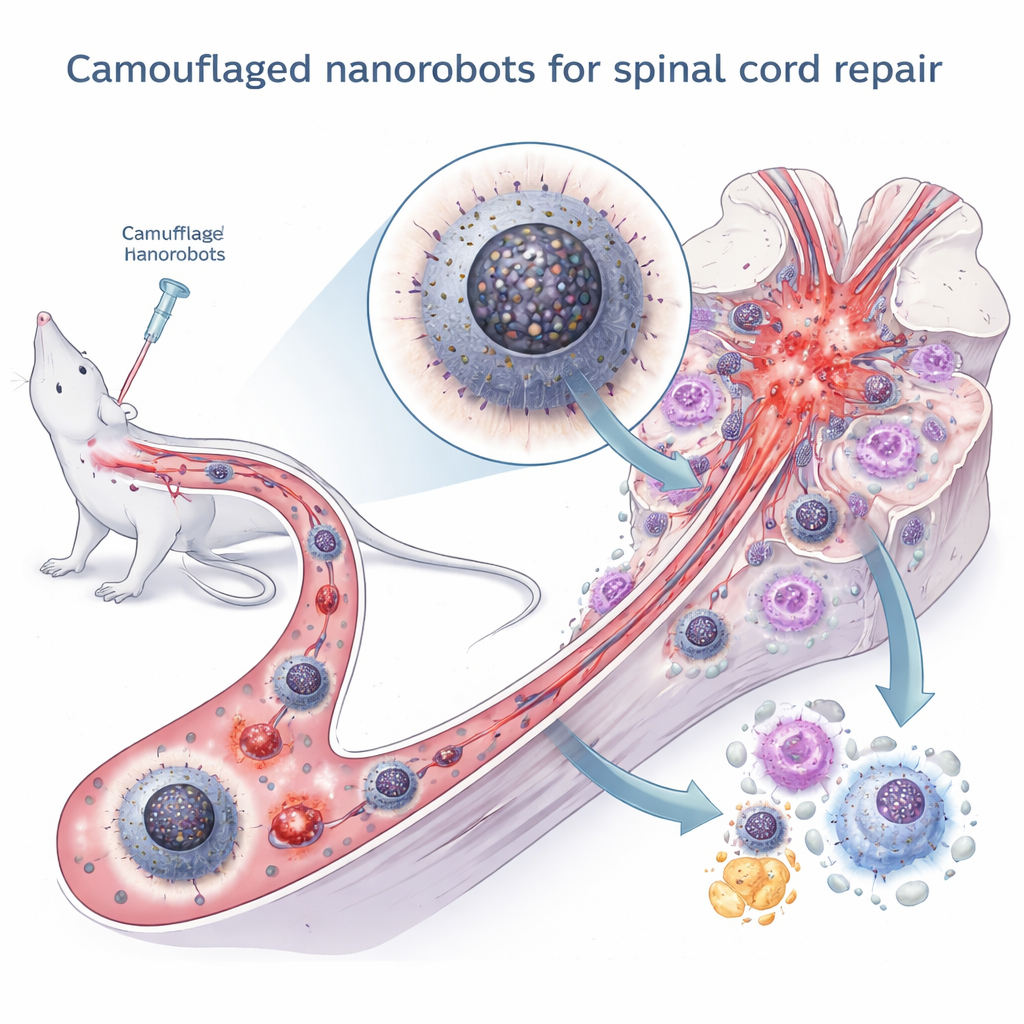
Una conversación oculta entre partes de la célula
Los autores se centraron en una “conversación” interna sutil pero crucial dentro de los macrófagos: la comunicación entre dos compartimentos clave, el retículo endoplásmico (que ayuda a plegar proteínas y almacena calcio) y las mitocondrias (las centrales energéticas de la célula). En condiciones normales, estas estructuras comparten pequeñas cantidades de iones de calcio a través de zonas de contacto especializadas, lo que ayuda a ajustar la producción de energía a las necesidades de la célula. Tras la lesión, sin embargo, el exceso de especies reactivas de oxígeno causa el mal plegamiento de proteínas y estrés en el retículo endoplásmico. Ese estrés, a su vez, impulsa una transferencia excesiva de calcio hacia las mitocondrias, provocando un colapso energético, más moléculas tóxicas y la fuga de ADN mitocondrial al citosol. Ese ADN escapado activa una vía de alarma potente llamada cGAS–STING–NFκB, que refuerza el estado inflamatorio M1 de los macrófagos.
Diseñando un nanorobot camuflado
Para romper este ciclo vicioso, el equipo construyó un nanorobot multicapa llamado BP@D/N. En su núcleo hay puntos cuánticos de fósforo negro, partículas diminutas con fuerte actividad antioxidante y antiinflamatoria pero con escasa estabilidad en el organismo. Estos puntos se empaquetan en una cáscara hueca de polidopamina, un material biocompatible que los protege de degradarse prematuramente y aporta además propiedades antioxidantes. Finalmente, toda la partícula se envuelve con una membrana tomada de neutrófilos activados, un tipo de glóbulo blanco atraído de forma natural a los sitios de inflamación. Este “camuflaje” permite al nanorobot evadir la eliminación inmune, seguir señales inflamatorias hasta la médula lesionada y adherirse a los macrófagos para una captación eficiente.
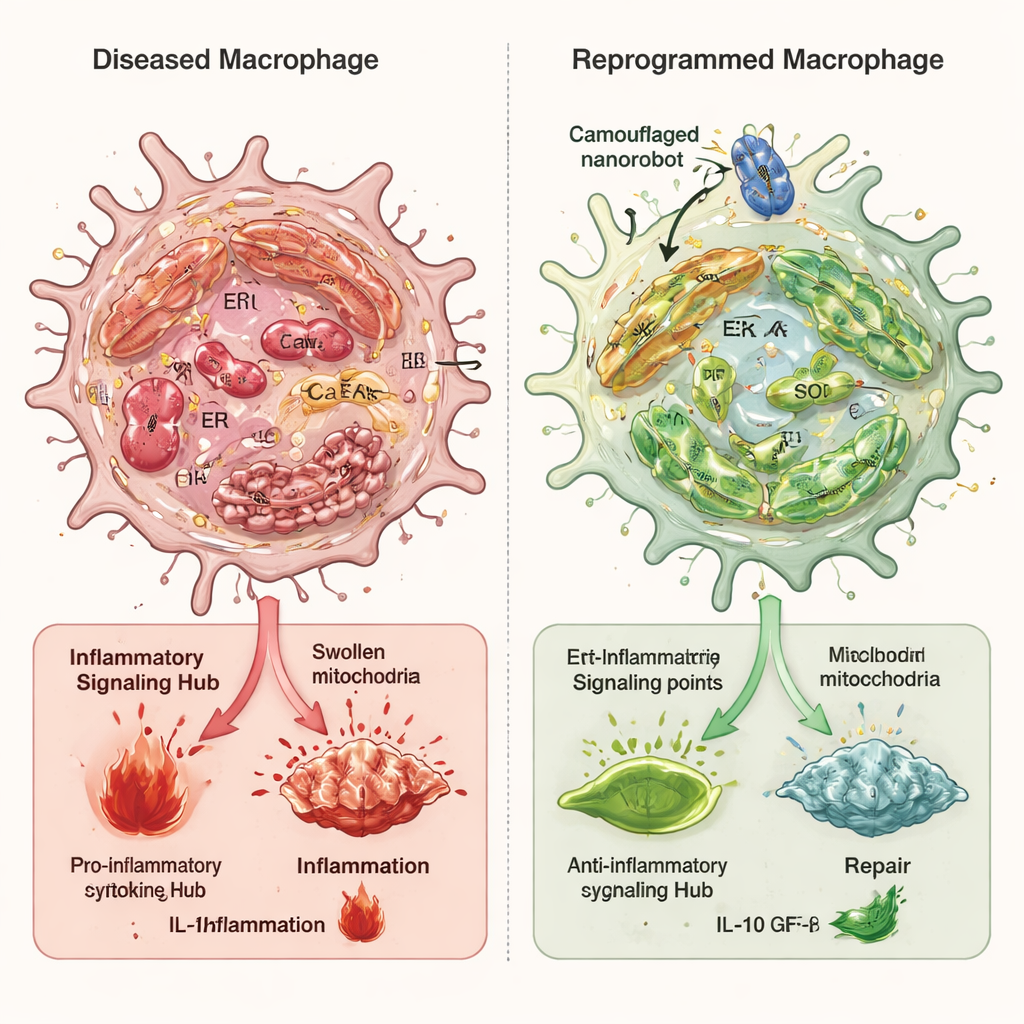
Reprogramando células inmunitarias estresadas
En estudios celulares, los macrófagos expuestos a desencadenantes inflamatorios mostraron altos niveles de estrés en el retículo endoplásmico, mitocondrias hinchadas y dañadas, sobrecarga de calcio y fuerte activación de la vía de alarma cGAS–STING–NFκB. Al tratarse con los nanorobots camuflados, el estrés oxidativo global cayó bruscamente, las membranas internas entre retículo endoplásmico y mitocondrias se volvieron menos hiperconectadas y el calcio mitocondrial volvió hacia la normalidad. Esto evitó que el ADN mitocondrial se filtrara al citosol y atenuó la cascada de señalización inflamatoria. Un actor clave en este proceso fue una enzima llamada Ero1α, que ayuda a controlar el ambiente oxidativo y la liberación de calcio desde el retículo endoplásmico. Los nanorobots redujeron la actividad de Ero1α, y cuando los investigadores aumentaron artificialmente Ero1α, esto anuló en gran medida los beneficios del nanorobot, confirmando su papel central.
De calmar la inflamación a regenerar nervios
Estos cambios internos hicieron que los macrófagos pasaran del destructivo estado M1 al reparador M2. En cultivos, las células orientadas hacia M2 secretaron menos moléculas inflamatorias como TNF-α e IL-6 y más factores de crecimiento que fomentan que las neuronas y las células de soporte crezcan y extiendan axones. En modelos de ratas con lesión medular, la inyección repetida de los nanorobots condujo a menos señales inmunitarias dañinas en la zona de la lesión, menos formación de cicatriz, cavidades más pequeñas y más fibras nerviosas en regeneración. Los animales que recibieron los nanorobots camuflados recuperaron mejor el movimiento de las extremidades traseras, respuestas musculares más fuertes y una mejor estructura vesical en comparación con los no tratados o con tratamientos nanoparticulados menos dirigidos.
Qué podría significar esto para futuros pacientes
Este trabajo muestra que afinar con precisión el estrés interno y la comunicación entre compartimentos celulares puede transformar a las células inmunitarias de dañinas a beneficiosas para los nervios lesionados. Al empaquetar partículas antioxidantes potentes pero frágiles en un nanorobot dirigido y camuflado, los investigadores restauraron un equilibrio más sano entre inflamación y reparación en la médula espinal lesionada de ratas. Aunque queda mucho por hacer antes de que este enfoque pueda probarse en humanos, ofrece un plano prometedor: en lugar de simplemente suprimir la inflamación de forma general, las terapias futuras podrían guiar la maquinaria celular específica dentro de los macrófagos para crear un entorno más favorable a la regeneración neural tras una lesión medular.
Cita: Guo, Q., Wang, W., Jiang, X. et al. Camouflaged nanorobots target and regulate macrophage subcellular organelle crosstalk patterns to promote neural regeneration. Nat Commun 17, 1952 (2026). https://doi.org/10.1038/s41467-026-68636-5
Palabras clave: lesión de la médula espinal, nanorobots, macrófagos, regeneración neural, nanomedicina