Clear Sky Science · es
Caracterización metabólica de las interacciones tumor-inmunidad mediante inmunofluorescencia multiplexada revela mecanismos espaciales de respuesta a la inmunoterapia en carcinoma de pulmón no microcítico (CPNM)
Por qué importa esta investigación
La inmunoterapia ha transformado el tratamiento de algunas personas con cáncer de pulmón avanzado, sin embargo la mayoría de los pacientes siguen viendo crecer su tumor a pesar de estos fármacos potentes. Este estudio plantea una pregunta simple pero crucial: ¿podemos examinar más de cerca el propio tejido tumoral—dónde se ubican las diferentes células y cuánta energía consumen—para predecir quién se beneficiará realmente de la inmunoterapia? Al convertir pequeñas muestras de biopsia en mapas celulares detallados, los investigadores pretenden acercar la atención del cáncer de pulmón a un enfoque verdaderamente personalizado.
Mirando dentro de los tumores pulmonares como un mapa de ciudad
El equipo examinó tejido de 55 personas con carcinoma de pulmón no microcítico (CPNM) avanzado tratadas con inhibidores de puntos de control inmunitario, una clase principal de fármacos inmunoterapéuticos. Antes del tratamiento, sus muestras tumorales se tiñeron con un panel de 44 marcadores usando inmunofluorescencia multiplexada, lo que permitió visualizar muchas proteínas a la vez. Un sistema de aprendizaje profundo identificó luego los tipos celulares clave—como células tumorales, células T, células B, macrófagos y fibroblastos—y clasificó su estado funcional (por ejemplo, activadas, en división o agotadas) así como su perfil metabólico, es decir, cómo generaban y utilizaban energía. En lugar de limitarse a contar células, los investigadores también cartografiaron la posición relativa de las células entre sí, creando regiones tipo vecindario dentro de cada biopsia.
Tumores con gran demanda energética y su entorno inmunitario
Un foco principal fue el metabolismo—las maneras en que las células generan combustible para crecer o defenderse. Los investigadores definieron “vecindarios metabólicos” con distintos niveles y tipos de uso energético, desde actividad baja hasta zonas muy activas ricas en fosforilación oxidativa y glucólisis. Encontraron que tanto las células tumorales como ciertos tipos de células inmunitarias, como los macrófagos, a menudo mostraban vías intensas de producción de energía. Algunos de estos patrones se asociaron con los resultados de los pacientes. Por ejemplo, los tumores con alta actividad en vías que les ayudan a utilizar aminoácidos y alimentar el ciclo del TCA tendieron a corresponder a pacientes que recidivaron pronto tras la inmunoterapia. En contraste, algunas células plasmáticas (células B productoras de anticuerpos) con vías energéticas activas dentro del tumor fueron más frecuentes en pacientes con mejores resultados, lo que sugiere que no todas las células muy energéticas son perjudiciales; algunas pueden favorecer una inmunidad antitumoral eficaz.
Actores inmunitarios buenos y malos en el paisaje tumoral
Más allá de la simple abundancia, el tipo y el comportamiento de las células inmunitarias también importaron. Los macrófagos que portaban la molécula citotóxica granzima B se asociaron fuertemente con una peor supervivencia libre de progresión, especialmente cuando se encontraban en vecindarios metabólicamente bajos o inactivos. Estas regiones pueden representar áreas pobres en nutrientes o dormantes donde el ataque inmunitario está debilitado. Por el contrario, ciertos arreglos de células T reguladoras (Tregs) y fibroblastos en el límite entre el tumor y el tejido circundante parecieron relacionarse con mejores resultados, posiblemente reflejando un patrón en el que las células supresoras permanecen en los bordes en lugar de infiltrarse profundamente en el tumor. Las proporciones entre distintos tipos de células inmunitarias, como granulocitos frente a células T CD8, también se asociaron con la respuesta, subrayando que el equilibrio y la localización inmunitaria, no solo los recuentos totales, son importantes.
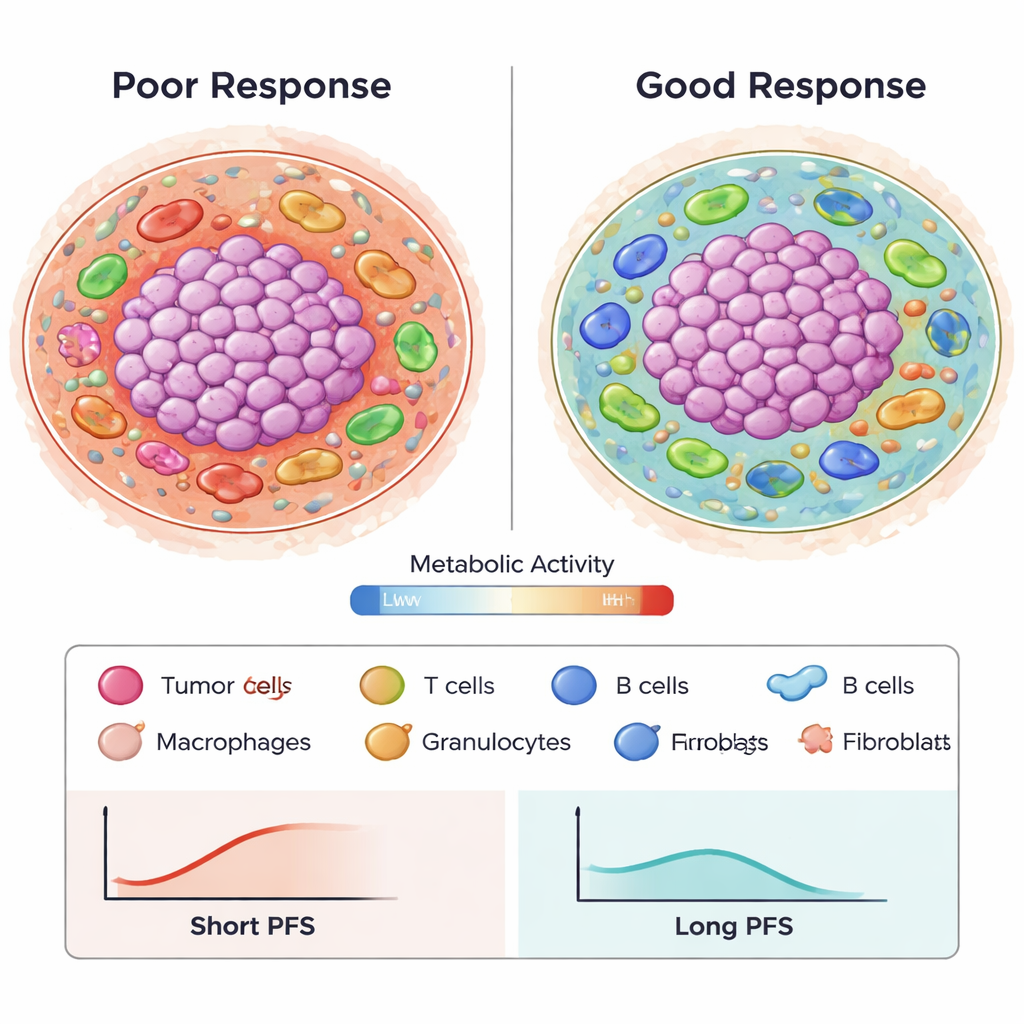
De imágenes complejas a patrones predictivos
Para dar sentido a más de un millón de características espaciales diseñadas que describían tipos celulares, distancias y estados metabólicos, los autores emplearon un método avanzado de selección de características (Stabl) y herramientas de modelado de supervivencia. Identificaron 87 características clave, muchas de ellas reflejando cómo las células tumorales metabólicamente activas interactúan con macrófagos y células T, o cómo tipos específicos de células inmunitarias se agrupan cerca de vasos sanguíneos y fibroblastos. Usando estas características en modelos de regresión de Cox, construyeron un predictor que estimó la supervivencia libre de progresión con una precisión (AUC) alrededor de 0,8 a lo largo de 24 meses, superando marcadores tradicionales únicos como la tinción de PD-L1 o la carga mutacional tumoral en trabajos publicados previamente. Es importante señalar que varias características se reprodujeron en dos cohortes de pacientes independientes, lo que sugiere que los patrones no son ruido aleatorio.
Qué significa esto para los pacientes
Para el público general, la idea principal es que la ubicación de las células en un tumor pulmonar y la forma en que obtienen energía pueden ayudar a explicar por qué algunos pacientes responden bien a la inmunoterapia y otros no. Este estudio muestra que la información espacial y metabólica detallada de una biopsia de rutina, combinada con inteligencia artificial y modelado estadístico, puede revelar firmas de probable beneficio o resistencia. Aunque el trabajo requiere validación en grupos más grandes y en secciones de tejido completas, traza un camino hacia futuras pruebas que podrían indicar a los médicos, antes de iniciar el tratamiento, qué pacientes probablemente obtendrán control duradero con inmunoterapia y cuáles podrían necesitar estrategias alternativas o combinadas.
Cita: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Palabras clave: resistencia a la inmunoterapia, cáncer de pulmón no microcítico, microambiente tumoral, biología espacial, metabolismo del cáncer