Clear Sky Science · es
H3K9me2 mediado por G9a orquesta la regeneración epitelial intestinal mediante el silenciamiento epigenético de genes relacionados con el ciclo celular
Por qué importa la autorreparación intestinal
Cada día, el revestimiento de tu intestino afronta condiciones duras: ácido gástrico, fragmentos de comida y trillones de microbios. Sin embargo, este tejido no solo sobrevive, sino que se repara constantemente. Cuando ese sistema de reparación falla —tras radioterapia, en la enfermedad inflamatoria intestinal o durante infecciones graves— las personas pueden sufrir dolor, hemorragias y complicaciones potencialmente mortales. Este estudio descubre un “interruptor” oculto dentro de las células intestinales que les ayuda a decidir cuándo dejar de estar en reposo y empezar a reconstruir, ofreciendo pistas para nuevos tratamientos que podrían potenciar el equipo de reparación natural del intestino.
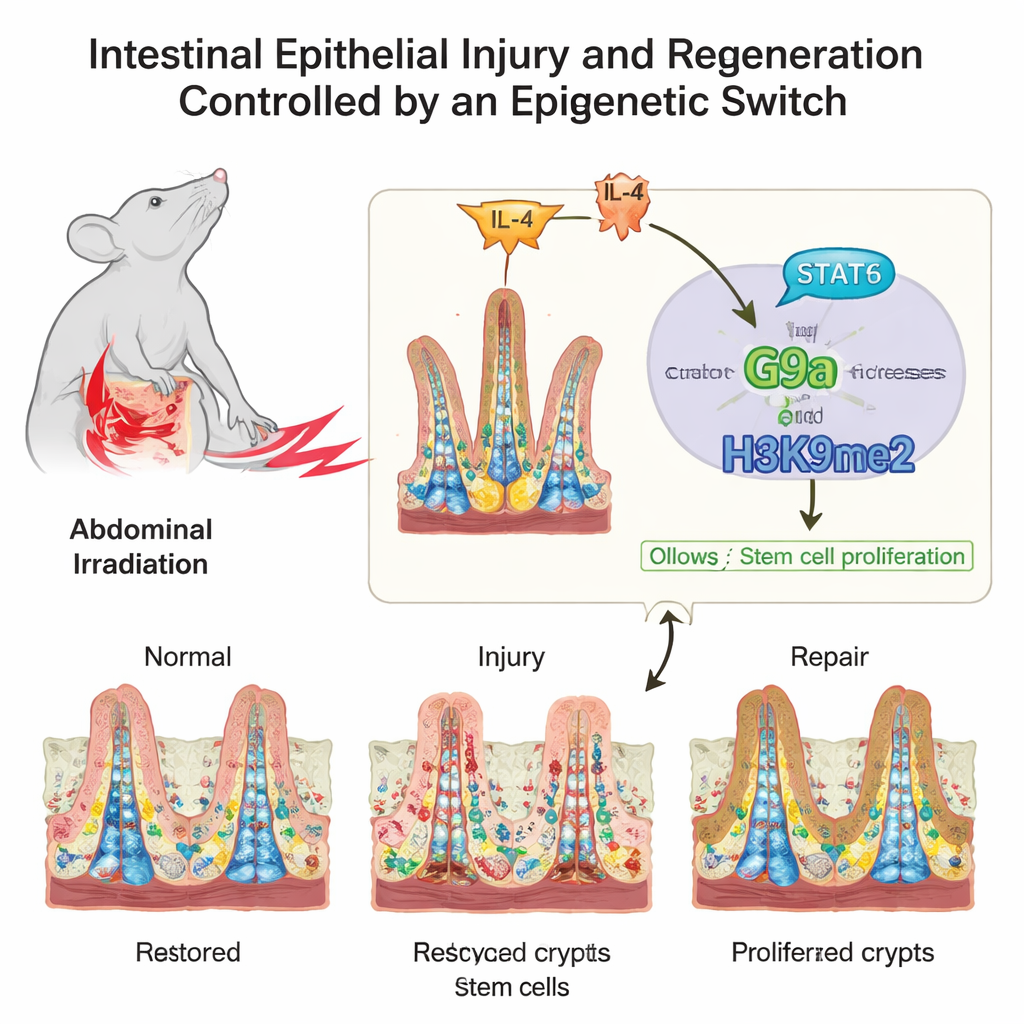
Una arquitectura delicada bajo estrés constante
La superficie interna del intestino parece una alfombra peluda al microscopio, con vellosidades en forma de dedo que absorben nutrientes y cavidades llamadas criptas donde viven las células madre. Estas células madre y sus hijas de rápida división deben hallar un equilibrio entre la renovación habitual y la reparación de emergencia. Los autores se centraron en cómo las marcas químicas en las proteínas que empaquetan el ADN, llamadas histonas, influyen en ese equilibrio. Estas marcas no cambian los genes en sí, sino que actúan más como reguladores de intensidad, subiendo o bajando la actividad de grupos de genes conforme el intestino pasa de la vida normal al daño y vuelve a la salud.
Una marca epigenética que sigue el daño y la curación
Usando ratones expuestos a radiación —una causa común de lesión intestinal durante el tratamiento del cáncer— los investigadores analizaron muchas marcas de histonas en las criptas ricas en células madre. Una marca, conocida como H3K9me2, aumentó de forma notable cuando el intestino pasó del daño a la reparación. Su enzima escritora, una proteína llamada G9a, siguió el mismo patrón. El equipo examinó luego muestras humanas de pacientes que habían recibido radioterapia pélvica, así como personas con enfermedad de Crohn. En ambos casos, niveles más altos de H3K9me2 y G9a en células intestinales se correlacionaron con mejores signos de reparación tisular, lo que sugiere que este sistema se conserva entre ratones y humanos.
Cuando el interruptor de reparación se rompe
Para comprobar si esta marca era solo un espectador o realmente impulsaba la curación, los científicos eliminaron G9a específicamente del revestimiento intestinal de ratones o bloquearon su actividad con un fármaco. En ambos casos, los niveles de H3K9me2 cayeron. Tras radiación o lesión química, estos ratones perdieron más peso, tuvieron intestinos más cortos y dañados, y presentaron menos criptas y células madre regenerantes que los animales normales. Incluso sin lesión deliberada, el revestimiento intestinal de los ratones deficientes en G9a se veía atrofiado: las criptas eran menos profundas, las vellosidades más cortas y disminuyeron los números de células madre y de sus descendientes especializados. Pequeños “mini‑intestinos” cultivados a partir de estas células en placa también crecieron mal, subrayando que este sistema molecular es central para la renovación cotidiana del intestino.
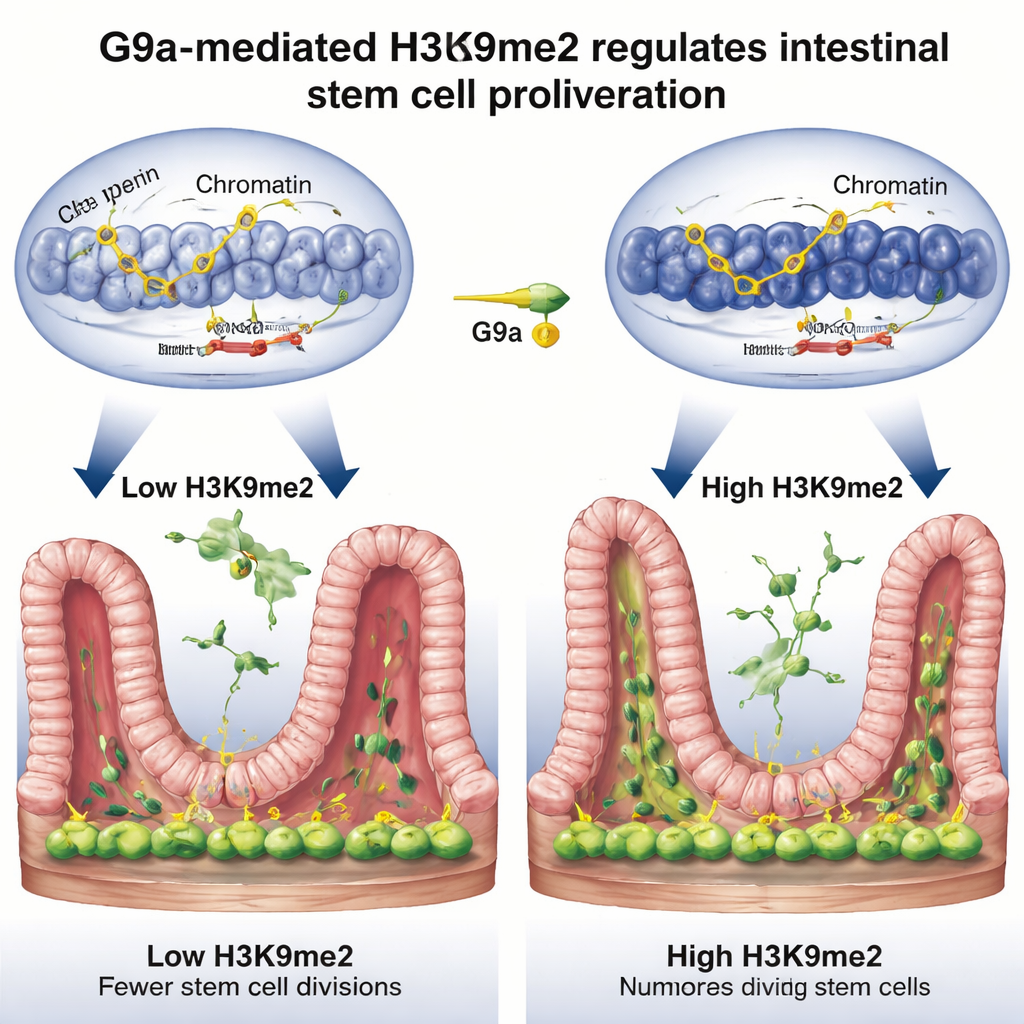
Soltando los frenos de la división celular
Profundizando, el equipo preguntó qué genes controla este interruptor de reparación. Combinando tres métodos genómicos potentes, hallaron que H3K9me2, depositada por G9a, tiende a localizarse en tramos de ADN que normalmente actúan como frenos del ciclo celular —genes como Rb1cc1, Rb1, Cdkn1a y Pten, que ralentizan o detienen la división celular. Cuando faltaba G9a, la marca química desaparecía de estas regiones, el ADN circundante se abría y esos genes freno se activaban con más fuerza, llevando a una proliferación más lenta de las células madre. Durante la reparación normal tras la lesión, los niveles de H3K9me2 en estos genes aumentaban, su actividad disminuía y las células madre tenían mayor libertad para dividirse y reconstruir el revestimiento. En esencia, G9a y H3K9me2 silenciaban temporalmente las señales de “alto” para que el tejido pudiera regenerarse.
Una cadena de señalización desde señales inmunes hasta la reparación
El intestino no actúa en solitario; escucha continuamente señales del sistema inmune. Los investigadores trazaron una de esas señales río arriba de G9a. Tras la lesión, aumentaron los niveles del mensajero inmunitario IL‑4, lo que activó una proteína llamada STAT6 dentro de las células intestinales. STAT6 activado se unió directamente a la región de control del gen G9a, impulsando su producción. Esto creó una cadena de mando: IL‑4 activa STAT6, STAT6 aumenta G9a, y G9a añade H3K9me2 para silenciar genes freno del ciclo celular, permitiendo que las células madre se expandan y restauren el revestimiento dañado.
Qué significa esto para futuros tratamientos
Para un no especialista, estos hallazgos muestran que la reparación intestinal está guiada no solo por los genes, sino por marcas químicas reversibles que afinan cuándo se usan esos genes. La vía IL‑4–STAT6–G9a–H3K9me2 actúa como un panel de control interno que afloja los frenos de la división de las células madre el tiempo suficiente para curar y luego puede restablecerse. En el futuro, terapias que potencien con suavidad esta vía —como fármacos o herramientas genéticas que aumenten G9a en el momento y lugar adecuados— podrían ayudar a los pacientes a recuperarse más rápido de lesiones por radiación, brotes de enfermedad inflamatoria intestinal u otras condiciones que dañan el revestimiento intestinal, minimizando a la vez los riesgos de crecimiento celular descontrolado.
Cita: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Palabras clave: regeneración intestinal, epigenética, células madre, metilación de histonas, enfermedad inflamatoria intestinal