Clear Sky Science · es
WDR5 remodela los condensados de NANOG para impulsar programas de transcripción y mantener la identidad de células madre
Por qué importa esto para las células madre y el cáncer
Las células madre tienen la notable capacidad de convertirse en muchos tipos celulares diferentes, una propiedad que impulsa el desarrollo temprano, la reparación de tejidos y, desafortunadamente, algunos cánceres. Este estudio revela cómo dos proteínas clave, NANOG y WDR5, cooperan para mantener a las células madre en ese estado flexible. Al mostrar que WDR5 puede remodelar físicamente la forma en que NANOG se agrupa en el ADN, el trabajo conecta la física de las gotas proteicas dentro del núcleo con el control de los genes tanto en células madre sanas como en la leucemia.
Proteínas que deciden el futuro de una célula
Las células madre embrionarias conservan la pluripotencia—es decir, la capacidad de convertirse en casi cualquier célula—gracias a reguladores maestros como NANOG, OCT4 y SOX2. Estas proteínas activan y silencian redes enteras de genes. NANOG es especialmente central: no solo se une al ADN, sino que también recluta grandes complejos enzimáticos que añaden marcas químicas activadoras a las histonas, las proteínas que empaquetan el ADN. WDR5 es otro actor crucial. Ayuda a las máquinas que modifican histonas a colocar marcas que señalan genes activos. Aunque se sabe que tanto NANOG como WDR5 sostienen la identidad de las células madre, cómo se comunican entre sí a nivel molecular, y si eso afecta la forma en que forman pequeñas gotas—o “condensados”—en el núcleo, no quedaba claro.
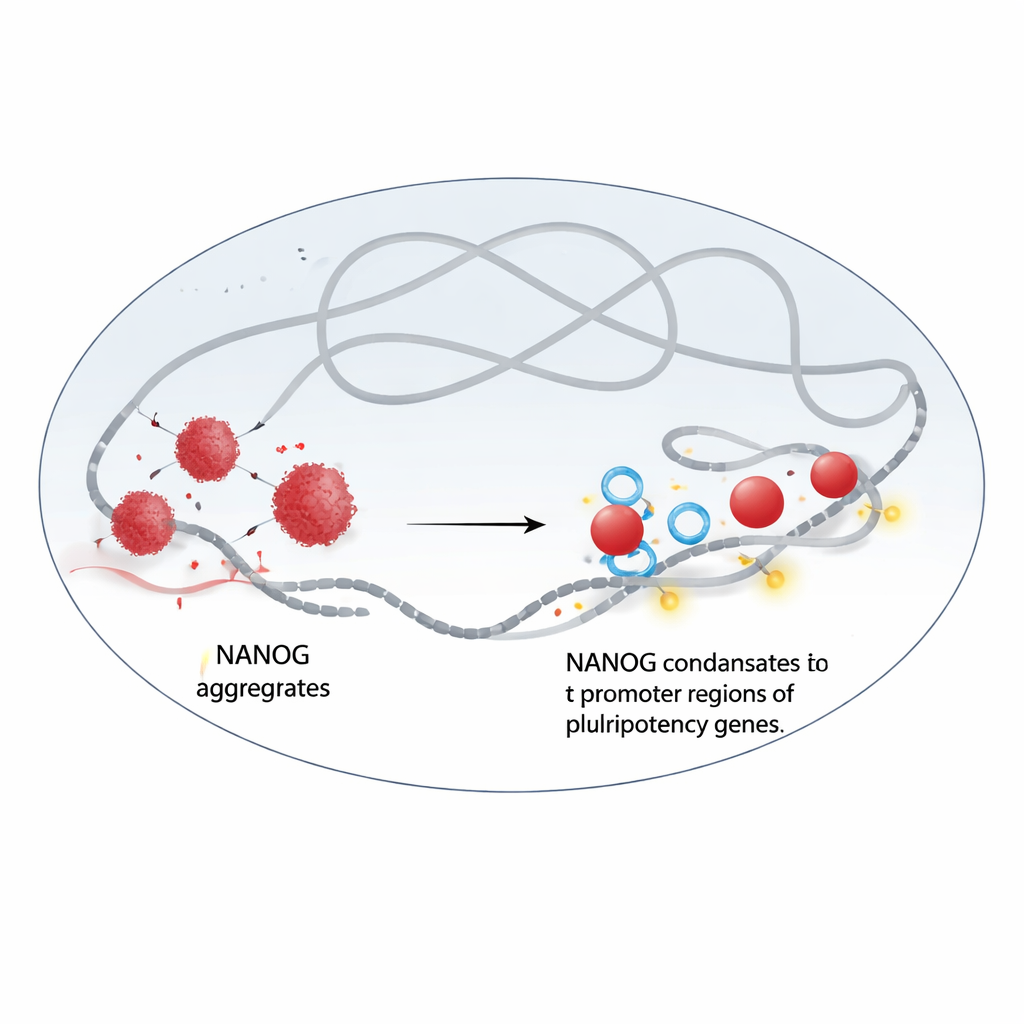
De grumos a gotas líquidas
Los autores descubrieron que NANOG y WDR5 interactúan directamente. Cuando NANOG se purifica por sí sola, tiende a agruparse en agregados irregulares, parecidos a sólidos. Mediante microscopía electrónica y experimentos de fluorescencia, el equipo mostró que la adición de WDR5 reorganiza esos grumos en gotas redondeadas, de aspecto líquido, que se comportan como condensados dinámicos. En células vivas, NANOG y WDR5 se reúnen en puntos nucleares brillantes que se disuelven rápidamente al tratarse con un químico conocido por perturbar la separación de fases líquido–líquido. Cuando esto ocurre, ambas proteínas pierden gran parte de su unión a la cromatina, el complejo ADN–proteína que almacena nuestra información genética, y su presencia en genes clave de pluripotencia cae drásticamente.
Un apretón de manos molecular especial
Para entender la asociación en detalle atómico, los investigadores resolvieron la estructura cristalina de la región de NANOG que se une al ADN cuando está ligada a WDR5. A diferencia de muchos otros socios de WDR5, que usan bucles cortos y flexibles, NANOG interactúa con WDR5 mediante una superficie extendida que incluye un brazo no estructurado y hélices cercanas. Un único aminoácido arginina en NANOG, en la posición 153, se inserta profundamente en un canal central de WDR5, formando una parte clave de la interacción tipo “cerradura y llave”. Cambiar este residuo por alanina (la mutación R153A) elimina en gran medida la unión. Importante: la NANOG mutante todavía puede unirse al ADN, pero WDR5 ya no puede remodelar eficientemente sus agregados en gotas fluidas, lo que indica que este contacto específico es esencial para formar condensados funcionales.
Mantener las células madre jóvenes—y qué sucede cuando falla
Cuando los autores diseñaron células madre embrionarias de ratón para que expresaran solo la NANOG mutante R153A, las consecuencias fueron dramáticas. Las células mutantes perdieron las colonias apretadas y en forma de cúpula típicas de las células pluripotentes y se aplanaron, una señal visual de diferenciación. Formaron menos colonias positivas para fosfatasa alcalina, otro sello de la condición de célula madre, y disminuyeron muchos genes centrales de pluripotencia como Nanog mismo, Sox2, Esrrb y Klf4. Al mismo tiempo, se activaron genes asociados con linajes concretos, incluidos reguladores del hueso y del desarrollo. El perfilado a escala del genoma reveló que NANOG y WDR5 dejaron de coinmocar miles de promotores, y dos marcas histónicas activadoras clave, H3K4me3 y H4K16ac, se perdieron específicamente en estos sitios compartidos. Temprano durante la diferenciación, estas marcas químicas y los nuevos transcritos de ARN disminuyeron antes de que cayeran los niveles totales de ARNm, lo que apunta a una falla primaria en el mantenimiento de la cromatina activa.
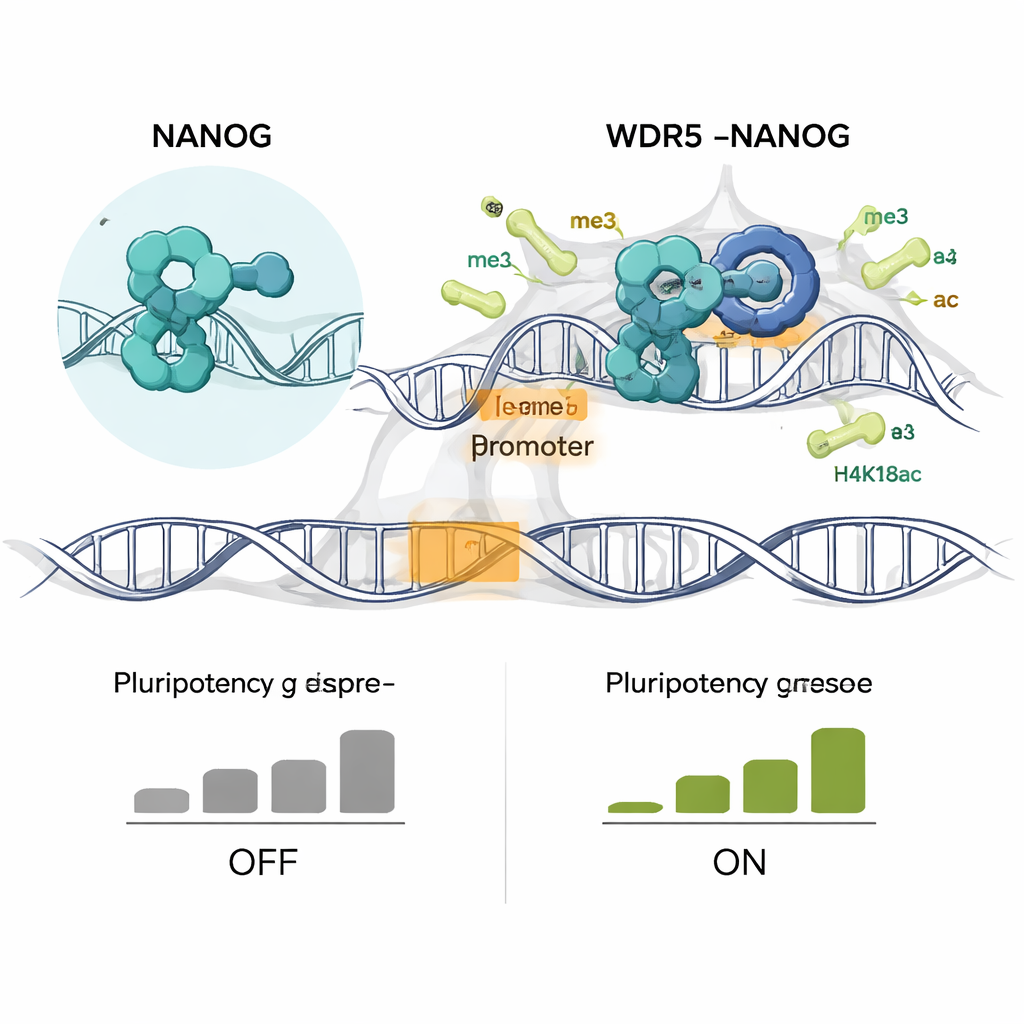
Convertir un mecanismo fundamental en una estrategia contra el cáncer
Dado que redes génicas similares impulsan algunas células madre cancerosas, el equipo probó si interrumpir el eje NANOG–WDR5 podría frenar células madre de leucemia en un modelo de ratón de leucemia mieloide aguda. Un fármaco de pequeña molécula, C16, que se une al mismo bolsillo de WDR5 utilizado por NANOG, debilitó selectivamente la interacción WDR5–NANOG. En células de leucemia, C16 redujo drásticamente la formación de colonias, agotó la población con rasgos de células madre y empujó a las células hacia destinos mieloides maduros, mientras que respetó las células madre sanguíneas normales mucho más que un fármaco anti-leucemia existente que apunta a otro socio de WDR5. La secuenciación de ARN mostró que C16 apagó programas génicos de pluripotencia y autorrenovación y potenció vías de diferenciación. En ratones, el tratamiento con C16 redujo las poblaciones de células madre y progenitores leucémicos, subrayando la promesa terapéutica de apuntar a esta asociación proteica.
Panorama general: cómo las gotas ayudan a decidir la identidad celular
Este trabajo revela que WDR5 hace más que situarse en la cromatina y reclutar enzimas: puede remodelar físicamente a NANOG, transformándolo de agregados inertes en condensados líquidos flexibles que se sitúan en promotores de genes de pluripotencia y atraen marcas histónicas activadoras. Cuando este remodelado se bloquea—ya sea por una mutación precisa en NANOG o por una molécula pequeña que interrumpe su contacto—las células madre pierden su identidad y las células madre cancerosas pierden su capacidad de autorrenovación. Para un lector no especializado, el mensaje clave es que pequeños cambios en la forma en que las proteínas se ensamblan en gotas sobre el ADN pueden tener consecuencias enormes sobre si una célula se mantiene joven y flexible, madura hacia un destino específico o alimenta una enfermedad.
Cita: Wang, D., Shi, X., Xie, J. et al. WDR5 remodels NANOG condensates to drive transcriptional programs and sustain stem cell identity. Nat Commun 17, 1907 (2026). https://doi.org/10.1038/s41467-026-68623-w
Palabras clave: pluripotencia de células madre, NANOG, WDR5, separación de fases, células madre de leucemia