Clear Sky Science · es
Las sintasas de señalización de quorum con doble función DspII y DspI coordinan el cambio de virulencia en Pseudomonas aeruginosa
Cómo un supergermen hospitalario cambia su estrategia de ataque
Pseudomonas aeruginosa es un patógeno hospitalario notorio que puede causar infecciones persistentes en los pulmones y en heridas, especialmente en pacientes vulnerables. Sobrevive alternando entre dos estilos de vida: una comunidad protegida y de crecimiento lento llamada biopelícula y una forma agresiva y móvil que invade tejidos. Este estudio revela cómo la propia bacteria decide cuándo romper una biopelícula de larga duración y lanzar un ataque agudo repentino, desvelando posibles puntos débiles nuevos para futuros tratamientos.
Una vida microbiana entre esconderse y atacar
Muchas infecciones bacterianas se desarrollan en etapas. Al principio, las células libres se desplazan por el organismo y despliegan armas potentes que dañan los tejidos del hospedador. Más tarde, a menudo se establecen en biopelículas: capas gruesas y viscosas adheridas a superficies como catéteres, tejido pulmonar o heridas. En estas comunidades, las células están envueltas en una matriz protectora que las hace difíciles de eliminar con antibióticos o las defensas inmunitarias. Sin embargo, las biopelículas no son un callejón sin salida. Las células pueden salir, recuperar la motilidad e iniciar nuevas rondas de infección aguda en otros lugares. Hasta ahora, no estaba claro cómo Pseudomonas aeruginosa coordina activamente este cambio de persistencia crónica a enfermedad agresiva.
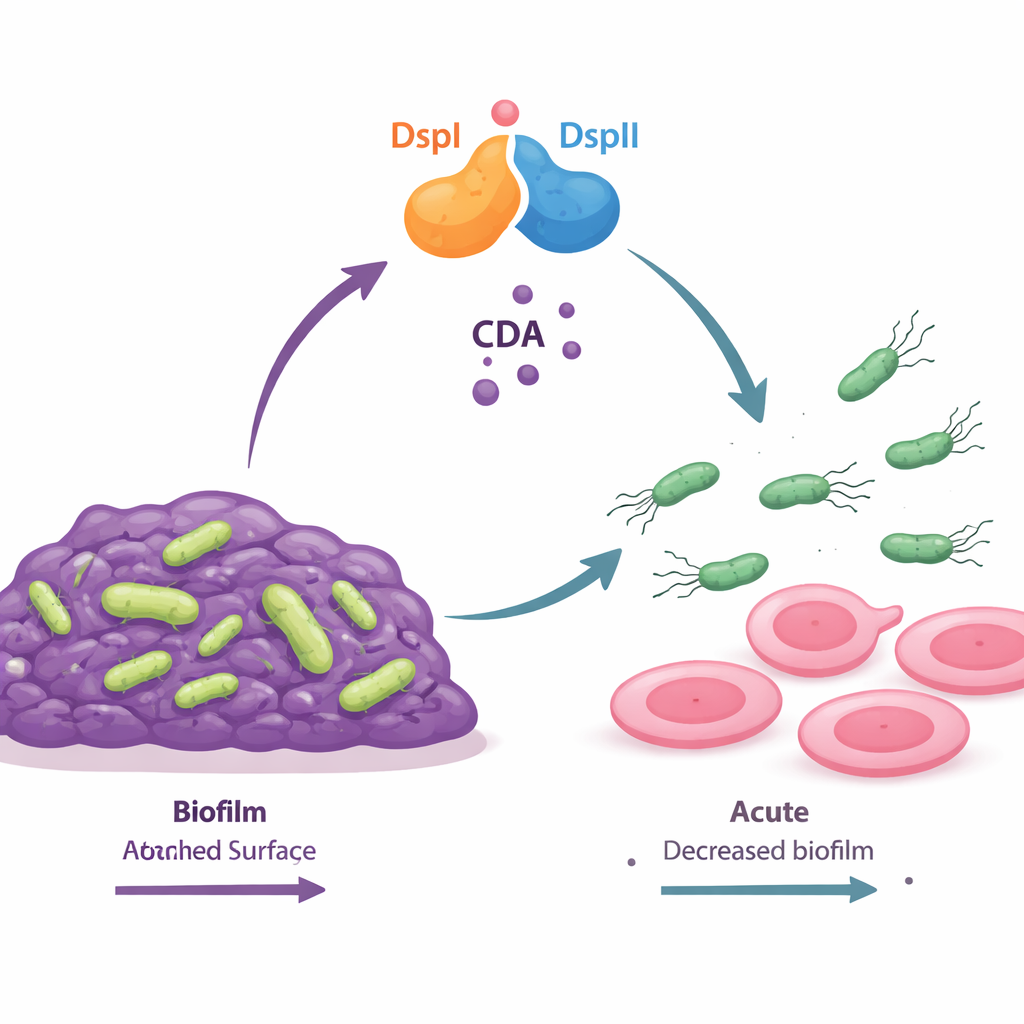
Un interruptor de dos proteínas que fabrica una señal química de “arranque”
Los autores descubrieron que dos proteínas bacterianas, llamadas DspI y DspII, actúan en conjunto como una especie de interruptor molecular. Ambas son enzimas del mismo tipo general y están situadas una junto a la otra en el genoma bacteriano, activándose a la vez a medida que la población se densifica. Cuando forman pareja, sintetizan una pequeña señal grasa llamada cis-2-decenoico (CDA), parte de un grupo más amplio de moléculas de comunicación conocidas como señales DSF. Las bacterias mutantes que carecían de DspI o DspII no podían producir CDA, formaban biopelículas inusualmente gruesas y perdían su capacidad de desplazarse por la superficie. Solo cuando se restauraban ambas proteínas juntas las células recuperaban la producción normal de señal, la ruptura de la biopelícula y la motilidad, demostrando que las dos enzimas funcionan como un equipo interdependiente.
De la señal química al movimiento y la huida
La CDA no actúa sola; se integra en el cableado interno de la bacteria. El equipo mostró que la CDA reduce los niveles de otra molécula mensajera, el di-GMP cíclico, al potenciar la actividad de una enzima específica llamada RbdA que degrada este mensajero. Altos niveles de di-GMP cíclico normalmente fomentan la formación de biopelículas estimulando la producción de matriz azucarada y suprimiendo los flagelos, las diminutas hélices que impulsan la natación. Cuando está presente CDA, los niveles de di-GMP cíclico caen, un regulador llamado FleQ cambia de modo, la producción de azúcares adhesivos disminuye y los flagelos se extienden y fortalecen. Como resultado, las biopelículas se aflojan y las células recuperan la capacidad de desplazarse, colonizando nuevos territorios.
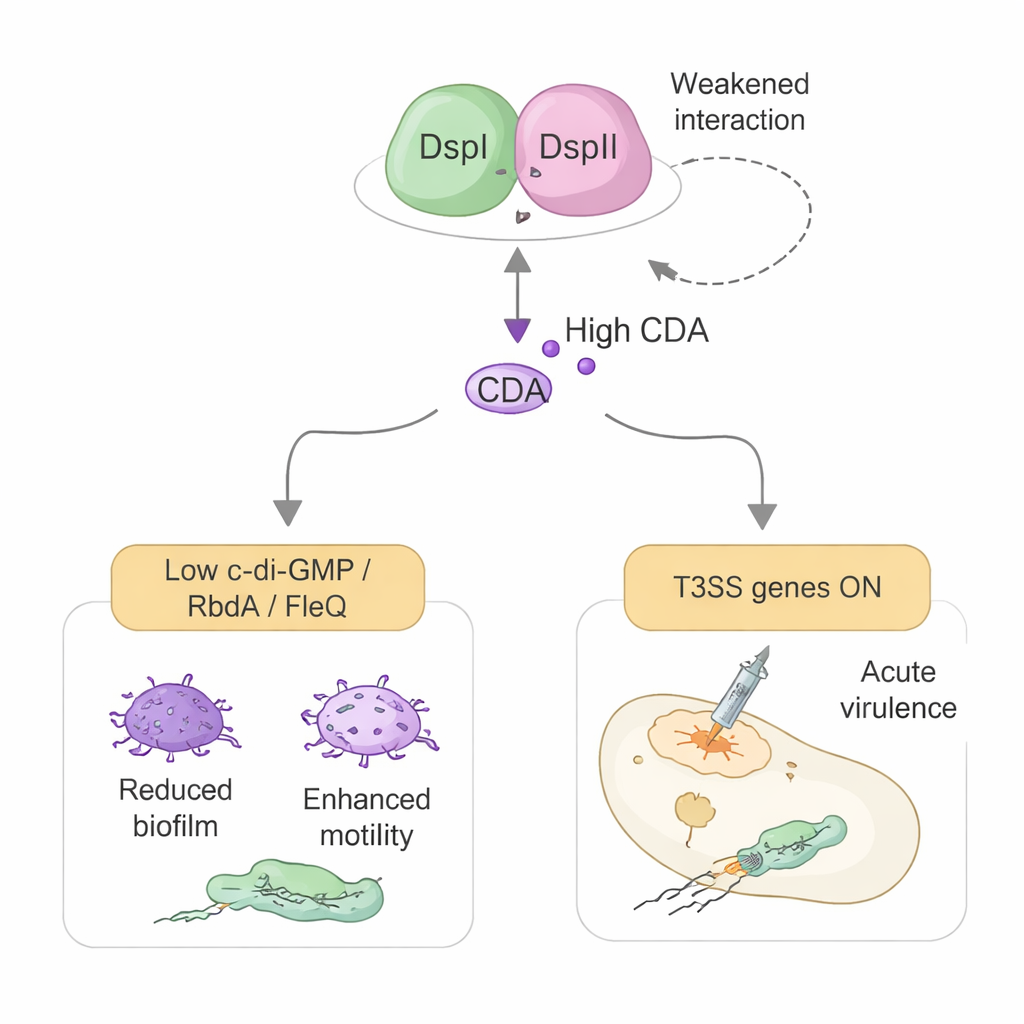
Reconfigurando el sistema de armas bacteriano
El estudio también revela un segundo papel inesperado de DspI y DspII que va más allá de la química. Este par proteico ayuda a activar el sistema de secreción tipo III (T3SS) de la bacteria, un aparato similar a una jeringa usado para inyectar toxinas directamente en las células del hospedador. En lugar de actuar a través de la CDA, este efecto ocurre mediante el control directo de interruptores genéticos. DspI y DspII reducen la producción de dos pequeños ARN reguladores, RsmY y RsmZ, que normalmente inhiben la síntesis de proteínas del T3SS. Lo hacen uniéndose a la región de control del ADN de uno de estos ARN e interactuando físicamente con una proteína reguladora maestra llamada GacA. Cuando RsmY y RsmZ están controlados, un activador en la vía descendente llamado RsmA queda liberado, y los genes del T3SS y su controlador maestro ExsA se activan, aumentando la citotoxicidad en cultivo celular y la letalidad en un modelo de infección en insectos.
Un sistema que se autorregula con dianas farmacológicas
De manera ingeniosa, la fuerza de la asociación DspI–DspII y su control sobre la virulencia se ajustan a su vez por los niveles de CDA. A bajas concentraciones—como las que se esperan en células que acaban de abandonar una biopelícula—la CDA refuerza la interacción entre las dos proteínas y promueve más producción de señal y activación del T3SS. A concentraciones altas dentro de biopelículas densas, la CDA debilita su interacción y reduce su unión al ADN, limitando la síntesis adicional de señal y la producción de armas costosas en las células que se quedan. Este doble papel convierte al complejo DspI–DspII en un centro clave que vincula el tamaño de la población, la escape de la biopelícula y la virulencia aguda. Dado que interrumpir el complejo puede bloquear tanto la producción de la señal como la activación del sistema de toxinas, ofrece una diana atractiva para futuros fármacos que podrían mantener a Pseudomonas en un estado crónico menos dañino y prevenir brotes peligrosos.
Cita: Huang, J., Zhou, T., Zhou, X. et al. Dual-functional quorum sensing signal synthases DspII and DspI coordinate virulence switch in Pseudomonas aeruginosa. Nat Commun 17, 1926 (2026). https://doi.org/10.1038/s41467-026-68622-x
Palabras clave: Pseudomonas aeruginosa, dispersión de biopelículas, detección de quórum, cambio de virulencia, cis-2-decenoico