Clear Sky Science · es
Firma dinámica del compromiso actividad‑estabilidad en la evolución de la lactamasa
Por qué importa para la resistencia a los antibióticos
La resistencia a los antibióticos a menudo parece una caja negra: las bacterias "de algún modo" cambian y los fármacos dejan de funcionar. Este estudio abre esa caja para una de las enzimas de resistencia más conocidas del mundo, la β‑lactamasa TEM‑1, que ayuda a las bacterias a destruir antibióticos tipo penicilina. Al observar cómo cambian la forma y los movimientos de esta enzima mientras evoluciona para atacar fármacos más recientes, los autores revelan por qué las mutaciones que aumentan la actividad suelen debilitar la estabilidad, y cómo la evolución encuentra maneras ingeniosas de equilibrar ambos aspectos.
De romper penicilina a atacar fármacos más amplios
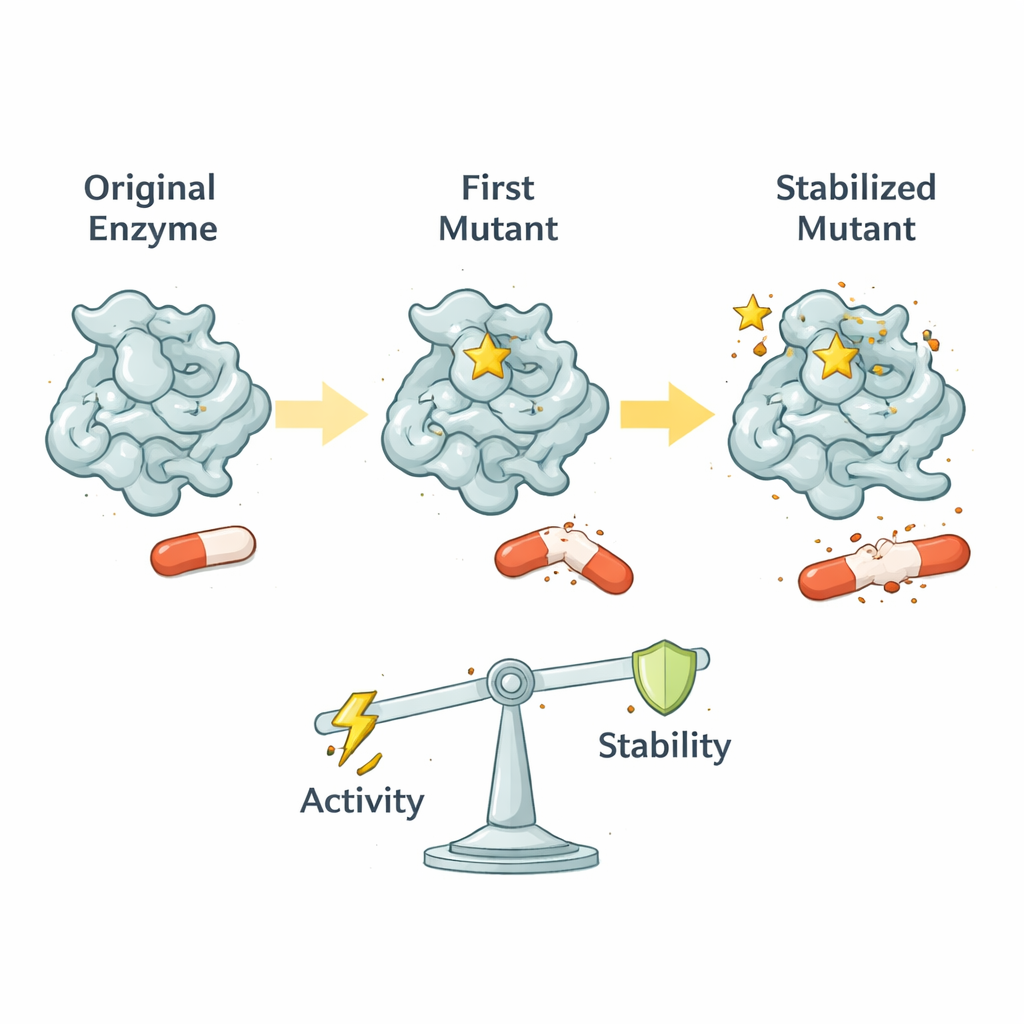
TEM‑1 originalmente sobresale en descomponer las penicilinas antiguas pero es pobre para enfrentarse a fármacos más modernos y voluminosos como la cefotaxima. En muchas cepas clínicas aparece una mutación clave única denominada G238S cerca del sitio activo de la enzima, el bolsillo donde se cortan los antibióticos. Esta mutación mejora drásticamente la capacidad de la enzima para destruir la cefotaxima, dañando solo de forma modesta su función original contra penicilinas. Los autores muestran que G238S no simplemente ensancha el bolsillo; reorganiza cómo se mueven varios bucles y hélices circundantes, creando una nueva conformación funcional que acomoda mejor a los fármacos voluminosos.
El movimiento proteico como un mando de ajuste evolutivo
Usando avanzadas técnicas de resonancia magnética nuclear (RMN), los investigadores midieron cómo se mueven distintas partes de TEM‑1 en escalas de tiempo que van desde billonésimas hasta milésimas de segundo. La TEM‑1 de tipo salvaje es bastante rígida, lo que le ayuda a procesar eficientemente sus sustratos originales. G238S deja intacta la mayor parte de esa rigidez rápida pero introduce movimientos más lentos y cuidadosamente ajustados en muchos muros del sitio activo. Estos movimientos son lo bastante rápidos para seguir el ritmo de la química enzimática y, al mismo tiempo, no tan violentos como para perturbar residuos catalíticos críticos. El resultado es una "ventana optimizada" de flexibilidad: el movimiento justo para abrir el bolsillo a la cefotaxima, manteniendo a la vez la maquinaria química central correctamente alineada.
Equilibrar dos formas en lugar de elegir una
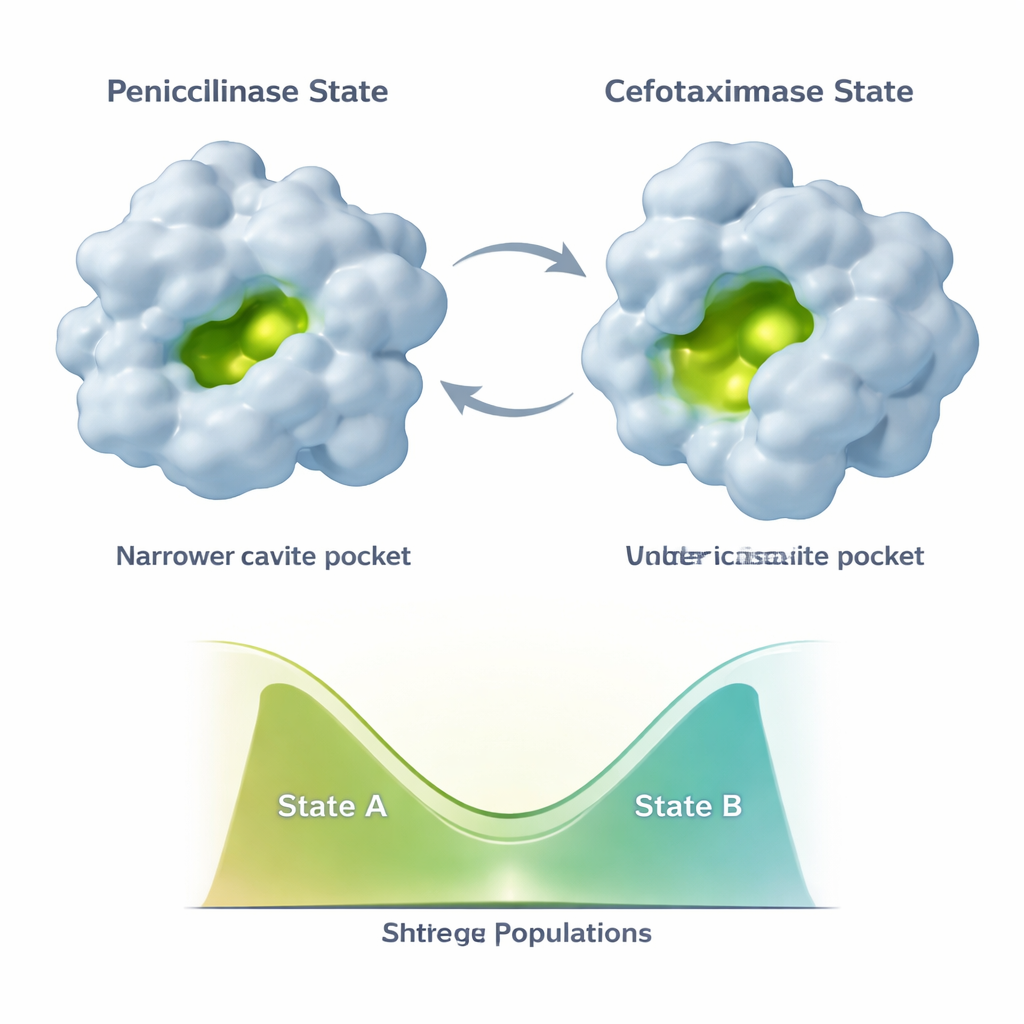
La evolución no congela a TEM‑1 en una única nueva forma. En lugar de ello, la enzima muestrea al menos dos conformaciones principales: un estado "penicillinasa" que se parece a la estructura original y un estado más abierto, "cefotaximasa", mejor adaptado para fármacos más nuevos. Mutaciones adicionales que aparecen más tarde, como E104K y A42G, hacen algo sutil. En vez de simplemente estabilizar más la nueva forma favorable para la cefotaxima, reequilibran la mezcla de los dos estados. Los datos de RMN muestran que distintas partes del sitio activo y del armazón de soporte pueden cambiar sus poblaciones de forma independiente a lo largo de este continuo de dos estados. Esto da lugar a un conjunto combinatorio de variantes enzimáticas, cada una con una mezcla distinta de conformaciones parecidas a penicilina y a cefotaxima, y por tanto con perfiles catalíticos diferentes.
Puntos débiles ocultos y reparaciones a distancia
Las mutaciones que mejoran la actividad con frecuencia conllevan un coste oculto: hacen la proteína menos estable. En lugar de fijarse solo en el desdoblamiento completo, el equipo cartografió la estabilidad local a nivel de segmentos cortos usando intercambio hidrógeno–deuterio con espectrometría de masas. Se encontró que G238S desestabiliza no solo bucles cercanos sino también hélices y regiones de lámina distantes que forman una columna vertebral estructural. Algunas de estas regiones se solapan con un bolsillo alostérico “críptico”, una apertura poco visitada en el núcleo de la proteína que puede unirse a pequeñas moléculas y atenuar la actividad. G238S facilita la apertura de este bolsillo, construyendo efectivamente una característica leve de autoinhibición en la enzima. Mutaciones posteriores, especialmente A42G, refuerzan esta red de soporte debilitada a distancia, mejorando la estabilidad local alrededor de tres hélices interaccionantes sin eliminar la dinámica beneficiosa del sitio activo. En otras palabras, la evolución parchea puntos débiles estructurales distantes en lugar de deshacer la innovación original.
Lo que el estudio revela sobre la estrategia de la evolución
Para un lector no experto, el mensaje central es que proteínas como TEM‑1 no desarrollan resistencia con un simple interruptor de encendido/apagado. Cada mutación remodela ligeramente cómo la enzima respira, se flexiona y reparte su tiempo entre distintas posturas funcionales. G238S abre la puerta a un nuevo trabajo—romper antibióticos más recientes—pero también crea fragilidades locales y un estado parcialmente autoinhibidor. Las mutaciones secundarias actúan como refuerzos cuidadosos, estabilizando el armazón y afinando el equilibrio entre las conformaciones antigua y nueva para que la enzima pueda seguir siendo a la vez activa y duradera. Esta visión dinámica de la evolución, donde los movimientos y las debilidades locales importan tanto como la estructura estática, puede ayudar a guiar el diseño de futuros antibióticos y fármacos dirigidos a enzimas que resulten más difíciles de superar para las bacterias.
Cita: Arcia, E., Keramisanou, D., Jacobs, L.M.C. et al. Dynamic signature of activity-stability tradeoff in lactamase evolution. Nat Commun 17, 1884 (2026). https://doi.org/10.1038/s41467-026-68620-z
Palabras clave: resistencia a antibióticos, beta‑lactamasa, evolución de proteínas, dinámica enzimática, estabilidad de proteínas