Clear Sky Science · es
Un estimulador vagal triboeléctrico totalmente degradable para atenuar la remodelación cardíaca y la insuficiencia cardiaca en diferentes estadios
Por qué importa un dispositivo cardíaco que se disuelva
La insuficiencia cardiaca es una afección frecuente y mortal que afecta a decenas de millones de personas y suele derivar en años de fatiga, falta de aire y hospitalizaciones repetidas. Los médicos saben que estimular suavemente un nervio importante, el nervio vago, puede ayudar al corazón en fallo, pero los implantes actuales son voluminosos, funcionan con baterías y deben extraerse o reemplazarse mediante cirugía. Este estudio presenta un estimulador pequeño y flexible que se alimenta con el movimiento del propio cuerpo y que, tras el tratamiento, se disuelve de forma segura dentro del organismo, abriendo la puerta a terapias a corto plazo y personalizadas sin cirugías adicionales.
Una forma más suave de aprovechar la red del cuerpo
El nervio vago se extiende desde el cerebro hasta muchos órganos y ayuda a equilibrar los sistemas de estrés y relajación del organismo. En la insuficiencia cardiaca, este equilibrio se desplaza hacia una activación constante de “lucha o huida”, lo que empeora el daño al corazón. La estimulación vagal de bajo nivel (LL-VNS) transmite señales demasiado débiles para ralentizar el corazón o alterar su ritmo, pero lo bastante intensas para restaurar parte de ese equilibrio y reducir la inflamación nociva. Ensayos clínicos previos con estimuladores estándar alimentados por batería mostraron que la LL-VNS podía mejorar los síntomas y la calidad de vida; sin embargo, el propio hardware planteaba problemas: vida útil limitada de la batería, necesidad de operaciones de reemplazo y la presencia prolongada de material extraño en el cuerpo.
Un dispositivo autoalimentado que desaparece
Para resolver estos problemas, los investigadores construyeron un nanogenerador triboeléctrico totalmente biodegradable, o BTENG, que convierte el suave movimiento mecánico en electricidad. El dispositivo está compuesto por capas de polímeros biodegradables comunes y finas películas metálicas, selladas dentro de un recubrimiento protector. Cuando las capas se unen y separan —impulsadas por pequeños movimientos— se generan cargas eléctricas que se dirigen a una funda que envuelve el nervio vago. En pruebas de laboratorio, el BTENG produjo de forma fiable voltajes de aproximadamente 9 voltios y corrientes en torno a 4 microamperios, suficientes para alcanzar el nivel de estimulación seguro establecido en ratones. La salida se mantuvo estable durante miles de ciclos y al menos cuatro semanas en un entorno lleno de fluido similar al corporal. Tras el tratamiento, un pulso de ultrasonido médico puede fracturar el recubrimiento exterior y acelerar la degradación del dispositivo, transformándolo en fragmentos inofensivos que el organismo elimina gradualmente. 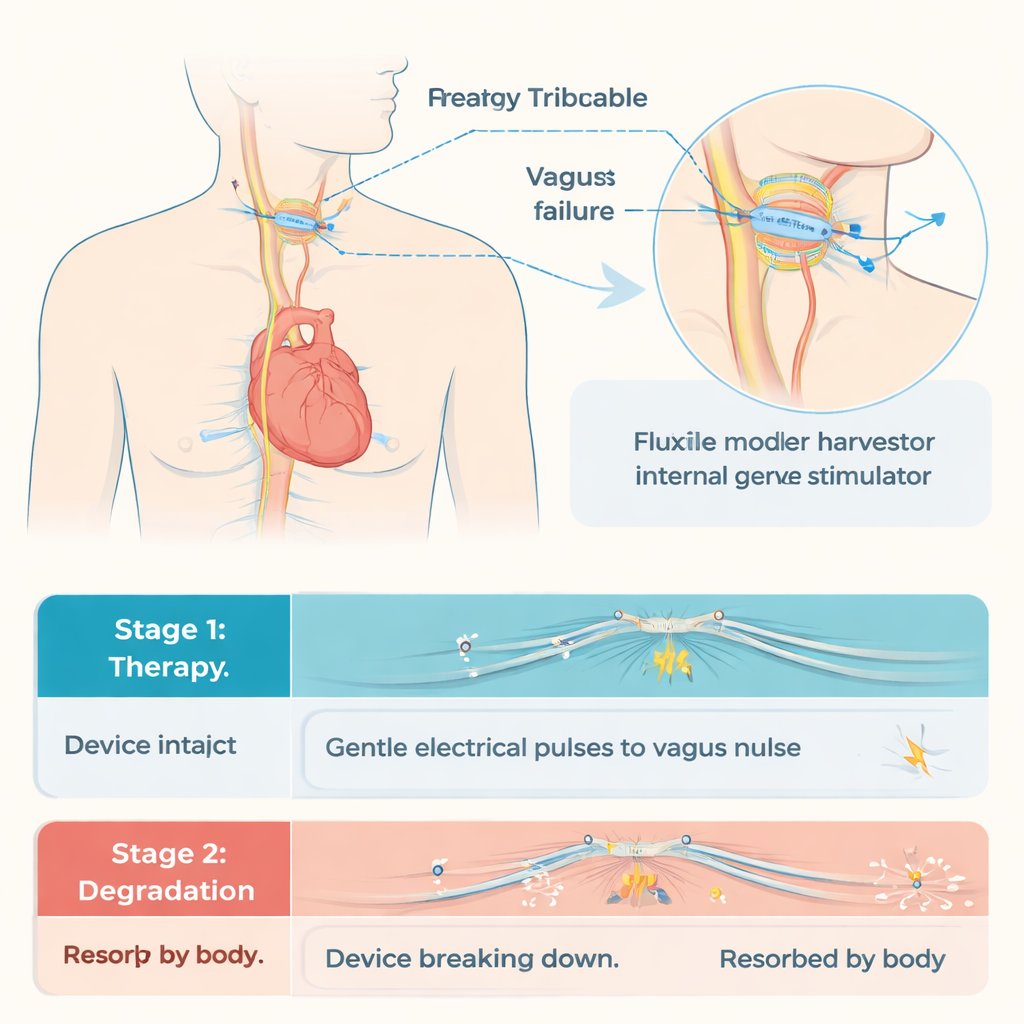
Protegiendo y reparando el corazón en fallo
El equipo probó el sistema en un modelo de ratón de insuficiencia cardiaca causada por una sobrecarga de presión prolongada en el corazón, similar a lo que ocurre en hipertensión arterial severa o válvulas cardíacas estrechas. Iniciaron la LL-VNS en tres estadios diferentes: muy temprano (antes de daños mayores), tras un engrosamiento inicial del músculo cardíaco y después de que se hubiera desarrollado la insuficiencia cardiaca completa. En las tres situaciones, los ratones que recibieron estimulación diaria de bajo nivel mediante el BTENG mostraron mejor función de bombeo, menor dilatación cardíaca y menos tejido cicatricial que los animales no tratados o que recibieron cirugía e implantes sin estimulación. Medidas como la fracción de eyección, la congestión pulmonar y la relación peso del corazón/tamaño corporal mejoraron, lo que indica que la terapia no solo puede ralentizar el daño sino también revertirlo parcialmente, incluso cuando se inicia en estadios avanzados.
Cómo las señales nerviosas remodelan la biología del corazón
Para entender cómo una pequeña señal eléctrica podía tener efectos tan amplios, los investigadores examinaron el tejido cardíaco a nivel genético. Hallaron que la LL-VNS modificaba la actividad de cientos de genes implicados en el andamiaje de soporte del corazón (la matriz extracelular), la estructura muscular, la muerte celular, el crecimiento y la inflamación. Estos cambios concordaban con la disminución observada de la cicatrización tisular y la mejora de la salud muscular. Dado que el nervio vago comunica mediante el mensajero químico acetilcolina, el equipo probó si esta molécula era esencial bloqueando sus receptores principales con el fármaco atropina. Cuando se administró atropina, los beneficios de la LL-VNS desaparecieron: la función cardíaca empeoró, la cicatrización aumentó y los genes relacionados con la enfermedad permanecieron elevados. Esto demostró que la liberación de acetilcolina inducida por las señales del nervio vago es un factor clave en los efectos protectores sobre el corazón. 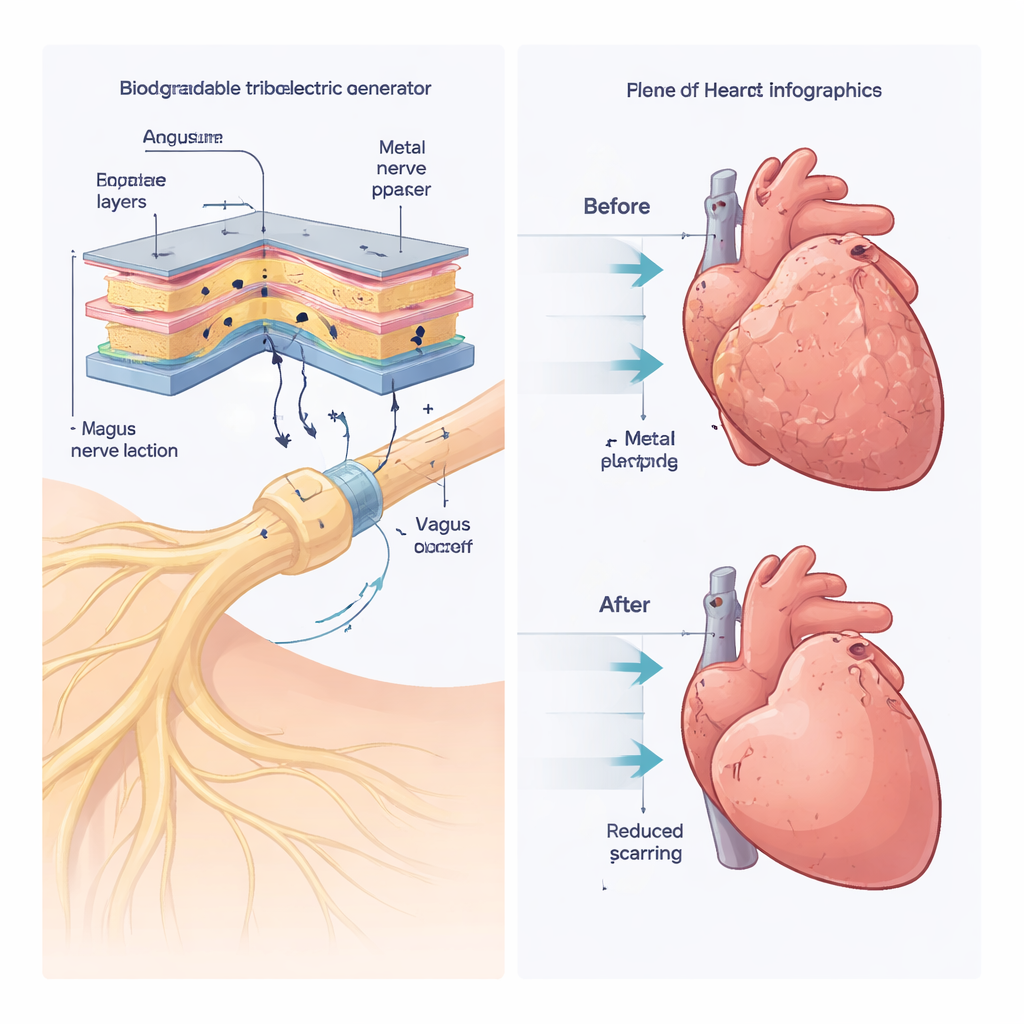
De implantes que se disuelven a una atención cardíaca personalizada
En conjunto, los hallazgos demuestran que un estimulador pequeño, autoalimentado y totalmente degradable puede entregar de forma segura señales nerviosas que previenen o revierten la remodelación cardíaca perjudicial en ratones. Para los pacientes, una versión futura de esta tecnología podría implantarse solo el tiempo necesario, alimentarse con sus propios movimientos y luego eliminarse del organismo mediante una simple sesión de ultrasonido —sin cambios de batería ni cirugía de extracción. Al combinar estimulación nerviosa precisa con materiales inteligentes que desaparecen a demanda, este enfoque apunta a una nueva clase de tratamientos temporales y personalizados para la insuficiencia cardiaca que podrían reducir complicaciones, bajar costes y mejorar la calidad de vida.
Cita: Guo, Z., Chao, SY., Kong, CY. et al. A fully degradable triboelectric vagus nerve stimulator for attenuating cardiac remodeling and heart failure at different stages. Nat Commun 17, 1893 (2026). https://doi.org/10.1038/s41467-026-68619-6
Palabras clave: insuficiencia cardiaca, estimulación del nervio vago, implante biodegradable, generador triboeléctrico, remodelación cardíaca