Clear Sky Science · es
Un atlas espacialmente resuelto del cáncer gástrico caracteriza una región agregada de linfocitos
Por qué importa el vecindario alrededor de un tumor
El cáncer no es solo un cúmulo de células rebeldes; vive en un vecindario concurrido de células inmunitarias y estructurales que pueden ayudar a combatir el tumor o permitir que crezca sin control. Este estudio cartografía ese vecindario en el cáncer gástrico con un detalle sin precedentes, mostrando cómo pequeños puntos calientes y fríos inmunitarios dentro del mismo tumor pueden influir en si un paciente responde a las inmunoterapias modernas.
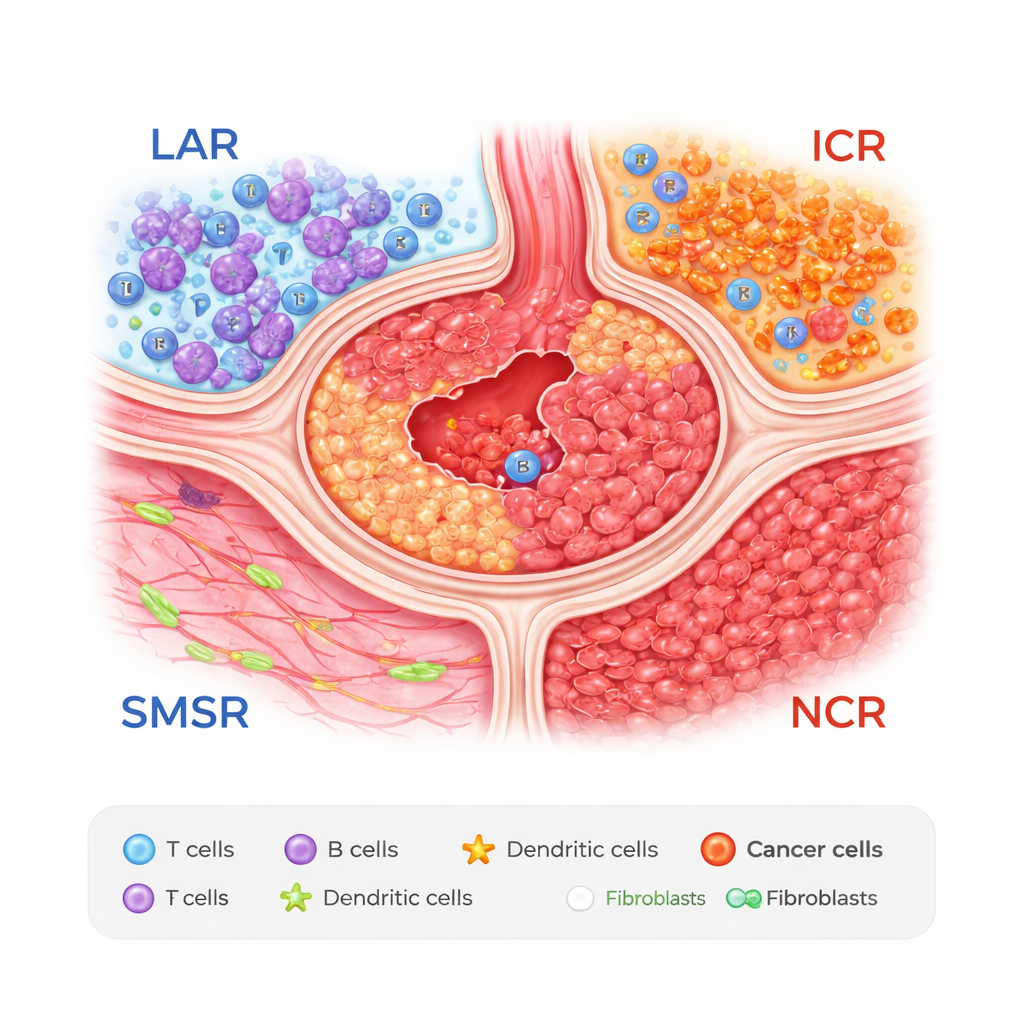
Cuatro zonas dentro de un tumor de estómago
Los investigadores combinaron dos herramientas potentes: secuenciación de ARN unicelular, que lee la actividad génica en células individuales, y transcriptómica espacial, que registra dónde se ubican esas células en cortes de tejido. Estudiando muestras de 27 pacientes, descubrieron que los tumores gástricos pueden dividirse en cuatro zonas recurrentes. Una es una región agregada de linfocitos, o LAR, rica en cúmulos de células T y B que recuerdan a pequeños ganglios linfáticos. Otra es una región de músculo liso y estroma (SMSR), dominada por músculo y tejido conectivo. Las dos zonas restantes son áreas densas en cáncer: una región tumoral inmunogénica (ICR), donde las células tumorales se mezclan con algunos tipos celulares protectores del estómago, y una región tumoral con baja inmunogenicidad (NCR), repleta de células malignas y con relativamente pocas células inmunitarias defensivas.
Puntos calientes inmunitarios relacionados con mejores resultados
El equipo encontró que la zona LAR está enriquecida en genes que normalmente se observan en ganglios linfáticos, donde las células inmunitarias se entrenan y activan. Estos incluyen señales que ayudan a reclutar linfocitos y a organizarlos en estructuras llamadas estructuras linfoides terciarias. Al analizar grandes conjuntos de datos públicos de cáncer, los tumores con mayor expresión de genes vinculados a LAR tendían a asociarse con una mejor supervivencia de los pacientes y con una probabilidad algo mayor de responder a terapias de puntos de control inmunitario que liberan los frenos sobre las células T. En contraste, las firmas génicas de regiones ricas en músculo o fuertemente cancerosas se asociaban generalmente con peores resultados en varios tipos de cáncer.
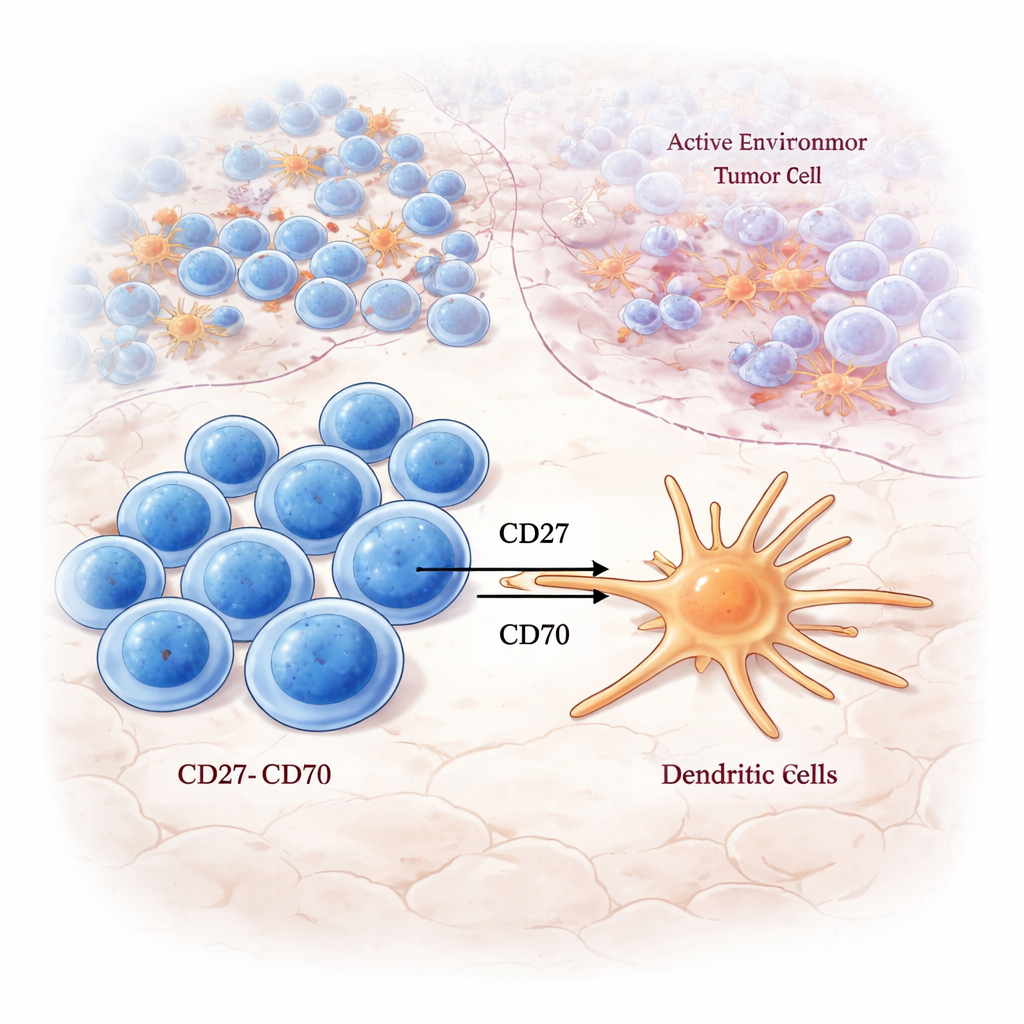
Dónde las células T naïvas aprenden a combatir
Al acercarse a la LAR, los autores observaron una fuerte actividad en vías de señalización centrales para despertar a las células T: señalización del receptor de células T, vías de costimulación y procesamiento de antígeno. Las células T CD8 naïvas—células que aún no se han comprometido por completo a atacar un objetivo específico—estaban especialmente vinculadas a estas señales de activación dentro de la LAR, pero no en otros lugares. Mediante tinción multicolor, detectaron células T CD8 en la LAR que mostraban marcadores tanto de renovación como de proliferación, lo que sugiere que esta región actúa como una zona de entrenamiento y expansión in situ donde se preparan células frescas para combatir el tumor.
Dos sabores de vecindario inmunitario
No todas las LAR eran iguales. Cuando los investigadores agruparon a los pacientes según la composición celular de sus LAR, descubrieron dos patrones. En los tumores del “Grupo A”, las LAR se parecían mucho a ganglios linfáticos clásicos, ricas en células B especializadas y células dendríticas, y las regiones tumorales adyacentes a estas LAR estaban llenas de linfocitos activados y preparados para la batalla. En el “Grupo B”, las LAR estaban menos desarrolladas y el tejido tumoral contiguo contenía más células T en reposo, menos comprometidas. Un análisis computacional avanzado de las imágenes tisulares confirmó que las células inmunitarias activadas se agrupaban físicamente cerca de estas LAR más maduras, lo que sugiere que la arquitectura local puede orientar la intensidad con que el sistema inmunitario ataca el tumor.
Señales de puntos de control en el espacio
El estudio también rastreó dónde se expresan los “interruptores” inmunitarios conocidos como moléculas de punto de control. Pares estimuladores como CD27–CD70 se concentraron en la LAR, particularmente en los tumores del Grupo A, conectando células T CD8 exhaustas pero reactivas frente al tumor con células dendríticas que podrían potenciar aún más su actividad. En contraste, muchos pares de puntos de control inhibidores, como TIGIT–NECTIN2 y LAG3–LGALS3, se enriquecieron en la NCR, la zona más cargada de cáncer. Esto sugiere que incluso cuando la señalización del receptor de células T está presente, el paisaje de puntos de control circundante puede inclinar la inmunidad local hacia el ataque o la supresión, según la región del tumor.
Qué significa esto para los pacientes
Para un público no especializado, el mensaje clave es que dónde se ubican las células inmunitarias y las señales dentro de un tumor puede importar tanto como cuántas hay. Este trabajo muestra que los cánceres gástricos contienen vecindarios inmunitarios distintos, y que regiones robustas, similares a ganglios linfáticos, cerca del tumor se asocian con células T más activas y mejor posicionadas y con resultados más favorables. Al aprender a reconocer y posiblemente reforzar estas regiones agregadas de linfocitos, las terapias futuras podrían adaptarse mejor: escoger fármacos, combinaciones o incluso enfoques de administración dirigidos que exploten los propios bastiones inmunitarios internos del tumor.
Cita: Gao, S., Qin, S., Wang, D. et al. A spatially resolved atlas of gastric cancer characterises a lymphocyte-aggregated region. Nat Commun 17, 2059 (2026). https://doi.org/10.1038/s41467-026-68612-z
Palabras clave: cáncer gástrico, microambiente tumoral, estructuras linfoides terciarias, transcriptómica espacial, inmunoterapia contra el cáncer