Clear Sky Science · es
Envejecimiento divergente de las glándulas mamarias nullíparas y páridas revela células epiteliales híbridas IL33+
Cómo el embarazo puede remodelar el riesgo vitalicio de cáncer de mama
¿Por qué tener un bebé a una edad temprana reduce el riesgo vitalicio de cáncer de mama en una mujer, mientras que el simple hecho de envejecer lo aumenta? Este estudio usa ratones para examinar el “ecosistema” celular de la mama a lo largo del tiempo, comparando animales que nunca quedaron embarazadas con los que sí lo hicieron. Al seguir cómo cambian células individuales con la edad y la reproducción, los investigadores descubren un tipo celular raro y cambiante de forma que podría ayudar a explicar la protección a largo plazo que confiere el embarazo frente al cáncer de mama.
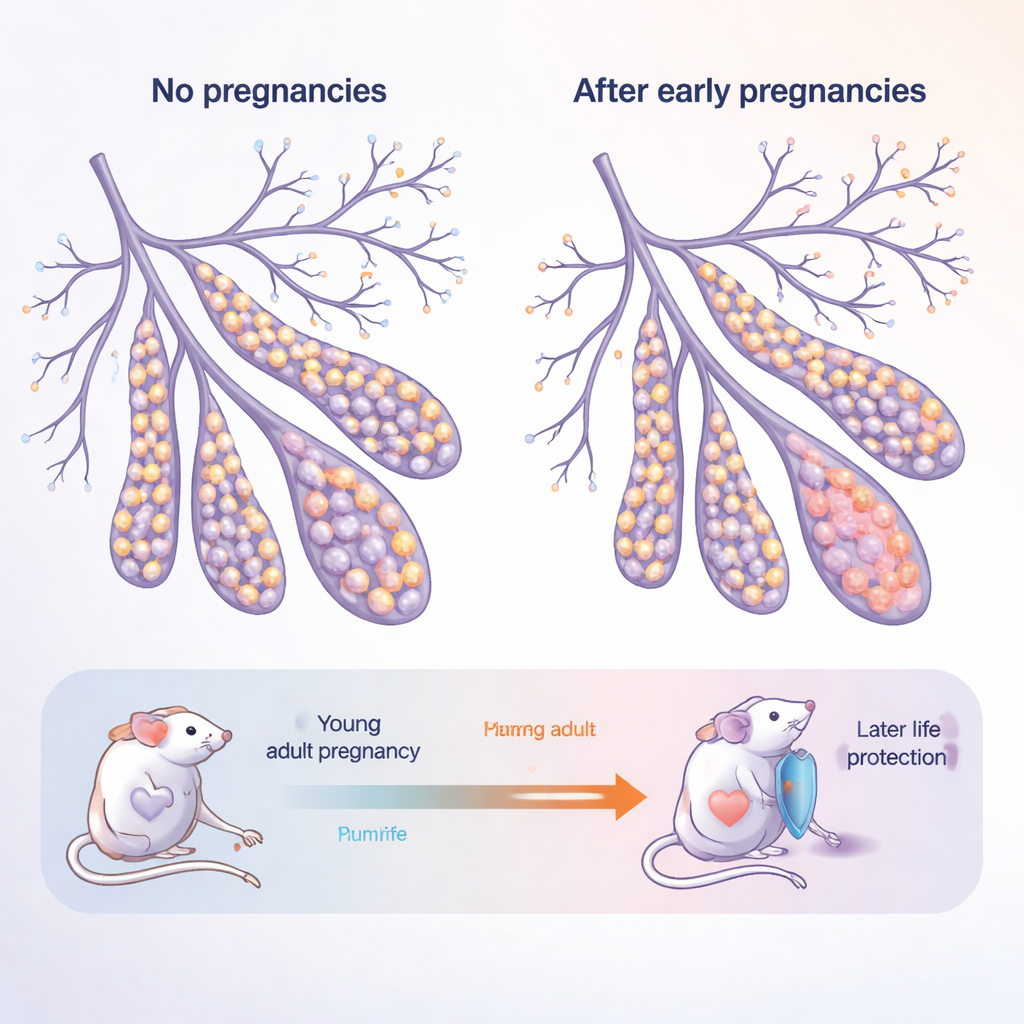
La mama como un tejido vivo y cambiante
La glándula mamaria no es un órgano estático: crece y se remodela de forma marcada en la pubertad, durante el embarazo y de nuevo cuando termina la producción de leche. Está formada por dos capas principales de células epiteliales que recubren los conductos: las células “luminales” internas que contactan la leche y las hormonas, y las células “basales” externas que aportan estructura y albergan células con rasgos de progenitoras. Los autores estudiaron ratones jóvenes adultos y ratones mayores, “postmenopáusicos”, cada grupo compuesto por animales nunca embarazados (nullíparos) o que habían pasado por múltiples embarazos (páridos). Este diseño imita a una mujer que da a luz en sus veinte años y luego envejece hasta sus cincuenta o más.
Cómo el envejecimiento y el embarazo tiran del tejido en direcciones diferentes
A medida que los ratones envejecían sin haber estado nunca embarazados, sus glándulas mamarias se desplazaron hacia una mayor proporción de células basales y menos células luminales. Estas glándulas de animales mayores y nunca embarazados también produjeron muchos más organoides—estructuras 3D en miniatura cultivadas desde células individuales—lo que indica que sus células estaban inusualmente predispuestas a proliferar. En contraste, los ratones que habían pasado por embarazos mostraron un equilibrio “normalizado”: el aumento relacionado con la edad de células basales se atenuó y sus células formaron menos organoides. Esto sugiere que el embarazo deja una huella duradera que tanto altera cómo las células eligen su destino como contiene su potencial regenerativo y, potencialmente, la propensión a cancerizarse.
El descubrimiento de células híbridas y cambiantes
Para profundizar, el equipo usó secuenciación de ARN unicelular para leer qué genes estaban activos en miles de células mamarias individuales. Entre las esperadas células luminales, basales, inmunes y estromales, encontraron un grupo raro que no encajaba claramente en ninguna de las dos capas principales. Estas células expresaban marcadores de ambas líneas, luminal y basal, ganándose el nombre de células epiteliales “híbridas”. De manera llamativa, estos híbridos se acumularon con la edad en ratones nunca embarazados, pero eran mucho menos comunes en ratones de la misma edad que habían sido embarazadas. Los híbridos expresaban fuertemente un gen llamado Il33, que codifica la molécula de señalización IL-33, junto con marcadores vinculados a etapas tempranas del desarrollo y alta plasticidad—la capacidad de cambiar de identidad o comportamiento.
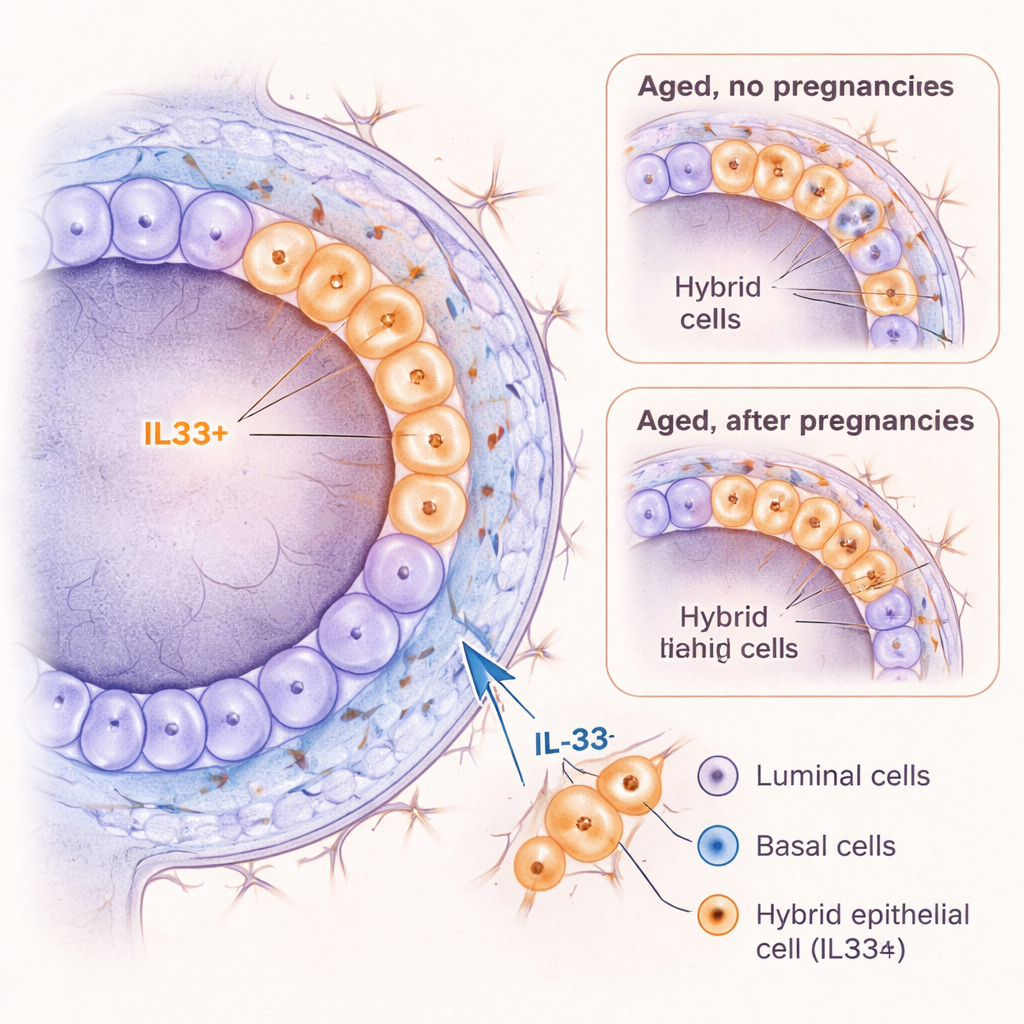
IL-33 como impulsor de estados celulares riesgosos
Como IL-33 se ha relacionado con inflamación y cáncer en otros órganos, los investigadores preguntaron si puede empujar activamente a las células mamarias hacia un estado parecido al híbrido. Cuando trataron células mamarias jóvenes de ratón con IL-33 en cultivo 3D, las células de la capa basal formaron más organoides, mantuvieron una identidad más primitiva y produjeron más células con el marcador híbrido KRT6A. En ratones jóvenes vivos, inyecciones a corto plazo de IL-33 provocaron el ensanchamiento de los conductos y desataron una oleada de división celular, junto con un aumento temporal de células híbridas KRT6A-positivas y un desplazamiento hacia más células de tipo basal. Importante, cuando las células portaban una mutación relacionada con el cáncer (pérdida del gen supresor de tumores Trp53), IL-33 potenció aún más su crecimiento. En conjunto, estos hallazgos sugieren que IL-33 ayuda a crear un estado celular plástico y proliferativo que podría ser especialmente vulnerable a convertirse en canceroso.
Pistas procedentes del tejido mamario humano
Para comprobar si existen células similares en personas, los autores reanalizaron varios conjuntos de datos unicelulares grandes de tejido mamario humano normal. Identificaron una pequeña población de células epiteliales humanas que, como los híbridos de ratón, exhibía rasgos tanto luminales como basales y expresaba IL33 y genes relacionados. Las células IL33-positivas se volvieron más comunes con la edad en varios conjuntos de datos. En células mamarias humanas primarias cultivadas en el laboratorio, el tratamiento con IL-33 aumentó la formación de organoides, desplazó las células hacia un perfil de tipo basal y enriqueció para células CD44-positivas—un marcador a menudo asociado con células inmaduras con rasgos de progenitoras en el cáncer de mama. Aunque las muestras humanas disponibles no permitieron probar claramente cómo altera esta población un embarazo temprano, los paralelismos con los ratones son llamativos.
Qué implica esto para entender la protección frente al cáncer de mama
Para un lector no especializado, el mensaje central es que el embarazo parece reconfigurar la forma en que el tejido mamario envejece. En ratones, un embarazo temprano evita la acumulación de células híbridas ricas en IL-33 que difuminan la frontera entre las principales capas celulares de la mama y se comportan con alta flexibilidad y predisposición al crecimiento. La propia IL-33 puede empujar a las células hacia este estado arriesgado y cambiante, especialmente cuando están presentes mutaciones vinculadas al cáncer. Al reducir el número o la persistencia de estas células híbridas, el embarazo podría disminuir las probabilidades de que el tejido mamario envejecido contenga el “tipo equivocado” de célula en el “momento equivocado”, es decir, una célula predispuesta a pasar a cáncer. Esta visión mecanística podría finalmente orientar estrategias para imitar los efectos protectores del embarazo temprano sin necesidad de embarazo.
Cita: Olander, A., Medina, P., Haro Acosta, V. et al. Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells. Nat Commun 17, 1898 (2026). https://doi.org/10.1038/s41467-026-68611-0
Palabras clave: envejecimiento de la mama, embarazo y cáncer de mama, células madre mamarias, señalización IL-33, células epiteliales híbridas