Clear Sky Science · es
Ampliación del alcance de la carga útil en conjugados anticuerpo-fármaco mediante la entrega de fármacos con grupos hidroxilo a través de fosforamidatos auto-inmolativos
Misiles más inteligentes contra el cáncer
Los fármacos contra el cáncer pueden ser increíblemente potentes, pero con frecuencia actúan como bombardeos indiscriminados: dañan los tejidos sanos casi tanto como a los tumores. Los conjugados anticuerpo–fármaco (ADC) se inventaron para resolver este problema al unir un fármaco potente a un anticuerpo que se dirige a las células cancerosas, convirtiendo el tratamiento en un misil guiado. Este artículo explica un nuevo “enchufe” químico entre anticuerpo y fármaco que hace que estos misiles sean tanto más precisos como más flexibles, abriendo la puerta a muchos tipos de medicamentos contra el cáncer que los ADC actuales no pueden transportar.
Por qué los fármacos dirigidos de hoy siguen siendo limitados
Los ADC se construyen a partir de tres partes: un anticuerpo que reconoce un marcador en las células cancerosas, un fármaco tóxico (la “carga útil”) y un enlazador químico que los une. La mayoría de los ADC aprobados dependen de solo unos pocos tipos de cargas útiles que dañan el ADN o bloquean la división celular de formas similares. Una razón principal es el enlazador: debe mantener el fármaco firmemente sujeto mientras el ADC circula en el torrente sanguíneo y luego liberarlo de forma limpia una vez dentro de la célula tumoral. Los enlazadores existentes funcionan bien solo con ciertos grupos químicos en los fármacos, especialmente aminas, y con frecuencia tienen dificultades con los numerosos medicamentos que contienen grupos alcohol (–OH). Esto deja en el estante una gran cantidad de agentes anticancerígenos prometedores porque no pueden ser administrados de forma segura o eficiente por los diseños actuales de ADC.
Tomando prestado un truco de las pastillas antivirales
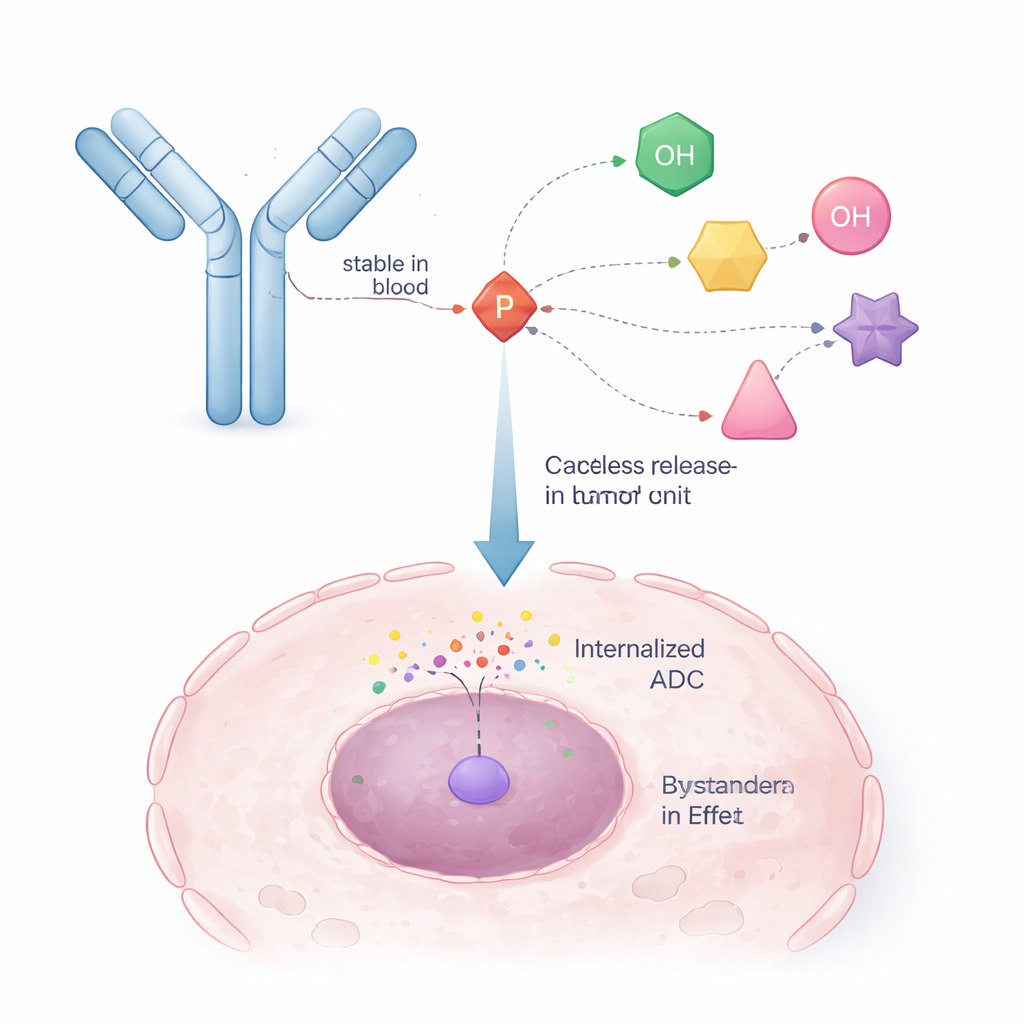
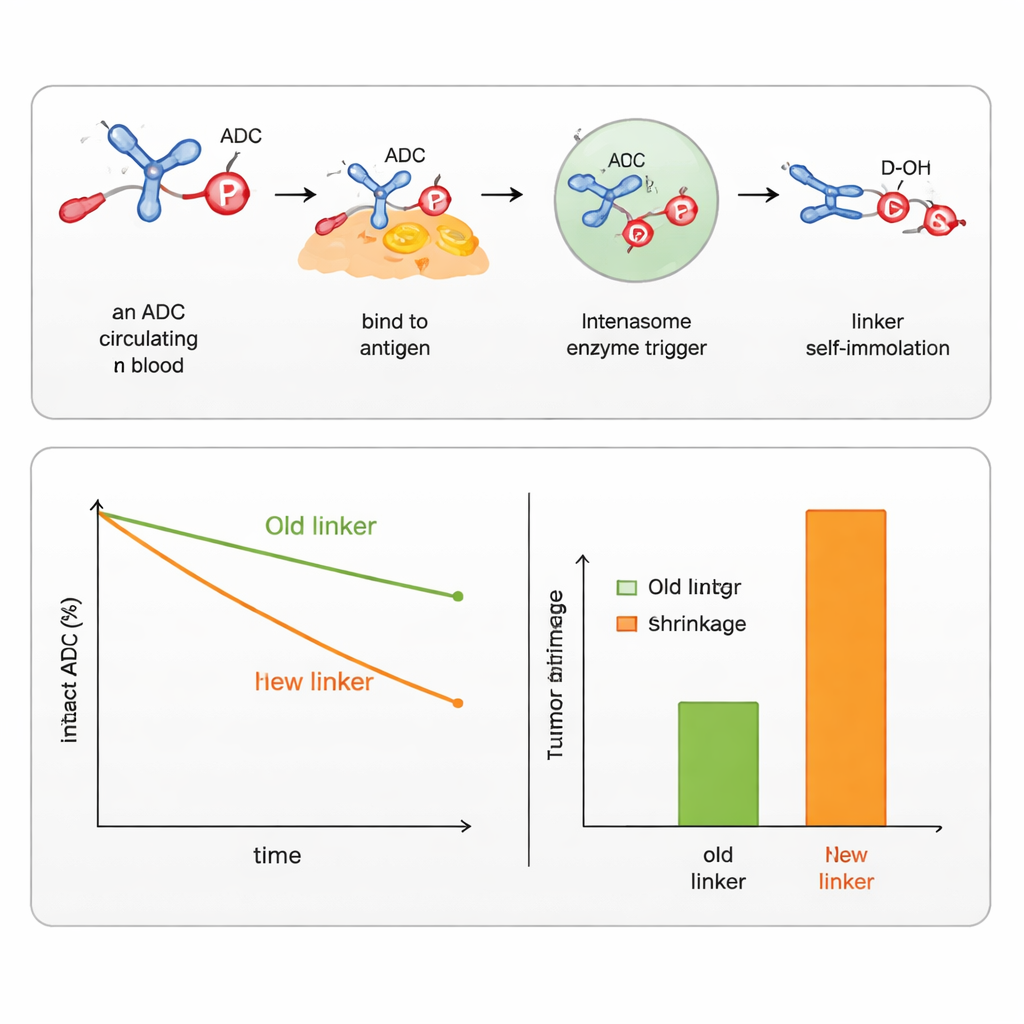
Los investigadores recurrieron a una estrategia ya probada en fármacos antivirales llamada ProTides. En esos medicamentos, una unidad química a base de fósforo enmascara temporalmente el grupo fosfato cargado de un fármaco para que pueda entrar en las células, y luego se descompone en su interior para liberar la forma activa. Los autores reingeniaron este concepto de modo que un brazo del núcleo de fósforo se usa para unirse a un anticuerpo, mientras que los otros brazos sostienen el fármaco contra el cáncer. Esto crea un enlazador “auto-inmolativo”: una vez que un disparador interno (como una enzima en una célula tumoral) corta una pequeña parte de la estructura, la unidad de fósforo colapsa de forma controlada y libera la molécula de fármaco original con su grupo alcohol restaurado y sin modificar.
Construyendo un enchufe químico versátil
El equipo demostró que al ajustar los grupos alrededor del átomo de fósforo podían afinar cuán estable es el enlazador en sangre y qué tan rápido se descompone dentro de las células. Diseñaron versiones que responden a varios tipos de disparadores comunes en el interior de las células cancerosas, incluidas esterasa y proteasas (enzimas que cortan enlaces específicos), así como enzimas que reconocen grupos basados en azúcares o condiciones reductoras en compartimentos celulares. Usando estos diseños, consiguieron unir y liberar tanto alcoholes aromáticos (como la quimioterapia SN38) como alcoholes alifáticos (como DXd, la carga útil en un ADC aprobado para cáncer de mama). Comparados directamente con enlazadores comerciales existentes para SN38 y DXd, los nuevos enlazadores de fosforamidato mantuvieron los fármacos unidos durante más tiempo en suero, entregaron más fármaco a los tumores y produjeron una mayor reducción tumoral en ratones, mostrando al mismo tiempo menos impacto sobre las células sanas.
Desbloqueando muchas nuevas cargas útiles contra el cáncer
Para probar la amplitud de uso del enlazador, los investigadores ensamblaron ADC que transportaban diez fármacos diferentes que contienen al menos un grupo –OH pero actúan de maneras muy distintas dentro de las células cancerosas. Estos incluyeron inhibidores de la síntesis de ADN, del plegamiento de proteínas (HSP90), del metabolismo energético (NAMPT y DHODH) y de la traducción proteica, así como agentes bien conocidos como paclitaxel y gemcitabina. A pesar de la amplia variedad de estructuras, pudieron fabricar ADC uniformes con una alta carga de fármaco para todos ellos. En estudios celulares en varios tipos de cáncer, la mayoría de estos ADC mostraron potencias en el rango nanomolar o incluso subnanomolar y una selectividad clara por las células que expresaban el objetivo del anticuerpo, confirmando que el enlazador podía liberar de forma consistente el fármaco activo dentro de las células adecuadas.
La gemcitabina como ejemplo
La gemcitabina es una quimioterapia ampliamente utilizada, pero en su forma convencional se elimina del cuerpo tan rápidamente que los pacientes deben recibir dosis repetidas y elevadas, lo que limita cuánto se puede administrar de forma segura. Usando el enlazador de fosforamidato, los autores unieron la gemcitabina a un anticuerpo dirigido a HER2 en cualquiera de dos posiciones alcohol y demostraron que ambas versiones recuperaban toda su actividad una vez dentro de las células cancerosas. En modelos de ratón con tumores HER2-positivos, una única dosis del ADC con gemcitabina—conteniendo aproximadamente mil veces menos gemcitabina total que los regímenes típicos de fármaco libre—produjo un control tumoral fuerte y selectivo. El comportamiento del ADC en el torrente sanguíneo coincidió estrechamente con el del anticuerpo desnudo, y altas dosis fueron bien toleradas en ratas, lo que sugiere un amplio margen de seguridad.
Qué significa esto para el tratamiento futuro del cáncer
Para los no especialistas, el mensaje principal es que este trabajo aporta un nuevo conector químico altamente adaptable que permite a los anticuerpos transportar un conjunto mucho más amplio de fármacos contra el cáncer que antes, y hacerlo de manera más segura. Al asegurar que los fármacos permanezcan unidos durante la circulación y se liberen limpiamente solo después de que el ADC sea internalizado por una célula cancerosa, los enlazadores de fosforamidato mejoran la cantidad de fármaco que llega al tumor y reducen el daño colateral a los tejidos sanos. Igualmente importante, permiten reutilizar como terapias dirigidas fármacos potentes de pequeña molécula existentes—con formas y mecanismos muy distintos. Esto podría ampliar considerablemente el repertorio de ADC disponibles para los pacientes y ayudar a combatir tumores que se han vuelto resistentes al conjunto limitado de cargas útiles actuales.
Cita: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
Palabras clave: conjugados anticuerpo–fármaco, administración de fármacos contra el cáncer, enlaces auto-inmolativos, química de fosforamidatos, quimioterapia dirigida