Clear Sky Science · es
Electrólito de hidrogenación de CO2 sin membrana para la gestión de precipitación de sales en la reducción electroquímica ácida del CO2
Convertir la contaminación climática en combustible líquido útil
El dióxido de carbono (CO2) procedente de centrales eléctricas y fábricas es un motor principal del cambio climático, pero también es una materia prima barata y abundante. Los científicos trabajan a contrarreloj para convertir el CO2 en productos químicos útiles usando electricidad de fuentes renovables. Este estudio aborda un obstáculo práctico que ha limitado discretamente estas tecnologías: la acumulación de sales dentro de reactores de tipo industrial que, con el tiempo, ahogan el rendimiento. Los investigadores presentan un nuevo diseño de reactor sin membrana que mantiene el funcionamiento durante días mientras convierte de forma eficiente el CO2 en ácido fórmico, un líquido que puede usarse como materia prima química, conservante o portador de energía.
Por qué los dispositivos actuales de CO2 se obstruyen
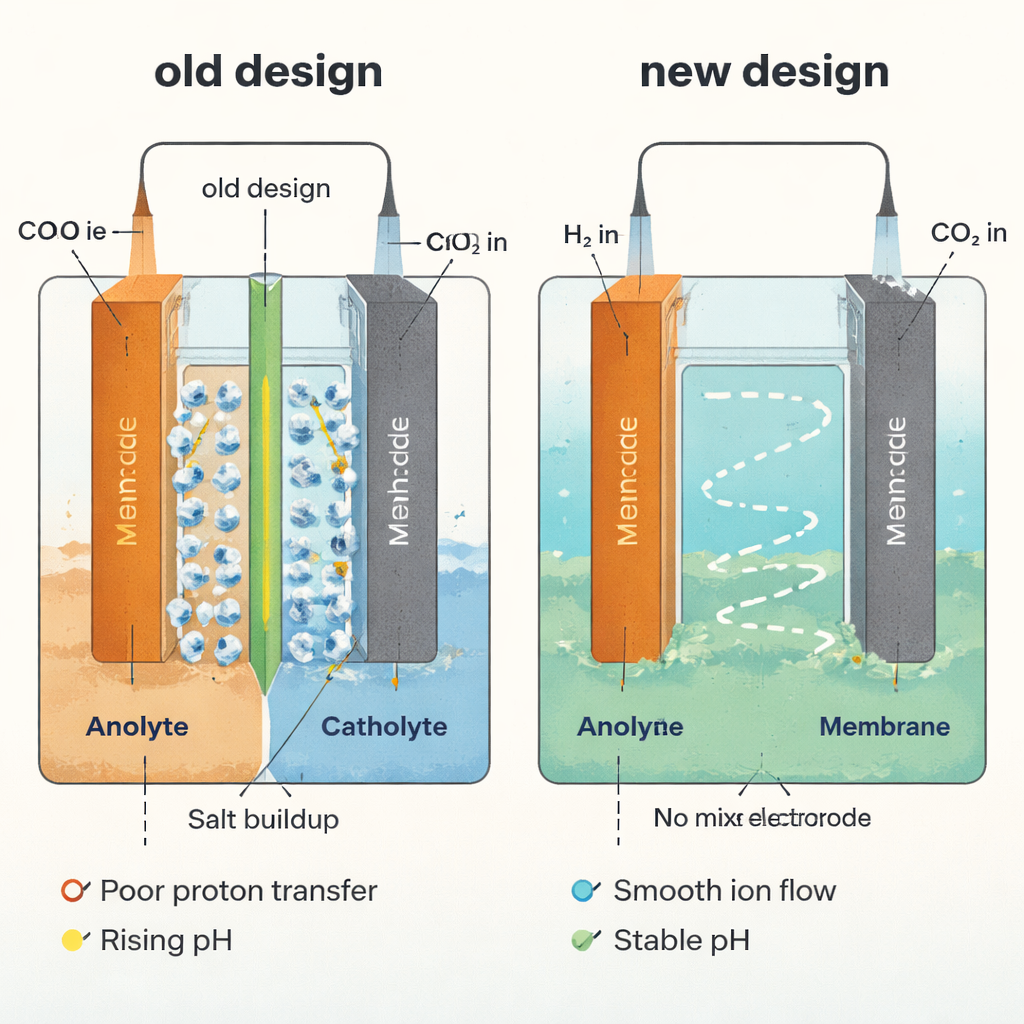
Muchos dispositivos que convierten CO2 en productos químicos se parecen a pilas de combustible compactas. El CO2 se alimenta a un lado (el cátodo), donde se convierte en productos, mientras que en el otro lado (el ánodo) se divide el agua para suministrar las cargas positivas necesarias (protones). Entre ambos lados hay una lámina polimérica fina llamada membrana, que permite el paso de ciertos iones pero mantiene los líquidos separados. En medios alcalinos o neutros, gran parte del CO2 reacciona con hidróxido para formar sales de carbonato en lugar de productos útiles, desperdiciando carbono y obligando a reciclajes energéticamente costosos. Los medios ácidos pueden evitar esto, pero entonces el sistema depende de la capacidad de la membrana para entregar protones rápida y uniformemente. Cuando la entrega de protones se retrasa, la acidez local en el cátodo tiende a subir, se cristalizan carbonatos y bicarbonatos, y las sales sólidas bloquean progresivamente las vías de gas necesarias para que el CO2 alcance el catalizador.
Una nueva manera de mover protones sin barrera
El equipo primero cuantificó cuán eficientemente se mueven los protones a través de las membranas en reactores ácidos típicos, introduciendo una medida simple: el número de protones que cruzan por cada electrón que pasa por el circuito. Usando teoría y simulaciones por ordenador, mostraron que las membranas reales rara vez alcanzan la transferencia ideal de protones. Películas más gruesas, menor selectividad protónica y ciertas mezclas iónicas ralentizan el movimiento de protones y crean una acidez desigual entre ambos lados. Los experimentos confirmaron esto: en una celda estándar con membrana, la catolita (el líquido en el cátodo) pasó de fuertemente ácida a casi neutra en pocas horas, favoreciendo la formación de carbonatos y la precipitación de sales en el interior del electrodo de difusión de gas.
Hidrogenación de CO2 sin membrana
Para escapar por completo del cuello de botella de la membrana, los investigadores la eliminaron y dejaron que un único líquido compartido fluyera junto a ambos electrodos. Eso por sí solo estabilizó el pH, pero generó un nuevo problema: el valioso ácido fórmico producido en el cátodo podía oxidarse en un ánodo convencional que realiza la reacción de evolución de oxígeno, la cual opera a un voltaje relativamente alto donde muchas moléculas orgánicas se oxidan. La solución fue reemplazar la evolución de oxígeno por la reacción de oxidación de hidrógeno—básicamente “quemar” hidrógeno para producir protones a muy bajo voltaje. En este electrólito de hidrogenación de CO2 sin membrana, se suministra hidrógeno al ánodo, CO2 al cátodo, y el líquido en flujo mezcla rápidamente los protones y el hidróxido producidos en cada lado, evitando cualquier gradiente de pH duradero y reduciendo drásticamente la acumulación de sales.
Catalizador inteligente y rendimiento a largo plazo
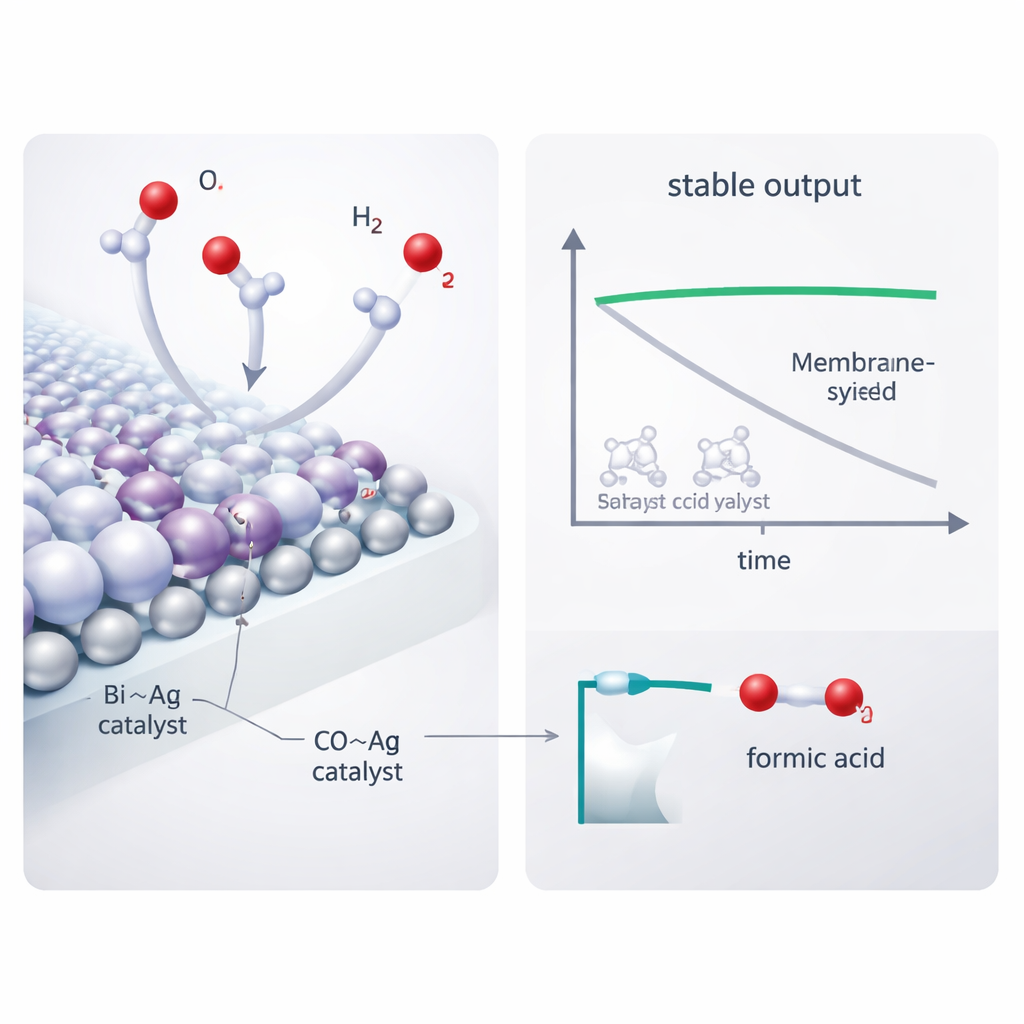
En el núcleo del cátodo, los autores construyeron un catalizador de bismuto–plata (Bi–Ag) que combina la afinidad del bismuto por formar formiato con la excelente conductividad eléctrica de la plata. Microscopía y espectroscopía revelaron nanopartículas de plata decorando nanosuperficies de bismuto y sutiles interacciones electrónicas entre los dos metales que mejoran la adsorción y activación del CO2. En solución ácida, este catalizador convirtió CO2 en ácido fórmico con más del 90% de eficiencia en un amplio rango de corriente. Al colocarlo en el reactor acoplado a hidrógeno sin membrana, alcanzó más del 90% de eficiencia a 100 miliamperios por centímetro cuadrado usando solo 1,7 voltios—significativamente menos que diseños competidores—y funcionó de forma estable durante 208 horas. Solo se detectaron trazas de sales de carbonato en el electrodo tras días de operación, lo que demuestra que el problema de precipitación se suprimió en gran medida.
Del montaje de laboratorio a la mejora práctica del CO2
Más allá de demostrar que el concepto funciona, el equipo llevó el diseño hacia la relevancia en el mundo real. Al reducir el canal de líquido entre los electrodos, disminuyeron la resistencia eléctrica y mantuvieron un alto rendimiento a voltajes menores. Lograron una eficiencia de conversión de CO2 en una sola pasada de hasta el 77%, lo que significa que la mayor parte del CO2 que entra en la celda se transformó en producto en un único paso. Modelos económicos sugirieron que eliminar la membrana, reducir el uso de energía y lograr una alta utilización del carbono pueden reducir significativamente el coste de producir ácido fórmico, aunque más ahorros dependerán de electricidad más barata, una separación más eficiente del producto del líquido y operación a corrientes más altas. En conjunto, el trabajo demuestra una vía práctica para convertir CO2 residual en un químico líquido útil a la vez que evita un problema clave de durabilidad que ha afectado a diseños de reactores anteriores.
Cita: Da, Y., Fan, L., Wang, W. et al. Membrane-free CO2 hydrogenation electrolyzer for salt precipitation management in acidic electrochemical CO2 reduction. Nat Commun 17, 1872 (2026). https://doi.org/10.1038/s41467-026-68600-3
Palabras clave: electrorreducción de CO2, ácido fórmico, electrólito sin membrana, oxidación de hidrógeno, utilización del carbono