Clear Sky Science · es
Cianación C–H regiodivergente y enantioselectiva de aminas secundarias controlada por ligando
Por qué cambiar enlaces diminutos importa para medicamentos importantes
Muchos fármacos más vendidos contienen pequeños bloques constructivos a base de nitrógeno llamados aminas. Cambios sutiles en cómo se conectan los átomos alrededor de estas aminas pueden convertir un medicamento débil en un tratamiento potente y preciso —o en algo inactivo o incluso perjudicial. Este artículo describe una nueva forma de modificar estos bloques amínicos a voluntad, permitiendo a los químicos elegir exactamente dónde en la molécula reaccionar y qué forma enantiomérica (imagen especular) producir, dos aspectos cruciales para diseñar fármacos más seguros y eficaces.
Elegir un sitio en una molécula congestionada
Las aminas en fármacos a menudo tienen varios enlaces carbono–hidrógeno (C–H) muy similares que normalmente se comportan casi igual. Los químicos desean sustituir solo uno de esos hidrógenos por un grupo útil, como un grupo ciano (–CN), sin alterar el resto de la molécula. Eso es difícil porque las reacciones estándar tienden a ir al sitio más reactivo marcado por la estructura de la molécula, no por la elección del químico. Aquí, los autores trabajan con aminas secundarias simples y flexibles que llevan dos cadenas de carbono distintas en el nitrógeno. Muestran que, partiendo de la misma amina, pueden dirigir la reacción a una de dos posiciones vecinas —ya sea junto al pequeño grupo N‑metilo (el llamado sitio α′) o un carbono más alejado en la otra cadena (el sitio β)— simplemente cambiando el ligando que rodea a un catalizador de cobre.
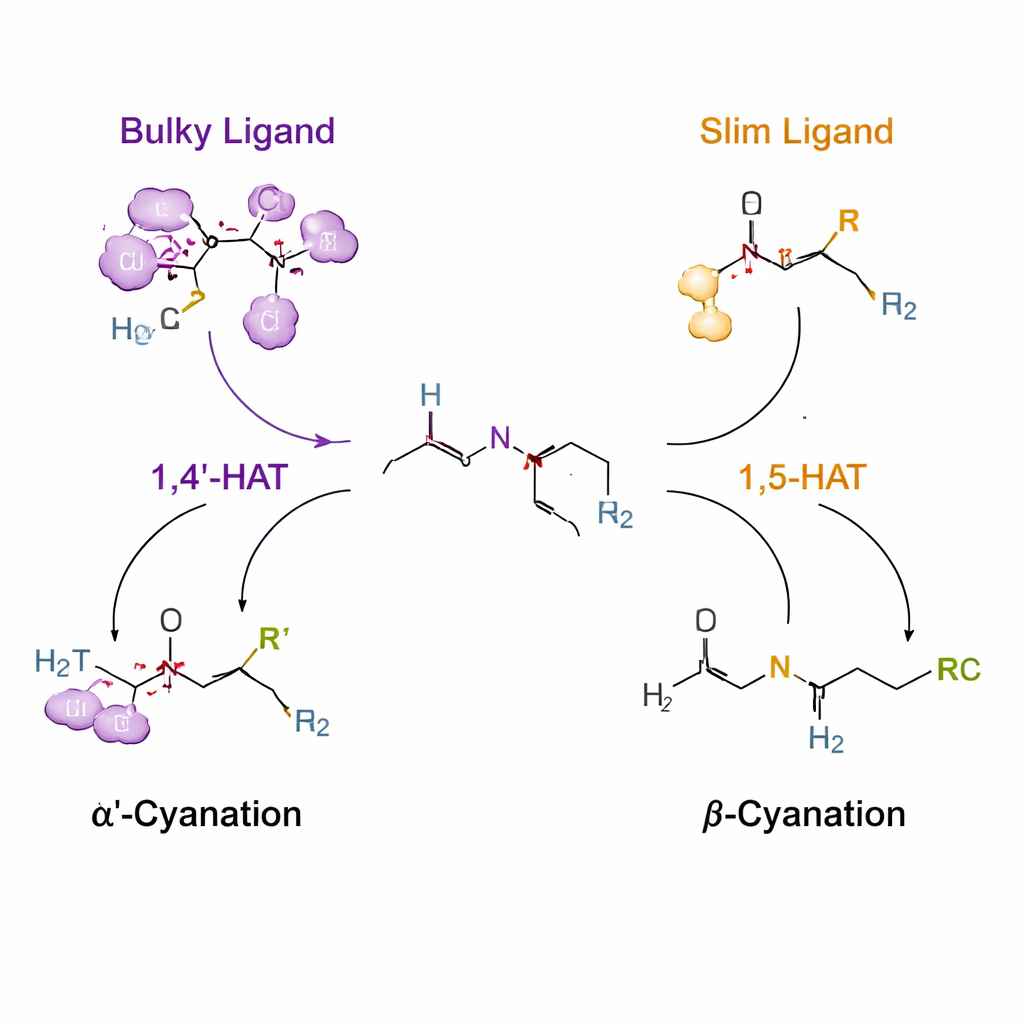
Usar “saltos” controlados de hidrógeno para guiar la reactividad
El truco clave se basa en un proceso llamado transferencia de átomo de hidrógeno, donde un radical de corta vida centrado en nitrógeno arranca un hidrógeno de un carbono cercano. Normalmente, tales radicales prefieren una distancia determinada, favoreciendo un “alcance” de seis miembros conocido como 1,5‑HAT. Los autores acoplan un grupo urea temporal y una manija de cloro a la amina para que, bajo catálisis de cobre, se forme este radical nitrogenado y pueda tomar hidrógeno tanto del sitio α′ como del β. Diseñando ligandos —moléculas orgánicas que envuelven al cobre— reconfiguran el entorno del radical. Un ligando muy voluminoso (denominado L14) empuja el sistema hacia un inusual paso 1,4′‑HAT que apunta al grupo N‑metilo, proporcionando cianación selectiva en α′. Ligandos más delgados (como L8) permiten la vía convencional 1,5‑HAT, dirigiendo la reacción al sitio β.
Del control de la posición al control de la quiralidad
Más allá de elegir dónde reaccionar, el equipo también busca controlar la quiralidad, que es vital porque muchos fármacos existen en formas izquierda y derecha que se comportan de manera diferente en el organismo. Para lograrlo introducen ligandos quirales —moléculas que tienen una forma con quiralidad— en el complejo de cobre. Dos de estos ligandos, L24 y L41, dan una alta preferencia por una de las imágenes especulares cuando la reacción instala un grupo ciano en posiciones β, incluyendo tanto sitios benílicos (junto a anillos aromáticos) como alílicos (junto a dobles enlaces carbono–carbono). A través de una amplia variedad de aminas de partida, el método entrega productos β‑cianados con excelente selectividad tanto de sitio como de quiralidad, y funciona a escala de gramos, mostrando que el proceso es práctico y robusto para la síntesis.
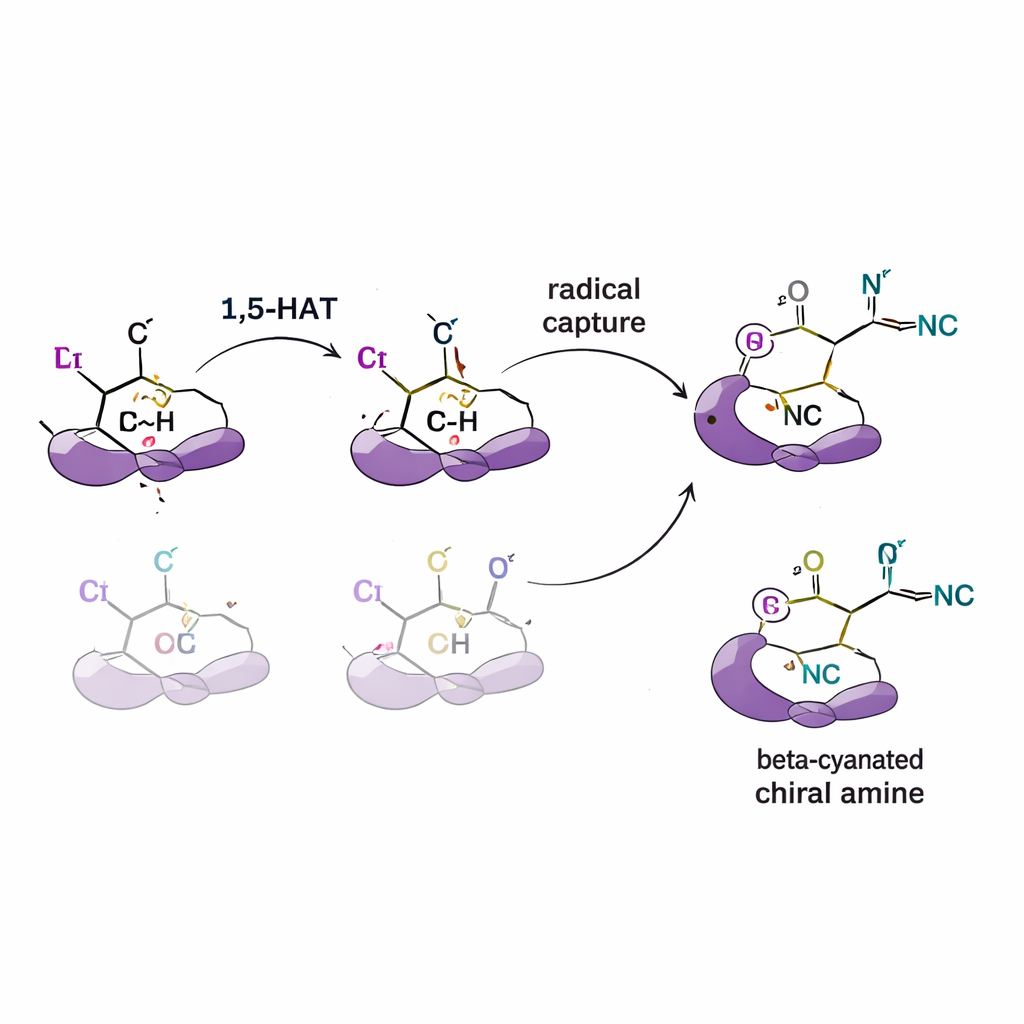
Comprobando el mecanismo detrás de la selectividad
Para entender cómo surge este control, los autores realizan una serie de experimentos mecanísticos. Añadiendo “trampas” de radicales, confirman que intervienen realmente intermedios radicalarios reactivos. Usando sustratos en los que ciertos hidrógenos se reemplazan por deuterio (una forma más pesada de hidrógeno), detectan efectos isotópicos cinéticos que señalan que el paso de transferencia de hidrógeno es la etapa lenta que determina la selectividad de la reacción. Experimentos de etiquetado también muestran que el hidrógeno se mueve en un único paso unidireccional en lugar de ir y venir entre posiciones. Simulaciones computacionales complementarias (teoría del funcional de la densidad) respaldan estos hallazgos, indicando que la forma y el volumen del ligando alteran la energía de las vías competidoras de transferencia de hidrógeno y la manera en que el radical luego se combina con el cobre y el cianuro para dar una imagen especular preferida.
Qué significa esto para el diseño futuro de fármacos
En conjunto, este trabajo introduce una estrategia flexible para reingenierizar grupos de amina comunes en dos sitios estrechamente relacionados, a demanda, con control fino de la quiralidad molecular. Cambiando solo el ligando de un catalizador de cobre, los químicos pueden elegir si colocar un grupo ciano en una pequeña unidad N‑metilo o en el carbono vecino de una cadena lateral diferente, y hacerlo en muchas moléculas complejas de tipo fármaco. Dado que los grupos ciano son valiosos puntos de partida hacia muchos otros grupos funcionales, este enfoque de “marcar el sitio” y “marcar la mano” debería facilitar la exploración y optimización de nuevos medicamentos construidos a partir de los mismos esqueletos amínicos básicos.
Cita: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
Palabras clave: funcionalización de aminas, transferencia de átomo de hidrógeno, catálisis con cobre, cianación enantioselectiva, química medicinal