Clear Sky Science · es
Localizaciones genómicas duales y funciones reguladoras de MBD-2 con y sin NuRD en Caenorhabditis elegans, que carece de metilación del ADN
Cómo los gusanos diminutos reescriben las reglas del control génico
Nuestras células usan marcas químicas en el ADN y en las proteínas para recordar qué genes deben estar encendidos o apagados. Una de las etiquetas más conocidas, la metilación del ADN, falta en algunos animales, pero aun así estos se desarrollan y reproducen con normalidad. Este trabajo explora cómo un gusano pequeño, Caenorhabditis elegans, gestiona el control génico sin metilación del ADN, revelando un sistema de respaldo inesperadamente flexible que podría cambiar nuestra visión sobre la epigenética.
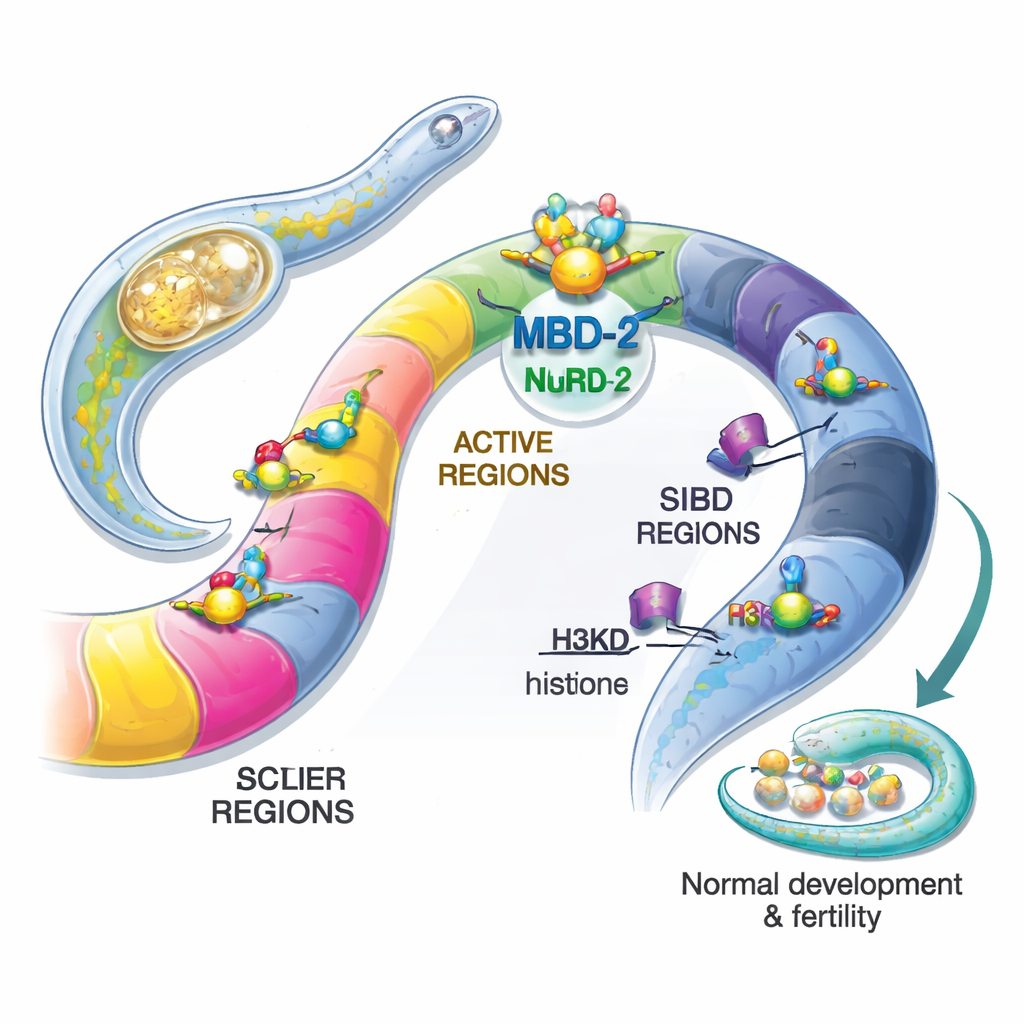
Una marca del ADN ausente plantea una gran cuestión
En los mamíferos, una marca química llamada 5‑metilcitosina (5mC) ayuda a silenciar genes durante el desarrollo, la inactivación del cromosoma X y la defensa frente a elementos móviles. Proteínas llamadas MBD2 y MBD3 leen estas marcas y reclutan una gran maquinaria proteica, el complejo NuRD, que puede remodelar y desactivar tramos de cromatina. Curiosamente, muchos invertebrados, incluidos C. elegans y la mosca de la fruta, han perdido la 5mC y las enzimas que la escriben, pero conservaron una proteína parecida a MBD2/3. Esto plantea un rompecabezas: ¿por qué mantener un “lector de metilación del ADN” en un genoma que ya no usa esa marca, y qué función desempeña en su lugar?
Una proteína andamiaje sin la que los gusanos no pueden vivir
Los autores se centraron en la versión de esta proteína en el gusano, denominada MBD‑2. A diferencia de sus homólogos mamíferos, MBD‑2 del gusano ha perdido el dominio clásico de unión a metil‑citosina, pero conserva segmentos flexibles y en espiral que pueden acoplarse a otras proteínas. Etiquetando MBD‑2 con marcadores fluorescentes, el equipo mostró que se localiza en los núcleos de casi todas las células a lo largo de la vida del gusano, coherente con un papel amplio en la regulación génica. Mediante ingeniería genética, crearon gusanos totalmente carentes de MBD‑2 y otros que carecían solo de su región de hélice en espiral, responsable del contacto con NuRD. Ambas mutaciones provocaron problemas severos: animales pequeños, con movilidad reducida, estructuras reproductoras malformadas y en gran medida estériles. Esto demostró que MBD‑2 es esencial para el desarrollo y la fertilidad normales, incluso en ausencia de metilación del ADN.
Reconstruyendo la máquina NuRD en un mundo sin metilación
Para averiguar si MBD‑2 del gusano aún funciona con NuRD, los autores purificaron MBD‑2 etiquetado de extractos de gusano e identificaron sus socios por espectrometría de masas. La mayoría de los componentes conocidos de NuRD estuvieron presentes, confirmando que MBD‑2 actúa como andamiaje central en este complejo, de forma similar a MBD2/3 en mamíferos. Cuando se eliminó la región de hélice en espiral, muchas de estas interacciones se perdieron, especialmente las relacionadas con proteínas que remodelan nucleosomas. Al mismo tiempo, secuenciación masiva de ARN a gran escala reveló que más de una cuarta parte de los genes del gusano cambiaron su actividad en los mutantes de MBD‑2, con muchos más genes activándose que reprimiéndose. Este patrón indica que MBD‑2, con frecuencia junto a NuRD, actúa mayoritariamente como represor para mantener silenciosos genes inapropiados, a la vez que ayuda a sostener la actividad adecuada de un subconjunto de genes altamente expresados.
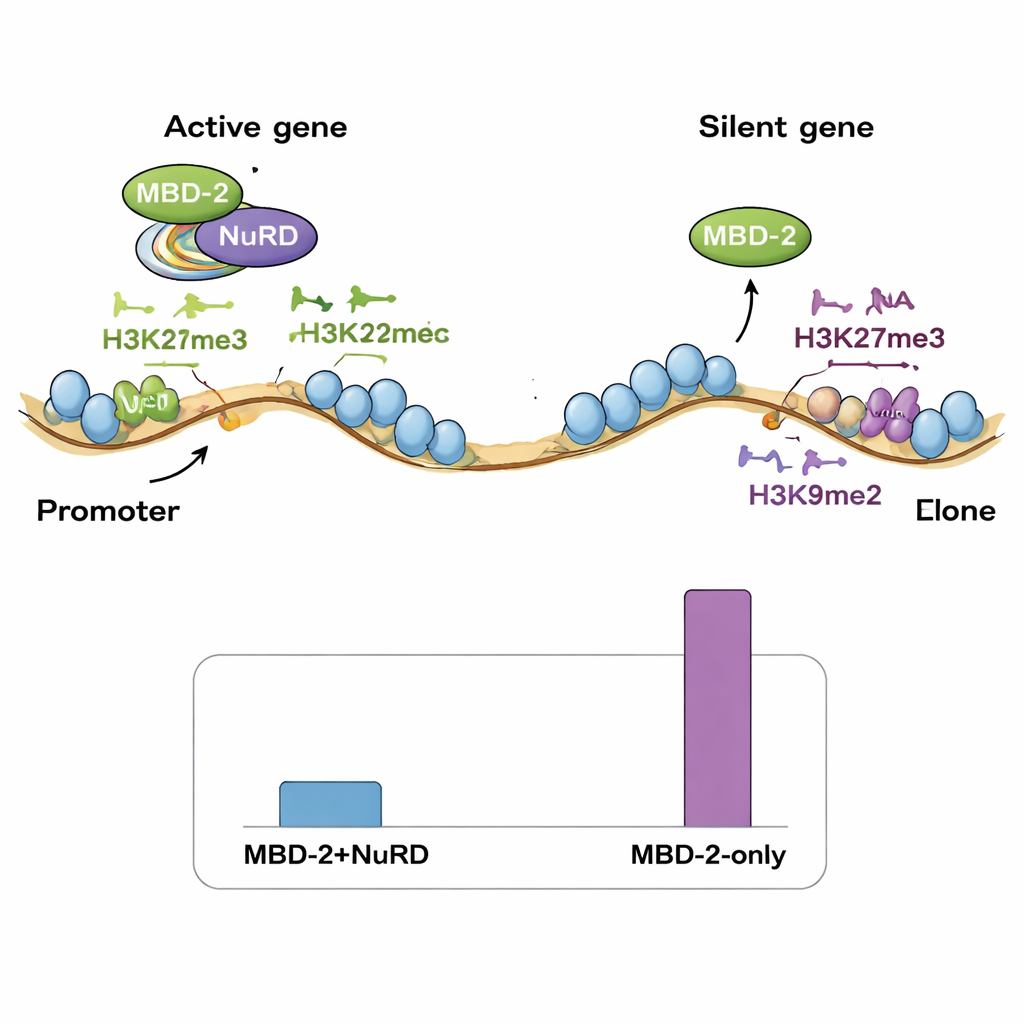
Dos modos de unión en el genoma
A continuación, el equipo mapeó dónde se localiza MBD‑2 a lo largo del genoma usando ChIP‑seq y comparó esas ubicaciones con mapas existentes de componentes de NuRD y varias marcas de histonas. Sorprendentemente, solo una pequeña fracción de los sitios de MBD‑2 se solaparon estrechamente con proteínas de NuRD y marcas de cromatina abierta y activa. La gran mayoría de los sitios de MBD‑2 se situaron en otros lugares, en las “brazos” cromosómicos ricos en marcas represivas de histonas como H3K27me3 y H3K9me2/3. En otras palabras, MBD‑2 muestra un comportamiento dual: en una minoría de sitios viaja con NuRD para afinar genes activos, pero en muchos más sitios se une de forma independiente en regiones ya silenciosas. El patrón de su unión dentro de los genes también importa: cuando MBD‑2 se agrupa cerca de los sitios de inicio génico, la pérdida de la proteína tiende a activar esos genes, mientras que la unión más profunda en los cuerpos génicos suele asociarse con una reducción de la expresión cuando se elimina MBD‑2.
Un respaldo evolutivo para la metilación del ADN perdida
Los autores proponen que, en las especies que perdieron la metilación del ADN, las marcas represivas de histonas—especialmente H3K27me3—podrían haberse expandido para ocupar un nicho regulador similar. MBD‑2 del gusano parece haber sido reutilizado: en lugar de leer 5mC en el ADN, ahora se asocia con regiones de cromatina marcadas por modificaciones específicas de histonas, manteniendo además la capacidad de anclar el complejo NuRD mediante sus dominios conservados de interacción proteica. Este trabajo muestra que un conjunto antiguo de silenciamiento génico puede ser reconectado durante la evolución: la etiqueta química en el ADN puede desaparecer, pero la maquinaria proteica asociada sobrevive cambiando a señales alternativas. Para el público no especializado, el mensaje clave es que la regulación génica es notablemente adaptable: las células pueden perder una marca epigenética principal y aun así conservar el control complejo de miles de genes apoyándose más en otras etiquetas de la cromatina y en los roles de andamiaje versátiles de proteínas como MBD‑2.
Cita: Tsui, H.N., Wong, C.Y.Y., Zheng, C. et al. Dual genomic localizations and gene regulatory functions of MBD-2 with and without NuRD in Caenorhabditis elegans which lacks DNA methylation. Nat Commun 17, 1875 (2026). https://doi.org/10.1038/s41467-026-68592-0
Palabras clave: epigenética, cromatina, regulación génica, C. elegans, modificación de histonas