Clear Sky Science · es
Una enzima mononuclear no hemo con mucha dinamismo para la biosíntesis de isonitrilos en dos pasos
Cómo las bacterias construyen herramientas químicas exóticas
Los isonitrilos son grupos químicos pequeños pero potentes que actúan como navajas suizas: pueden captar metales, reaccionar de muchas maneras distintas y con frecuencia funcionan como el “grupo activo” de poderosos antibióticos y toxinas naturales. Algunas bacterias patógenas, incluido el agente de la tuberculosis Mycobacterium tuberculosis, cosen isonitrilos a moléculas grasas para ayudar a robar metales de su huésped. Este artículo explora cómo una de sus enzimas, llamada Rv0097, lleva a cabo esta química particularmente exigente en dos pasos cuidadosamente coreografiados.
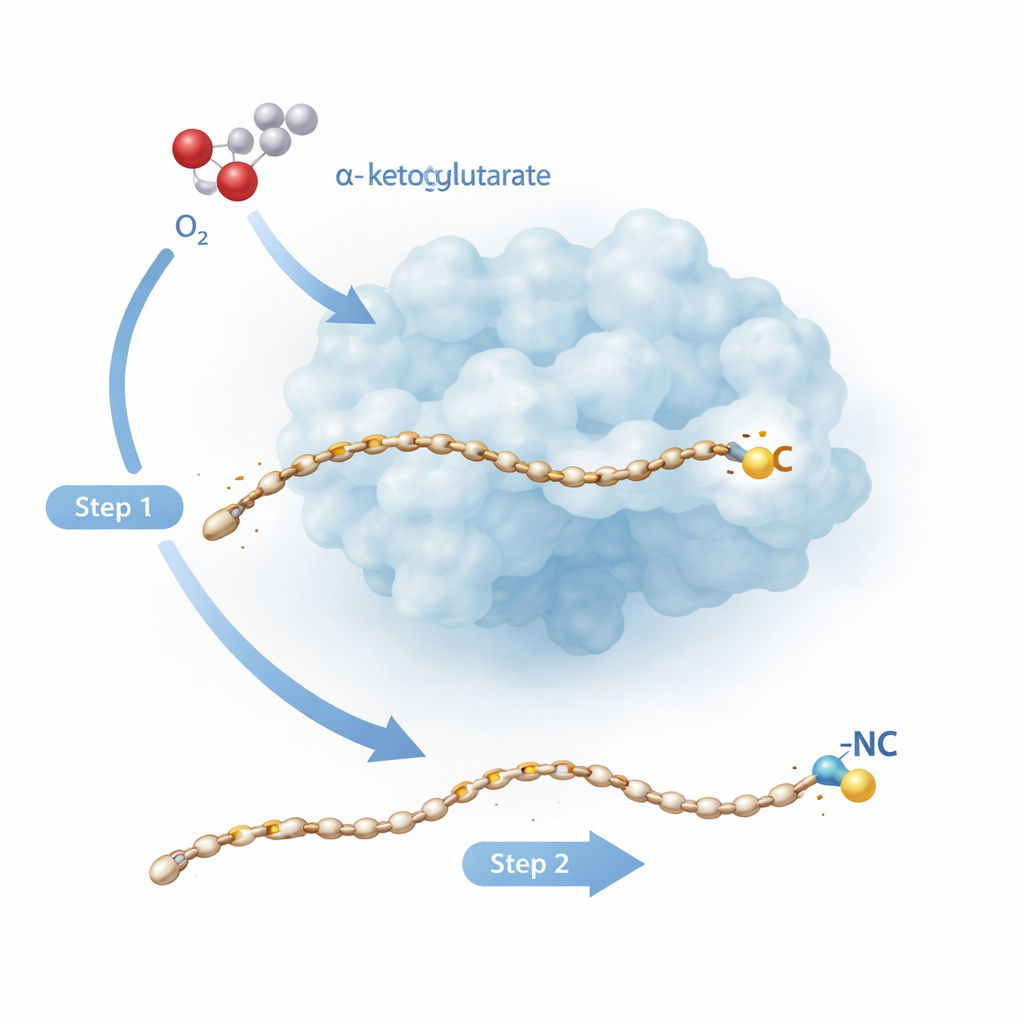
Una transformación molecular en dos pasos
Rv0097 pertenece a una amplia familia de enzimas dependientes de hierro que normalmente realizan tareas más sencillas, como añadir oxígeno en un único punto de una molécula. Aquí la tarea es más difícil: partiendo de un bloque constructivo “glicil–ácido graso”, la enzima debe crear un grupo isonitrilo completamente nuevo, con ambos átomos clave —el carbono y el nitrógeno— procedentes del mismo fragmento pequeño de glicina. Trabajos previos sobre una enzima relacionada, ScoE, sugirieron que esto no puede hacerse en una sola pasada. En su lugar, se necesitan dos “semiciclos” de reacción separados, cada uno impulsado por una especie hierro‑oxígeno formada cuando la enzima descompone una molécula auxiliar llamada α‑cetoglutarato y la combina con oxígeno del aire. El nuevo estudio se centra en la enzima de la tuberculosis Rv0097 para observar, a resolución atómica, cómo una enzima enlaza estos dos pasos radicalarios sobre el mismo sustrato sin perder el control.
Congelando la enzima en acción
Mediante cristalografía de rayos X, los investigadores capturaron dieciséis instantáneas de alta resolución de Rv0097 en diferentes estados: vacía, unida a su sustrato graso (una molécula de diez carbonos llamada CADA), unida al cofactor α‑cetoglutarato y en combinaciones que imitan intermedios de reacción fugaces. Estas estructuras muestran que Rv0097 tiene una personalidad dividida. En reposo, su sitio activo está mayormente cerrado, con un aminoácido clave (fenilalanina 102) alternando entre dos orientaciones que mantienen seco el bolsillo para la larga cola grasa y listo para la unión hidrofóbica. Cuando se une CADA, este residuo adopta una orientación única y la cabeza polar del sustrato queda anclada por cadenas laterales cargadas mientras su cola aceitosa se acomoda en un túnel ajustado. Mutar este par de compuertas (F102 y una glicina cercana, G204) bloquea el bolsillo o deja entrar demasiada agua, reduciendo drásticamente la actividad y cambiando las longitudes de cadena preferidas por la enzima.
Tapas móviles y bucles dinámicos
Más allá del bolsillo del sustrato, Rv0097 se comporta como una pequeña máquina con puertas móviles. El equipo observó conformaciones “abiertas” y “cerradas” en las que dos regiones tipo tapa se separan o se juntan sobre el sitio activo. Abrir expone el centro de hierro y crea una vía para que entren el α‑cetoglutarato y el sustrato; cerrar aísla la química del agua circundante una vez que la reacción está en marcha. Dos bucles superficiales flexibles, denominados bucle His y bucle Arg por la histidina y la arginina que contienen, actúan como una compuerta adicional. En algunas estructuras, estos bucles se pliegan hacia adentro para que el residuo de arginina pueda captar el α‑cetoglutarato; en otras se abren hacia fuera, aparentemente creando un canal lateral por el que pueden salir los fragmentos auxiliares gastados (succinato y dióxido de carbono) y por el que puede deslizarse un nuevo α‑cetoglutarato para el segundo paso, todo ello mientras el intermedio derivado del sustrato permanece sujetado en su lugar.
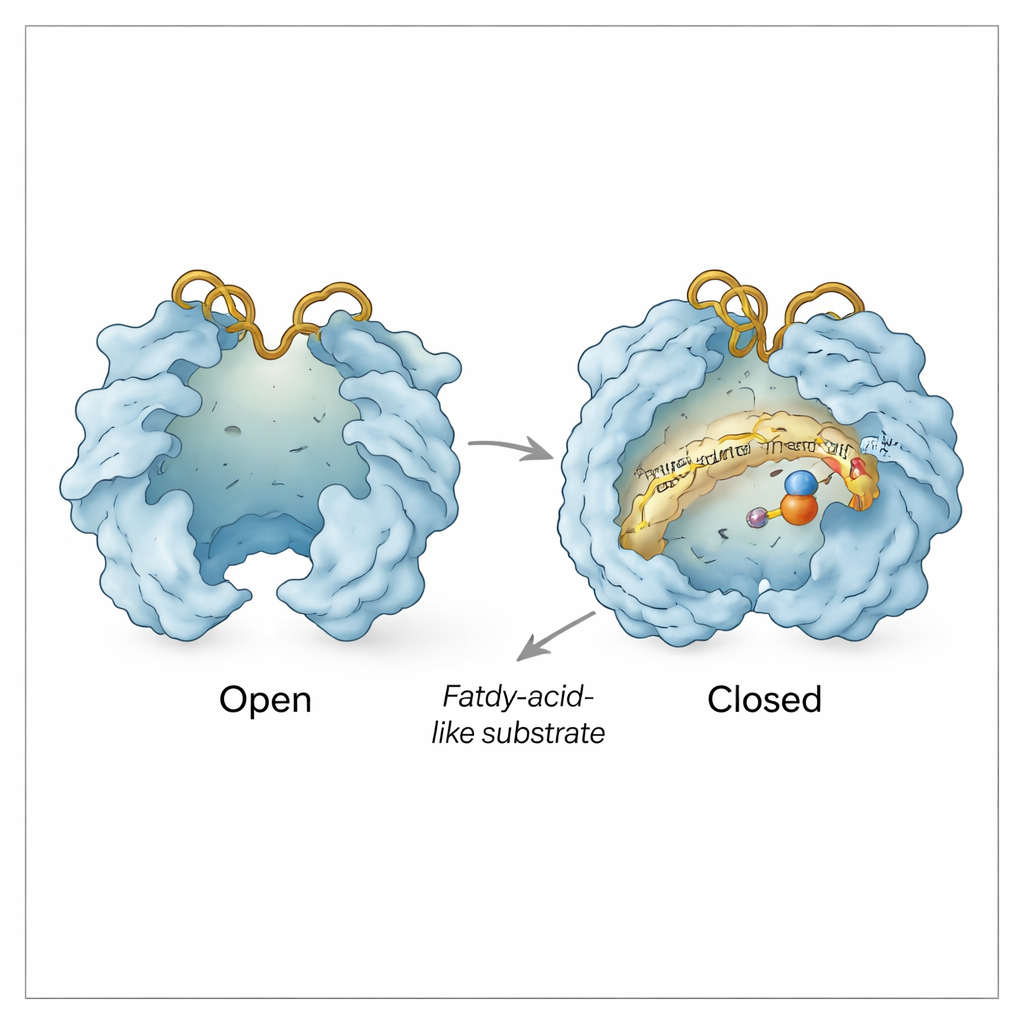
Protegiendo un intermedio frágil
Ensayos bioquímicos respaldan esta imagen estructural. La primera mitad de la reacción convierte CADA en un intermedio imina altamente reactivo que se descompondría con rapidez si se disolviera en solución. Al atrapar químicamente su producto de degradación, los autores muestran que la mayor parte de este intermedio solo se detecta cuando la enzima aún está presente, lo que implica que permanece unido y protegido dentro de Rv0097 entre las dos semicarreras de la reacción. Las estructuras explican cómo: el reposicionamiento sutil de los bucles His y Arg, junto con pequeños desplazamientos de residuos cercanos, parecen sellar el intermedio en una cavidad resguardada mientras permiten que moléculas pequeñas como α‑cetoglutarato, succinato y dióxido de carbono intercambien a través de canales controlados.
Por qué esto importa para la tuberculosis y más allá
En conjunto, estos resultados revelan a Rv0097 como una línea de ensamblaje altamente dinámica y de una sola proteína que usa química basada en hierro dos veces seguidas sobre el mismo sustrato sin liberar nunca un producto intermedio peligroso. Para las bacterias de la tuberculosis, esta precisión sustenta la fabricación de moléculas decoradas con isonitrilo que les ayudan a obtener metales esenciales dentro del organismo, y estudios genéticos indican que la vía es importante para su supervivencia durante la infección. Para químicos y diseñadores de fármacos, el trabajo ofrece un plano para diseñar enzimas afines capaces de construir nuevos compuestos que contengan isonitrilos, y sugiere que interferir con las tapas y compuertas móviles de Rv0097 podría ser una vía para desarrollar nuevos antibióticos.
Cita: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
Palabras clave: biosíntesis de isonitrilos, enzima no hemo de hierro, Mycobacterium tuberculosis, dinámica enzimática, productos naturales quelantes de metales