Clear Sky Science · es
La alteración de la homeostasis del hierro sensibiliza el cáncer de páncreas a la electroporación irreversible
Volver la electricidad y el hierro contra un cáncer letal
El cáncer de páncreas es uno de los más difíciles de tratar, y aun las terapias locales agresivas con frecuencia no evitan la recidiva. Este estudio explora una forma nueva de mejorar un procedimiento ya existente—la electroporación irreversible, que elimina tumores mediante pulsos eléctricos cortos y potentes—para hacerlo más eficaz y seguro. Alterando de manera inteligente cómo las células cancerosas gestionan el hierro, los investigadores muestran que pueden empujar a las células supervivientes hacia una forma destructiva de muerte, lo que potencialmente reduce la probabilidad de que el tumor vuelva a aparecer.
Por qué los pulsos eléctricos por sí solos no bastan
La electroporación irreversible (IRE) trata los tumores insertando electrodos finos en o alrededor del cáncer y disparando pulsos rápidos de alto voltaje. Estos pulsos perforan de forma permanente las membranas celulares, matando muchas células tumorales y provocando una respuesta inmune. Pero el campo eléctrico no es perfectamente uniforme. Áreas que reciben pulsos algo más débiles pueden dejar células cancerosas vivas, y esas supervivientes pueden dar lugar a un nuevo tumor. Cuando el equipo examinó de cerca células de cáncer pancreático y tumores de ratón expuestos a un campo eléctrico subletal, comprobaron que en lugar de morir por un proceso impulsado por hierro llamado ferroptosis, estas células activaron un amplio programa antioxidante. Se aumentó la expresión de genes protectores clave, incluidos los que neutralizan el daño relacionado con el hierro, lo que permitió a las células capear la tormenta y recuperarse.
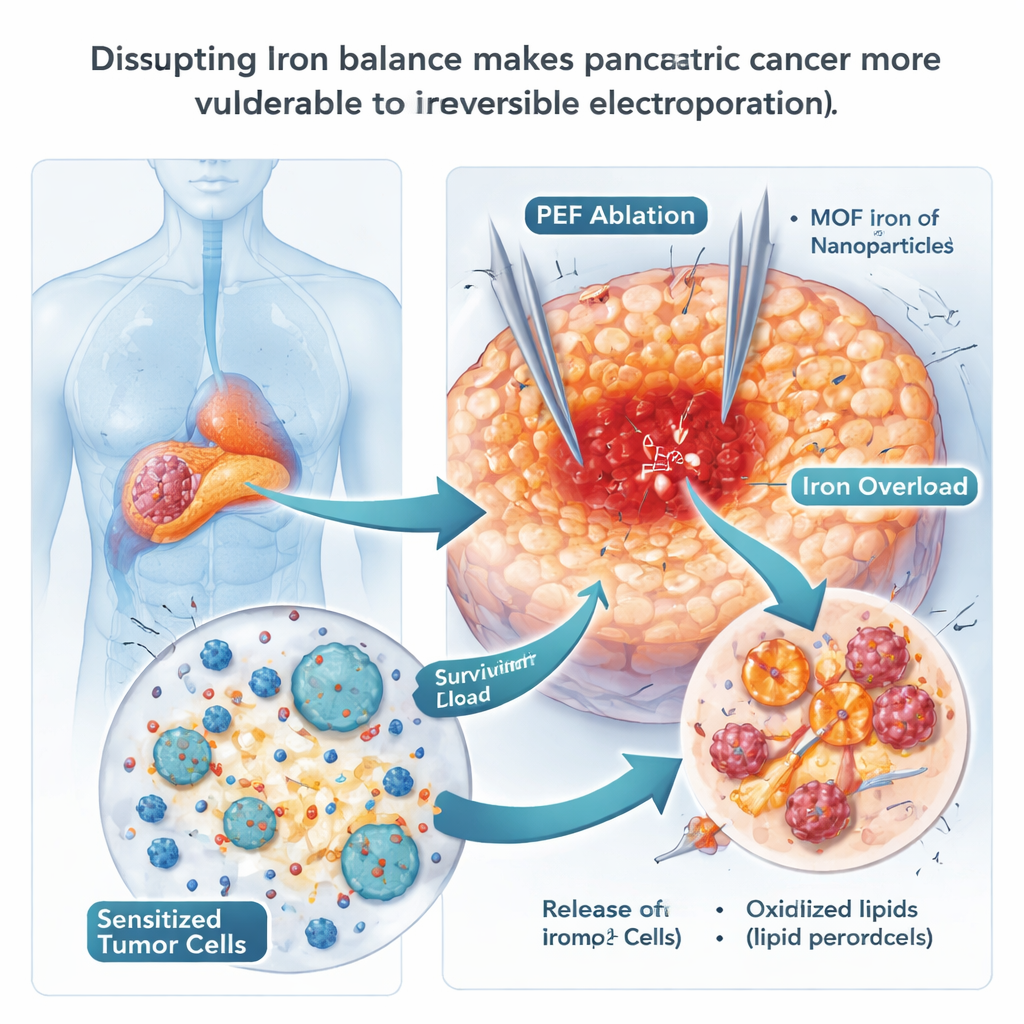
Uso de nanopartículas de hierro para empujar a las células hacia la destrucción
Dado que la ferroptosis depende del hierro, los científicos probaron si nanopartículas ricas en hierro podrían forzar a las células cancerosas a cruzar el umbral. Utilizaron partículas diseñadas a base de un armazón metal-orgánico que contienen hierro (MOF-Fe), que liberan rápidamente hierro dentro de los compartimentos ácidos de las células. En cultivos, las células de cáncer pancreático que internalizaron estas partículas acumularon hierro libre y grasas oxidadas en sus membranas, rasgos clásicos de la ferroptosis, y formaron muchas menos colonias. En ratones, la combinación de MOF-Fe con IRE retrasó la reaparición tumoral más tiempo que cualquiera de los tratamientos por separado, y los tumores mostraron más signos de daño oxidativo. Sin embargo, este beneficio fue temporal: tras unas tres semanas, los tumores empezaron a recuperarse, lo que sugiere que el cáncer halló una manera de adaptarse a la sobrecarga de hierro.
Apuntar a la "caja fuerte" del hierro celular
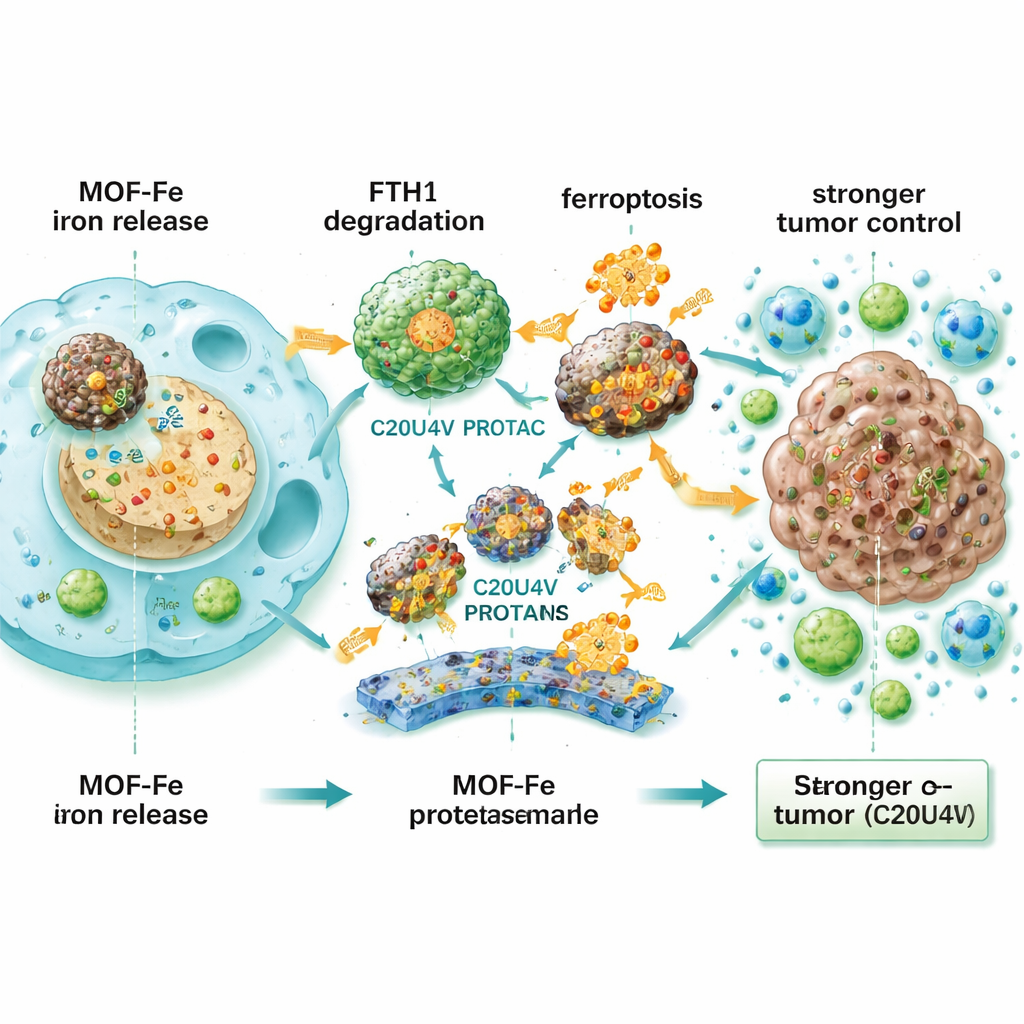
Para entender esta resistencia, el equipo analizó qué proteínas cambiaban tras el tratamiento con MOF-Fe. Un componente destacado fue la cadena pesada de la ferritina 1 (FTH1), parte del complejo de almacenamiento de hierro de la célula—el equivalente molecular de una caja fuerte ignífuga para el hierro sobrante. Cuando los niveles de FTH1 se elevaron experimentalmente, las células cancerosas se volvieron más resistentes a la ferroptosis; cuando FTH1 se redujo, se hicieron más vulnerables. Esto apuntó a FTH1 como un escudo central contra la muerte impulsada por el hierro. A continuación, los investigadores crearon una molécula diseñada, C20U4V, elaborada a partir de ácido araquidónico (una grasa altamente oxidizable) ligada a una estructura tipo PROTAC que dirige proteínas específicas hacia la maquinaria celular de eliminación. En presencia de MOF-Fe, C20U4V se unió a la ferritina y la reclutó para ser etiquetada y degradada, reduciendo drásticamente los niveles de FTH1 e impidiendo que la célula guarde el hierro de forma segura.
De placas de cultivo a mini-tumores y ratones
Cuando se combinaron MOF-Fe y C20U4V, las células de cáncer pancreático mostraron mayor estrés oxidativo, más lípidos de membrana dañados, mitocondrias más afectadas y una capacidad notablemente reducida para regenerarse. Esta sinergia también apareció en organoides tridimensionales derivados de pacientes—pequeñas estructuras tumorales cultivadas a partir de muestras reales—donde el par de fármacos colapsó el tamaño y el número de organoides. Como C20U4V es lipofílico e insoluble en agua, el equipo lo encapsuló en micelas sensibles al oxígeno reactivo (M-C20U4V) que circulan por la sangre y pueden liberar el fármaco en tejido tumoral estresado y dañado. En modelos murinos con tumores de páncreas implantados bajo la piel y en el propio páncreas, la combinación triple de IRE, MOF-Fe y M-C20U4V redujo los tumores con mucha más eficacia y prolongó la supervivencia en comparación con cualquier tratamiento simple o doble. Los tumores tratados mostraron menos células en división, más marcadores de ferroptosis y una mayor infiltración de células T y otras células inmunitarias, lo que indica que la estrategia no solo mata directamente a las células cancerosas sino que también ayuda al sistema inmunitario a reconocer y atacar el tumor.
Qué podría significar esto para los pacientes
Para un público no especialista, la idea clave es sencilla: los tumores pancreáticos a menudo escapan después de la ablación por pulsos eléctricos porque algunas células cancerosas sobreviven y se adaptan rápidamente. Este trabajo demuestra que sobrecargar esas células con hierro y, al mismo tiempo, desactivar su "bóveda" de seguridad para el hierro puede forzarlas a un estado autodestructivo que no pueden resistir fácilmente. Aunque este enfoque aún está en fase experimental y requeriría pruebas exhaustivas de seguridad y viabilidad en humanos, sugiere que afinar cómo los tumores gestionan un elemento tan básico como el hierro podría convertir un tratamiento local imperfecto en un golpe más decisivo contra uno de los cánceres más mortales.
Cita: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
Palabras clave: cáncer de páncreas, electroporación irreversible, ferroptosis, nanopartículas de hierro, terapia PROTAC