Clear Sky Science · es
Identificación de Chlamydia pneumoniae y activación del inflamasoma NLRP3 en la retina de la enfermedad de Alzheimer
Por qué importan los gérmenes en el ojo para la memoria
La enfermedad de Alzheimer suele considerarse un problema de placas y ovillos en el cerebro. Este estudio sugiere que una bacteria common que causa neumonía, Chlamydia pneumoniae, podría asentarse de forma silenciosa en el tejido fotosensorial en la parte posterior del ojo —la retina— y contribuir a la inflamación y el daño neuronal observados en el Alzheimer. Dado que la retina puede ser imagenada de forma no invasiva, este trabajo insinúa que en el futuro los exámenes oculares podrían ayudar a detectar enfermedades cerebrales vinculadas a infecciones y orientar tratamientos tempranos.
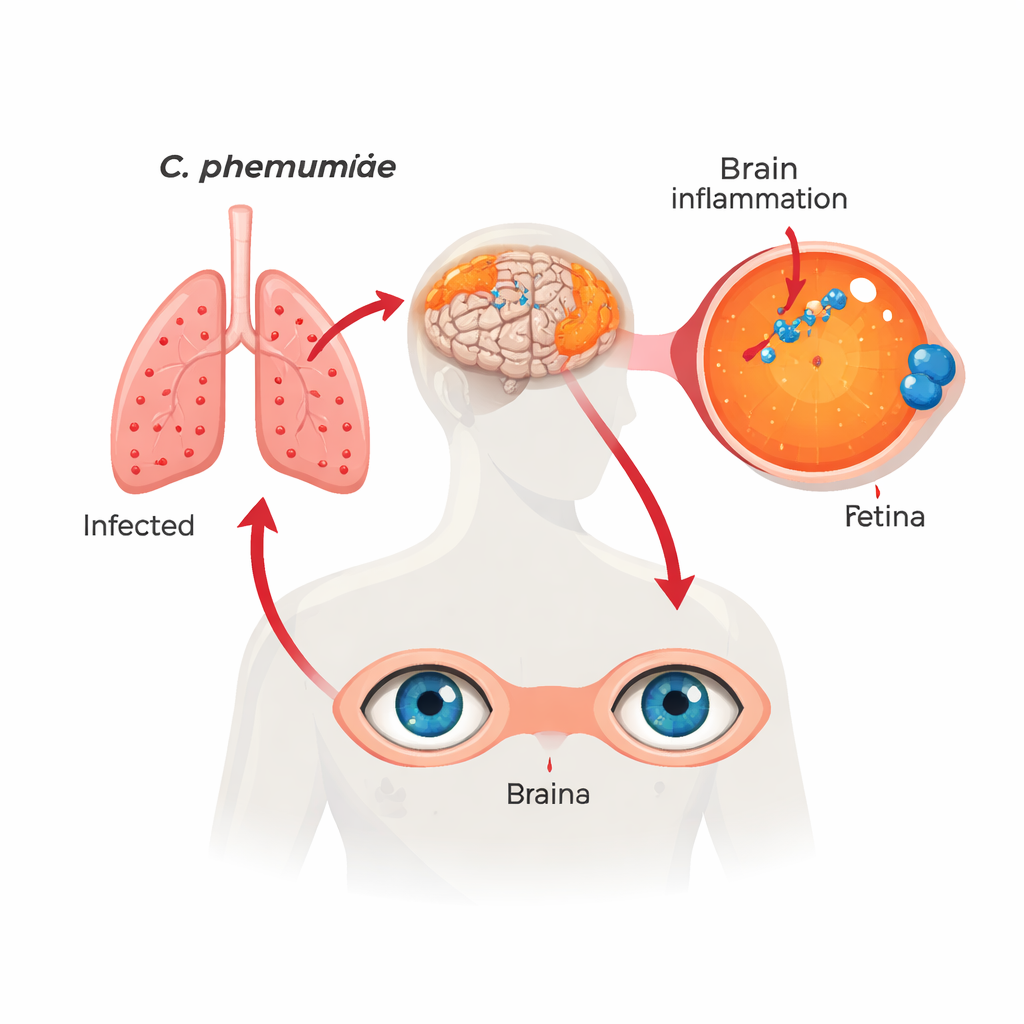
Una infección conocida en un lugar inesperado
Los investigadores examinaron retinas y muestras cerebrales emparejadas de más de 100 personas fallecidas que tenían función cognitiva normal, deterioro cognitivo leve o demencia por Alzheimer. Usando varias técnicas independientes —incluyendo anticuerpos especiales, sondas genéticas, métodos de tinción y pruebas de ADN— encontraron señales claras de Chlamydia pneumoniae dentro de células retinianas. Estas “inclusiones” bacterianas fueron más comunes y abundantes en personas con Alzheimer, menos en quienes tenían deterioro leve y menos aún en quienes permanecieron cognitivamente normales. La cantidad de bacteria en la retina se correspondía estrechamente con la encontrada en el cerebro, lo que sugiere que tanto el ojo como el cerebro participan en la misma infección de larga evolución.
Enlaces entre bacterias, placas y capacidad cognitiva
Encontrar el germen fue solo el primer paso; la cuestión clave era si tenía impacto en la enfermedad. El equipo midió marcadores clásicos del Alzheimer en los mismos tejidos. Observaron que una mayor carga bacteriana en la retina iba de la mano con más depósitos de amiloide‑beta —la proteína pegajosa que forma placas— así como con ciertas formas anormales de la proteína tau. Las personas cuyos cerebros mostraban más señal bacteriana también tenían más ovillos en las fibras nerviosas, peor patología global del Alzheimer y más atrofia cerebral. Clínicamente, quienes tenían mayor carga bacteriana retiniana tendían a obtener peores puntuaciones en pruebas de memoria y pensamiento y presentaban demencia más avanzada. Los portadores de la variante genética APOE ε4, un factor de riesgo genético fuerte para el Alzheimer, albergaban más de la bacteria tanto en retina como en cerebro, lo que sugiere una interacción gen‑infección.
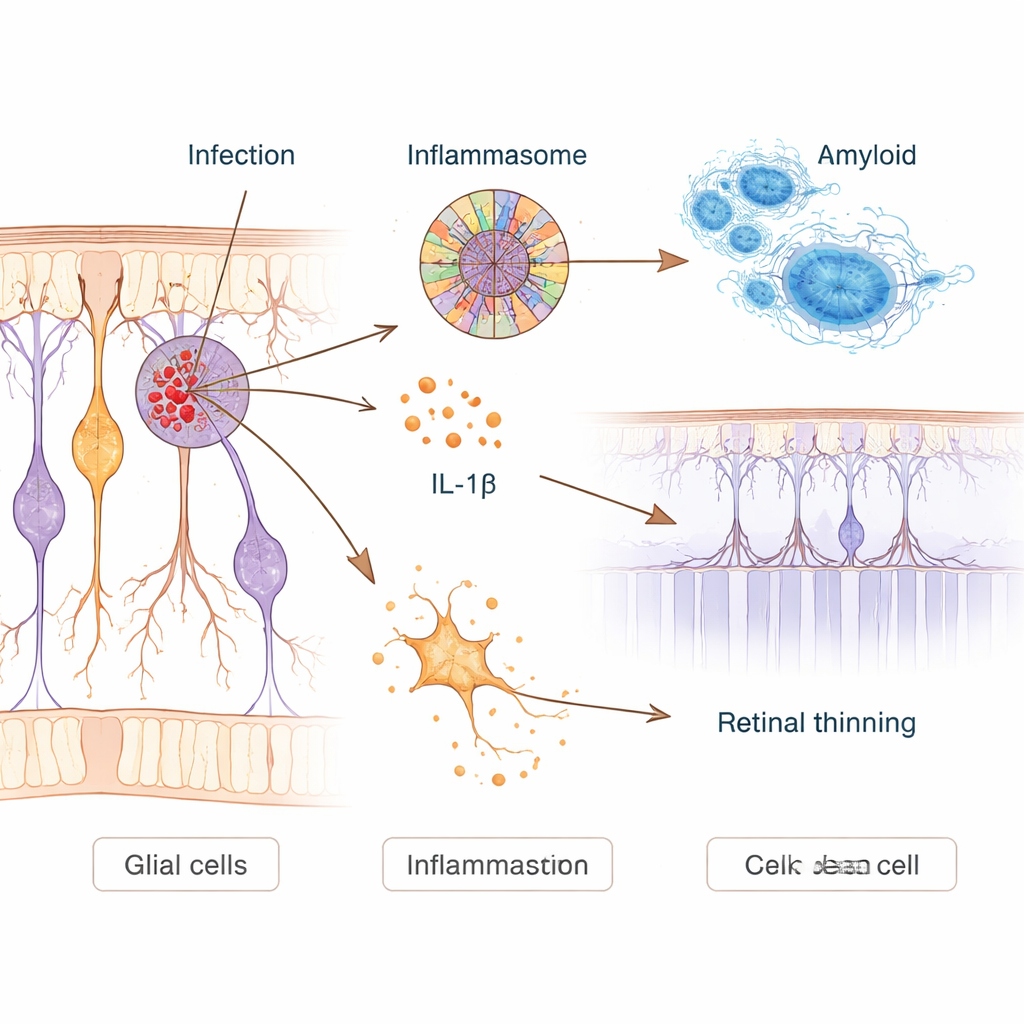
Cómo la infección puede desencadenar inflamación tóxica
Para indagar causa y efecto, los científicos infectaron en el laboratorio células humanas de tipo neuronal y ratones modelo de Alzheimer con Chlamydia pneumoniae. En neuronas en cultivo, la infección aumentó la producción de amiloide‑beta y activó un sistema de alarma molecular llamado inflamasoma NLRP3. Este sistema actúa como un cordón de seguridad celular: una vez activado libera mensajeros inflamatorios como la interleucina‑1β y puede perforar membranas celulares, conduciendo a una forma explosiva de muerte celular. Las neuronas infectadas mostraron signos claros de daño de membrana y activación de estas vías. En ratones, una única dosis nasal de la bacteria fue suficiente para que llegara al cerebro, donde aumentó las placas de amiloide, activó células inmunitarias y empeoró el rendimiento en tareas de laberinto basadas en memoria y visión meses después.
Células inmunitarias retinianas bajo presión
En ojos humanos, el equipo cartografió cómo la infección interactuaba con las células de soporte locales que normalmente protegen a las neuronas. Astroglía con forma estrellada y células de Müller, así como la microglía —las células “limpiadoras” residentes del cerebro y la retina— se agruparon alrededor de los sitios infectados. Las señales químicas del inflamasoma NLRP3 y sus vías de muerte a valle estuvieron fuertemente elevadas en retinas de personas con Alzheimer, y ya aumentaban en quienes tenían deterioro cognitivo leve. Muchas células infectadas mostraron marcadores tanto de la muerte “pirotótica” inflamatoria como de la apoptosis más clásica. Aunque se reclutó más microglía en las retinas con Alzheimer, cada bacteria pareció ser contactada o engullida por menos microglia que en ojos sanos, lo que sugiere que el sistema de limpieza se sobrecarga o se deteriora a medida que la enfermedad avanza.
Usar el ojo para leer la salud cerebral
Dado que la retina es accesible a imagen de alta resolución en personas vivas, los investigadores preguntaron si medidas retinianas relacionadas con Chlamydia pneumoniae podrían ayudar a predecir el estado del Alzheimer. Utilizaron modelos de aprendizaje automático para combinar niveles de infección retiniana con marcadores como depósitos de amiloide‑beta, inflamación y adelgazamiento local del tejido. Ciertas combinaciones —especialmente bacteria retiniana junto con amiloide— distinguieron a pacientes con Alzheimer de controles con alta precisión y se correlacionaron con la etapa de la enfermedad y las puntuaciones cognitivas. Aunque hacen falta más estudios y de mayor tamaño, los resultados sugieren que una prueba ocular simple podría algún día revelar no solo los cambios clásicos del Alzheimer sino también un componente infeccioso oculto, abriendo la puerta al uso temprano de antibióticos o fármacos que atenúen el inflamasoma en personas en riesgo.
Qué podría significar esto para los pacientes
Para no especialistas, la idea principal es que el Alzheimer puede no estar impulsado únicamente por proteínas que se comportan mal; infecciones de larga duración podrían actuar como gasolina vertida sobre un fuego lento. Este estudio aporta evidencia sólida de que una bacteria respiratoria común puede asentarse en retina y cerebro, provocar inflamación dañina y empeorar la pérdida de memoria en individuos susceptibles. Si futuros ensayos clínicos confirman que tratar tales infecciones o bloquear la vía del inflamasoma ralentiza el declive, la imagenología retiniana de rutina y terapias dirigidas podrían convertirse en parte de un enfoque más proactivo y personalizado para prevenir o retrasar la demencia.
Cita: Gaire, B.P., Koronyo, Y., Vit, JP. et al. Identification of Chlamydia pneumoniae and NLRP3 inflammasome activation in Alzheimer’s disease retina. Nat Commun 17, 771 (2026). https://doi.org/10.1038/s41467-026-68580-4
Palabras clave: Enfermedad de Alzheimer, retina, Chlamydia pneumoniae, neuroinflamación, amiloide‑beta