Clear Sky Science · es
HIF mantiene un circuito regulador transcripcional de la expresión de EPAS1 en carcinoma de células claras renal
Por qué el cáncer de riñón merece una mirada más atenta
El carcinoma de células claras renal es la forma más común de cáncer de riñón, y muchos pacientes reciben ahora fármacos que bloquean una proteína llamada HIF‑2α. Estos medicamentos pueden reducir los tumores, pero no funcionan igual de bien en todos los casos. Este estudio plantea una pregunta simple pero importante: ¿qué hace que algunos tumores renales produzcan tanto HIF‑2α, y puede entender este «interruptor» ayudarnos a predecir quién se beneficiará más del tratamiento y cómo diseñar nuevas terapias?
El sensor de oxígeno que se descontrola
Las células renales sanas usan una proteína de seguridad llamada VHL para mantener los factores sensores de oxígeno, conocidos como HIF, bajo estricto control. Cuando el oxígeno es abundante, VHL marca las proteínas HIF para su degradación, impidiendo que activen genes que fomentan el crecimiento de vasos sanguíneos y la división celular. En el carcinoma claro de riñón, VHL suele perderse o dañarse. Como resultado, un miembro de la familia HIF, HIF‑2α (codificado por el gen EPAS1), escapa a la destrucción y se acumula. Trabajos anteriores mostraron que la alta actividad de HIF‑2α se asocia con crecimiento tumoral más rápido y peores resultados, y que bloquear HIF‑2α puede frenar o detener tumores en algunos pacientes. Sin embargo, los pasos moleculares que aumentan la actividad del gen EPAS1 en los tumores renales no se entendían bien.
Un interruptor de ADN oculto para un gen cancerígeno
Usando muestras tumorales de pacientes, datos de célula única y modelos celulares cancerosos, los autores muestran que el ARN mensajero de HIF‑2α es marcadamente más alto en tumores renales de células claras que en tejido renal normal u otros tipos de tumor renal. Luego exploraron la región de EPAS1 en el genoma en busca de marcas químicas y estructurales que señalen ADN regulador activo. Esto revela un potenciador potente —una especie de interruptor génico a larga distancia— localizado a unos 70.000 nucleótidos aguas arriba de EPAS1 que está específicamente activo en tumores de células claras. En las células tumorales, la cromatina en este potenciador está abierta, decorada con marcas de activación y forma bucles que contactan físicamente el promotor de EPAS1, mientras que en las células tubulares renales normales esta región está en gran medida silente. La actividad en este potenciador se correlaciona con niveles más altos de EPAS1 en grandes conjuntos de datos de cáncer. 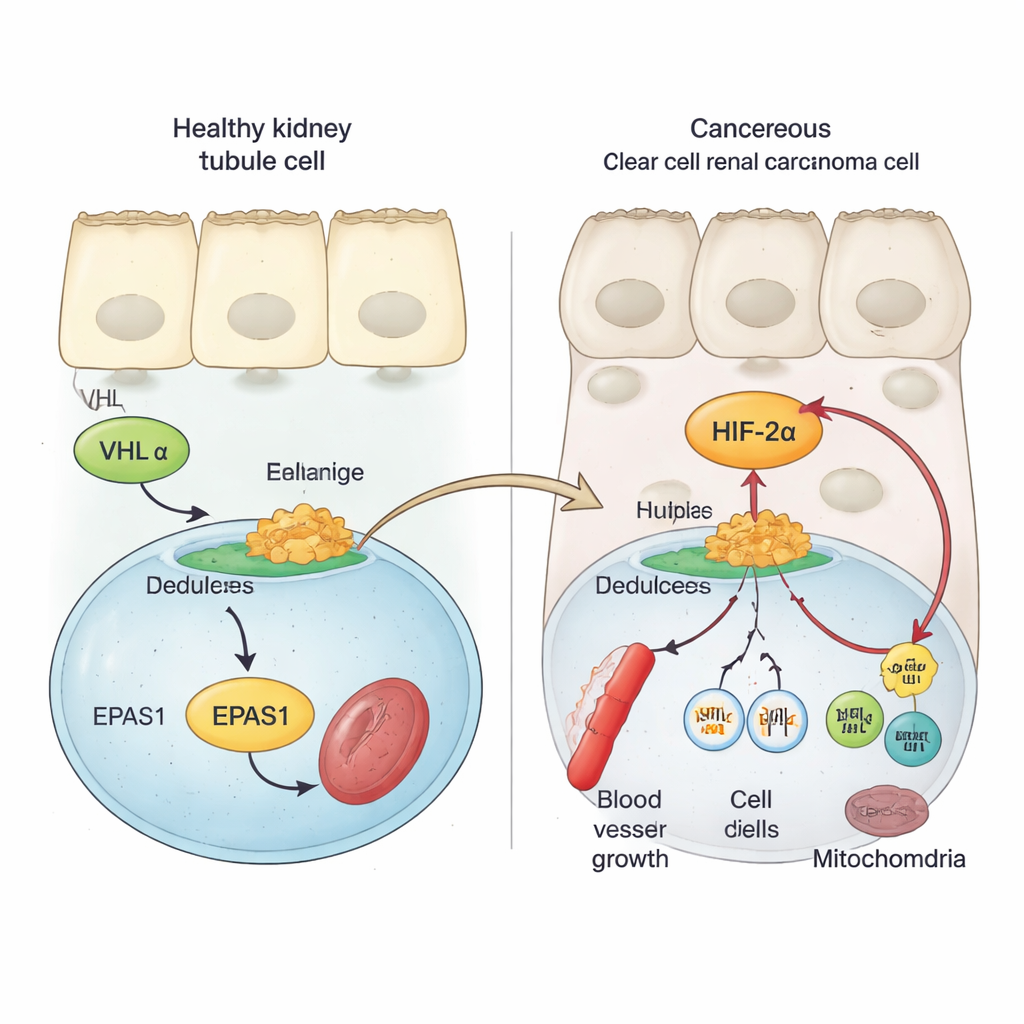
Un circuito autorreforzante impulsado por factores de identidad renal
El estudio encuentra que las proteínas HIF hacen más que responder a la baja disponibilidad de oxígeno: en realidad ayudan a impulsar su propia producción. Cuando los investigadores restauran VHL o eliminan una proteína compañera clave de HIF (HIF‑1β), los niveles de EPAS1 caen y el potenciador se vuelve menos accesible. El mapeo directo de contactos proteína–ADN muestra que HIF se une a dos regiones potenciadoras aguas arriba de EPAS1, incluido el potenciador específico de células claras. En las células tumorales renales, este potenciador también está ocupado por PAX8 y HNF‑1β, factores de transcripción que ayudan a definir la identidad de las células renales y se sabe que apoyan el crecimiento tumoral. Alterar PAX8 o HNF‑1β, o mutar sus sitios de unión dentro del potenciador, reduce el ARN y la proteína de HIF‑2α y debilita la actividad del potenciador. En conjunto, estos hallazgos revelan un circuito autorregulador: HIF‑2α, trabajando con factores de linaje renal, potencia la actividad de un potenciador de EPAS1, que a su vez impulsa una mayor producción de HIF‑2α.
Riesgo genético y comportamiento tumoral convergen en el mismo circuito
La región de EPAS1 ha sido señalada desde hace tiempo en estudios de asociación genómica amplia como un punto caliente para el riesgo de cáncer renal, con ciertas variantes heredadas vinculadas a tasas más altas de cáncer y a mutaciones en VHL en los tumores. Al combinar datos genéticos con mediciones de expresión génica, los autores muestran que las personas portadoras de la versión de alto riesgo de una variante clave de EPAS1 tienden a tener niveles más altos de HIF‑2α en sus tumores — e incluso en células tubulares renales normales cuando HIF se estabiliza experimentalmente. Esto sugiere que las diferencias heredadas en el ADN pueden modular cuán fuertemente responde el potenciador, predisponiendo a algunos riñones a aumentar HIF‑2α con más facilidad una vez que se pierde VHL. Experimentos en células de glioblastoma muestran que el mismo potenciador también puede activarse en ciertos tumores cerebrales, lo que insinúa que este módulo regulador podría reutilizarse en otros cánceres donde HIF‑2α es importante. 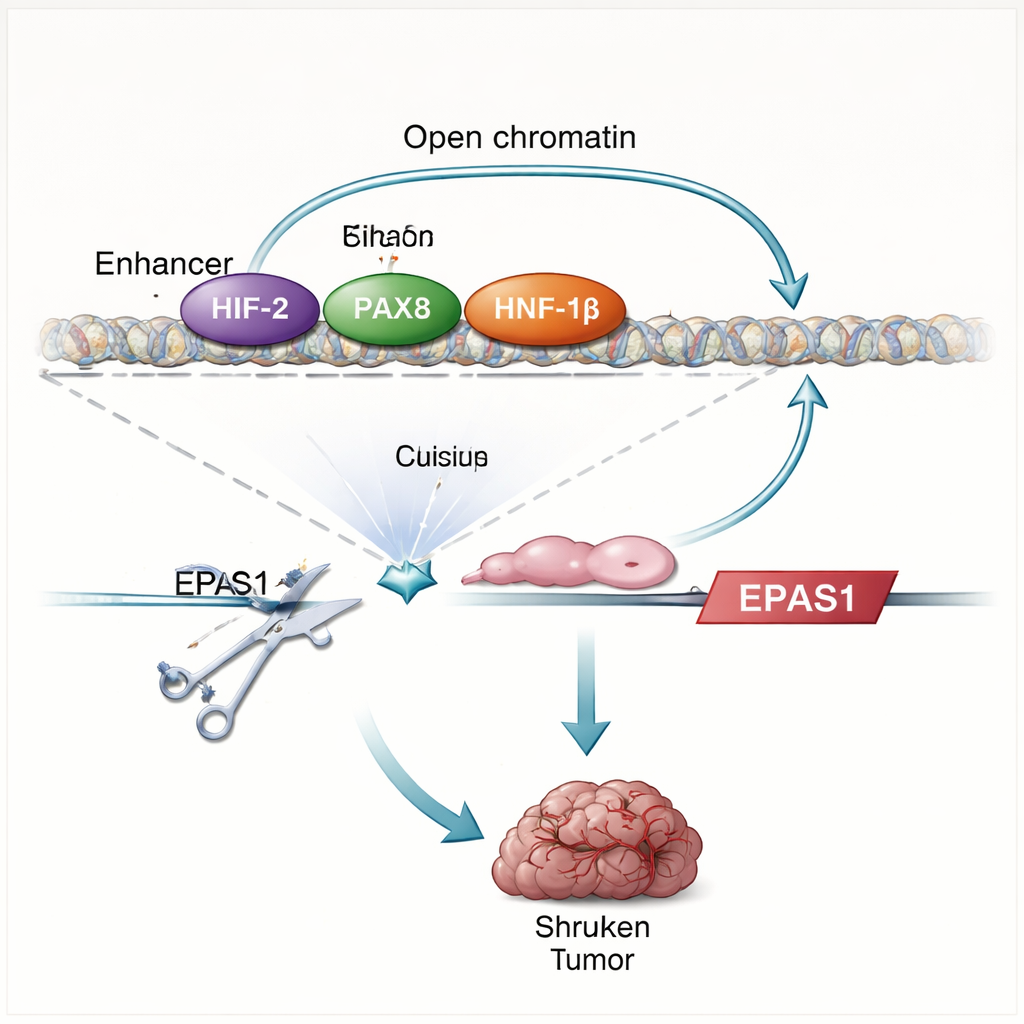
Romper el circuito para detener el crecimiento tumoral
Para probar cuán esencial es este potenciador, el equipo utiliza la edición genómica CRISPR para dañar los motivos de unión de HIF dentro de él en líneas celulares de cáncer renal y en células tumorales frescas de pacientes. Este corte reduce el ARN de HIF‑2α en aproximadamente un tercio a la mitad, disminuye los niveles de genes diana bien conocidos de HIF‑2α como CCND1 y VEGFA, y debilita el programa génico general de hipoxia. Cuando las células editadas se implantan en ratones, en gran medida no logran formar tumores, en marcado contraste con las células control. El patrón de cambios génicos tras la interrupción del potenciador refleja estrechamente los efectos de bloquear directamente HIF‑2α con un fármaco clínico, subrayando que este único elemento de ADN es un impulsor mayor de la vía HIF‑2α en estos cánceres.
Qué significa esto para pacientes y terapias
Para los no especialistas, el mensaje clave es que los autores han descubierto un interruptor de ADN autoamplificante que mantiene encendida una proteína promotora del cáncer importante, HIF‑2α, en los tumores renales de células claras. Este interruptor depende tanto de la pérdida del freno de seguridad VHL como de proteínas auxiliares específicas del riñón, y está influido por variantes genéticas heredadas. Dado que el potenciador está muy activo en muchos tumores de células claras y está estrechamente ligado a la intensidad de la vía HIF‑2α, medir su actividad —o dirigirlo de forma directa— podría ayudar a identificar a los pacientes que más se beneficiarán de los inhibidores actuales de HIF‑2α y ofrecer nuevas maneras de apagar esta vía cuando los tumores desarrollan resistencia a los fármacos.
Cita: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
Palabras clave: carcinoma de células claras renal, HIF-2α, enhancer de EPAS1, mutación VHL, genética del cáncer de riñón