Clear Sky Science · es
Reacción CuAAC interrumpida atroposelectiva usando dietilodonios cíclicos
Por qué importa esta nueva química
Los químicos han confiado durante mucho tiempo en una reacción “click” sencilla para unir bloques moleculares de forma rápida y limpia, un recurso que sostiene desde el descubrimiento de fármacos hasta materiales autorreparables. Este artículo describe una variación ingeniosa de esa reacción clásica que permite a los científicos construir moléculas tridimensionales más complejas con una quiralidad precisa—estructuras muy valoradas en medicamentos modernos y materiales avanzados.
Asignando un nuevo papel a una reacción click clásica
El punto de partida es la cicloadición azida–alquino catalizada por cobre, a menudo llamada simplemente CuAAC. Une dos componentes pequeños—una azida y un alquino—en un anillo de cinco miembros llamado triazol bajo condiciones suaves y con notable fiabilidad. Tradicionalmente, una vez que el cobre ayuda a formar el anillo de triazol, la reacción termina ahí. En los últimos años, sin embargo, los químicos han aprendido a “interrumpir” este proceso, atrapando un intermedio efímero cobre–triazol con un tercer socio para construir productos más elaborados. Hasta ahora, esas interrupciones no habían podido controlar la quiralidad molecular de manera general, lo que limitaba su utilidad para fabricar moléculas quirales sofisticadas.
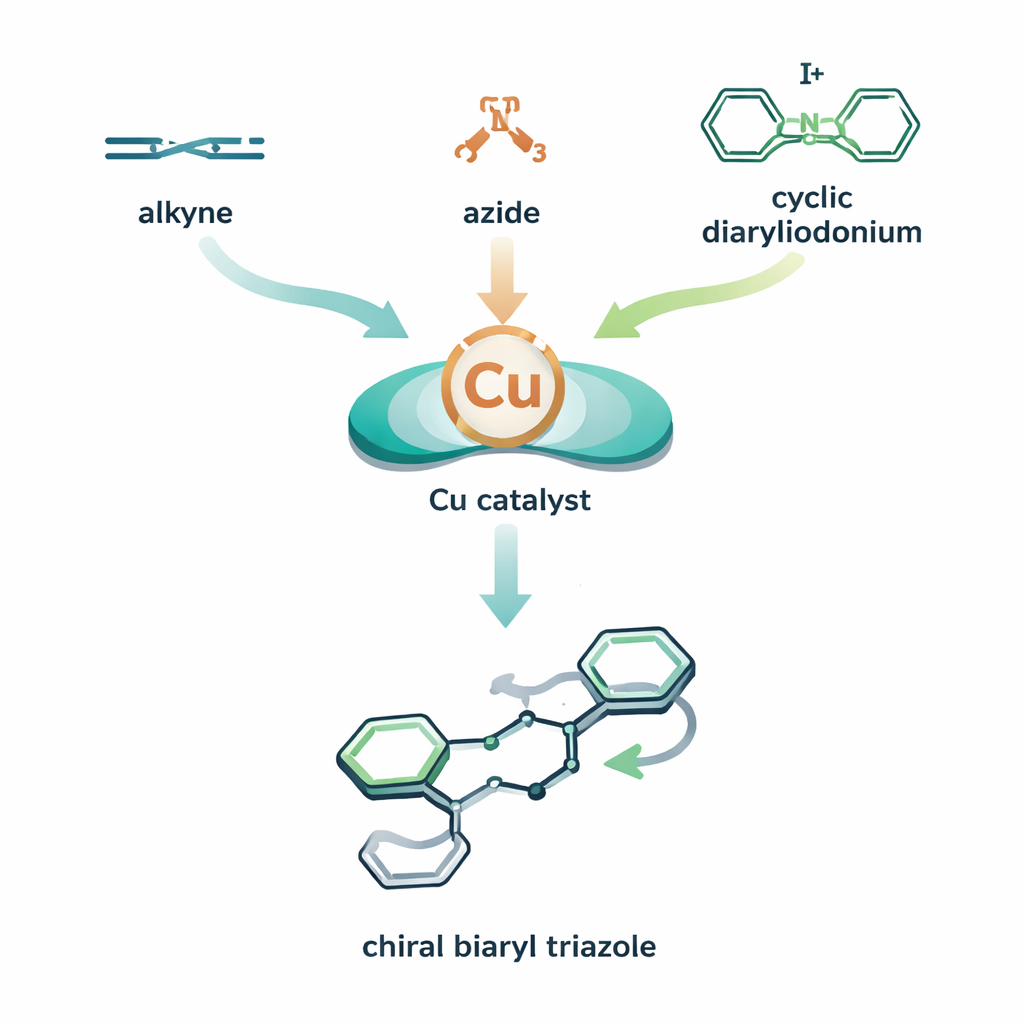
Un rompecabezas molecular de tres piezas con giro
Los autores combinan dos ciclos de reacción basados en cobre en un único proceso orquestado. En su diseño, un catalizador de cobre ayuda primero a que el alquino y la azida formen un intermedio cobre–triazol. Antes de que este intermedio se neutralice, se incorpora un tercer componente—una molécula en forma de anillo, altamente reactiva y que contiene yodo, denominada dietilodonio cíclico. El cobre se inserta en este anillo y luego lo abre, cosiendo uno de sus anillos aromáticos al triazol. El resultado es un triazol biarílico: dos sistemas anulares unidos alrededor de un enlace que puede actuar como un eje quiral, como una hélice que puede girar hacia la izquierda o la derecha. Al emparejar el cobre con un ligando quiral cuidadosamente elegido, el equipo inclina el proceso para que un giro se forme mucho más que el otro, logrando alta atroposelectividad (control sobre qué “mano” axial se genera).
Comprobando cuán flexible y fiable es el método
Para entender cuán general podría ser esta reacción, los investigadores variaron sistemáticamente cada uno de los tres bloques de construcción. Mostraron que muchos alquinos diferentes, incluidos los que llevan anillos ricos en electrones, pobres en electrones y heteroaromáticos, pueden participar y aun así ofrecer buenos rendimientos y fuerte preferencia por una forma quiral. Ciertas sustituciones voluminosas mejoraron la selectividad pero pudieron reducir el rendimiento, revelando un compromiso entre impedimento estérico y eficiencia. Los socios azida funcionaron mejor cuando derivaban de grupos éster o amida simples o de posiciones benzílicas, y una gama de dichas azidas entregó productos quirales altamente enriquecidos. El componente dietilodonio cíclico también se pudo ajustar: algunas sustituciones preservaron tanto el rendimiento como la selectividad, mientras que otras, especialmente cerca del centro reactivo de yodo, ralentizaron la reacción o disminuyeron su desempeño. En conjunto, el estudio proporcionó una amplia colección de nuevos triazoles biarílicos atropoisoméricos accesibles en un solo paso.
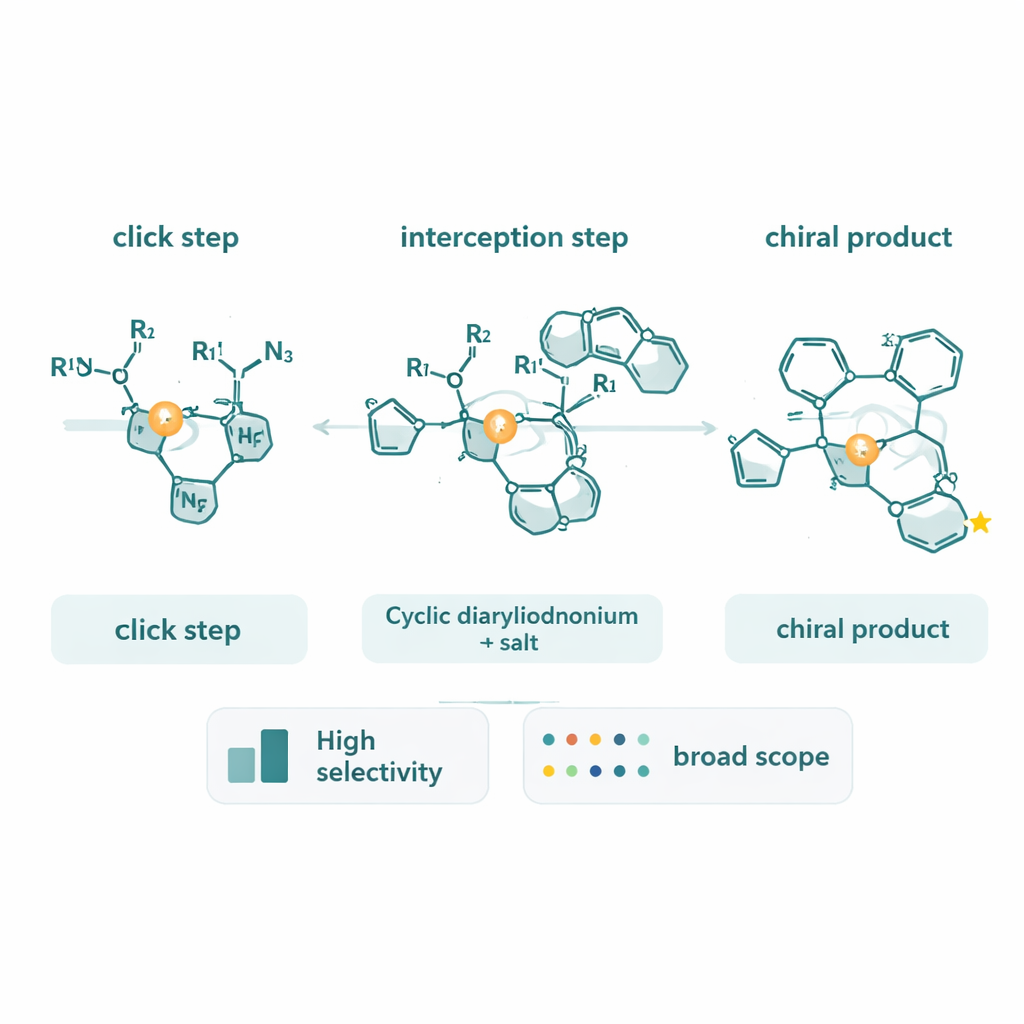
Mirando bajo el capó de la reacción
Más allá de crear nuevas moléculas, el equipo dedicó un esfuerzo sustancial a averiguar cómo funciona realmente la reacción. Usando alcinos marcados con deuterio, observaron un inusual efecto isotópico cinético inverso, que apunta a un paso limitante en el que el carbono del alquino cambia su carácter de enlace en lugar de simplemente romper un enlace C–H. El análisis del progreso de la reacción por calorimetría mostró que la velocidad depende fuertemente de las concentraciones del alquino y la azida, pero solo débilmente del dietilodonio cíclico. Estas mediciones respaldan una imagen en la que la formación y transformación del complejo cobre–triazol, y su adición oxidativa en el anillo del dietilodonio, fijan conjuntamente el ritmo de la reacción. También hallaron que los propios productos triazólicos quirales pueden quedarse adheridos al cobre y enlentecer el catalizador, lo que sugiere vías para optimizar aún más el sistema.
Qué significa esto en el futuro
En términos cotidianos, los investigadores han enseñado a una reacción click bien conocida un truco nuevo: en lugar de simplemente unir dos piezas, ahora ayuda a ensamblar tres componentes en moléculas complejas, con forma de hélice, eligiendo casi exclusivamente una torsión preferida. Esto proporciona una vía escalable hacia triazoles biarílicos quirales, estructuras valiosas como posibles moléculas farmacéuticas, catalizadores y materiales funcionales. Las ideas mecanísticas—especialmente cómo se intercepta el intermedio clave y cómo el producto puede envenenar el catalizador—ofrecen una hoja de ruta para diseñar versiones aún más eficientes y selectivas de esta química. Para los no especialistas, la conclusión clave es que una herramienta molecular tipo “Lego” ya poderosa acaba de volverse más versátil, permitiendo a los químicos construir formas más intrincadas y útiles con un control fino sobre su forma tridimensional.
Cita: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
Palabras clave: química click, catálisis con cobre, biarilo quiral, atropómero, triazol