Clear Sky Science · es
Rompiendo la pared celular para una entrega eficiente de ADN a diatomeas
Algas como pequeñas fábricas verdes
Las diatomeas —algas microscópicas que flotan en los océanos— generan de forma silenciosa aproximadamente una quinta parte del carbono orgánico del planeta, ayudando a alimentar las redes tróficas marinas y a secuestrar dióxido de carbono. Los científicos quieren convertir estos organismos resistentes y de rápido crecimiento en pequeñas fábricas verdes para producir combustibles, alimentos y productos químicos especializados. Pero ha habido un obstáculo importante: resulta sorprendentemente difícil introducir ADN nuevo en las células de diatomeas de manera fiable. Este estudio aborda ese problema práctico directamente, describiendo nuevas formas de introducir instrucciones genéticas y herramientas de edición del genoma más allá de la dura pared exterior de las diatomeas.
Suavizando la concha microbiana del océano
El trabajo se centra en la diatomea modelo Phaeodactylum tricornutum, una favorita en los laboratorios porque su genoma está bien cartografiado y ya dispone de algunas herramientas genéticas básicas. Los autores razonaron que la pared celular, la primera barrera física que debe atravesar cualquier ADN, era un cuello de botella clave. Mediante el tratamiento de las células con una enzima llamada alcalasa, eliminaron parcial o totalmente esta pared, creando «esferoplastos» y «protoplastos» frágiles que son mucho más fáciles de penetrar. Cuando después emplearon electroporación —breves pulsos eléctricos que abren poros temporales—, el número de transformantes exitosos aumentó de forma espectacular, aproximadamente dos órdenes de magnitud en comparación con métodos anteriores. Incluso cantidades minúsculas de ADN, tan bajas como un nanogramo, fueron suficientes para recuperar células modificadas. 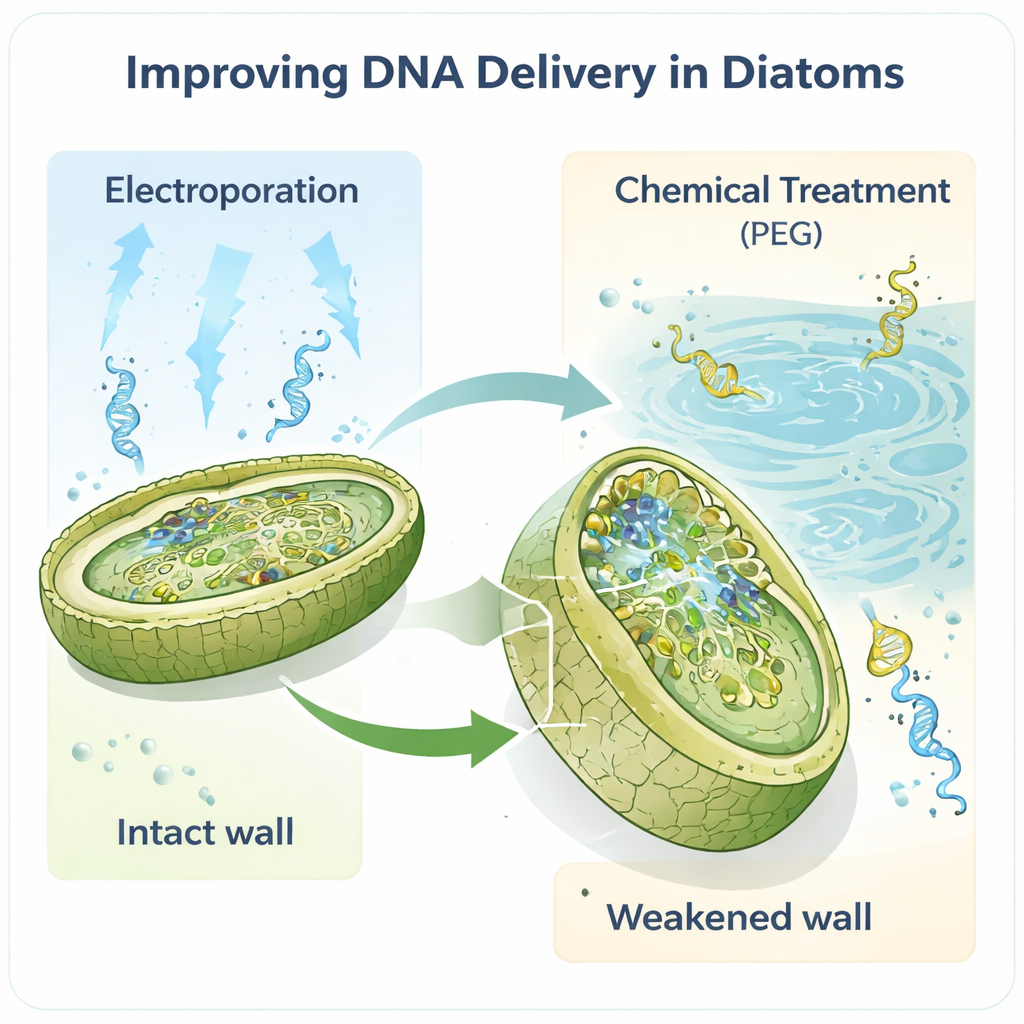
Entrega rápida de ADN sin desvíos por bacterias
Los métodos tradicionales para modificar diatomeas suelen depender de «mensajeros» bacterianos para transportar grandes moléculas circulares de ADN, llamadas episomas, hacia las algas. Aunque efectivo, ese enfoque es lento, técnicamente exigente y puede desestabilizar constructos de ADN delicados. Los nuevos protocolos muestran que tanto la electroporación como un método químico de polietilenglicol (PEG) refinado pueden introducir episomas directamente en las diatomeas, evitando la etapa bacteriana. De forma notable, se entregaron y recuperaron episomas de hasta 55,6 mil pares de bases intactos. Las mismas estrategias funcionaron también en una segunda especie, Thalassiosira pseudonana, que tiene una pared más mineralizada, lo que sugiere que se trata de un conjunto de herramientas de utilidad general y no de un truco aplicable a una sola especie.
Permitiendo que la propia célula construya sus círculos genéticos
Al investigar cómo se comportaba el ADN electroporado dentro de las células, el equipo tropezó con una habilidad sorprendente: las diatomeas pueden coser fragmentos de ADN por sí mismas. Fragmentos lineales de episomas entraron en la célula y se repararon en círculos mediante uniones imprecisas «no homólogas» o mediante una reparación más precisa guiada por solapamientos («dirigida por homología»). Los autores denominaron a este proceso «ensamblaje in vivo en diatomeas», o DIVA. Diseñando fragmentos con solapamientos, indujeron a las células a ensamblar dos, tres o cuatro piezas en episomas completos con altas tasas de éxito, a veces incorporando pequeños casetes sintéticos que añaden etiquetas fluorescentes o nuevas funciones. Esta capacidad convierte al núcleo de la diatomea en un pequeño taller de ADN, potencialmente sustituyendo pasos de ensamblaje laboriosos que habitualmente se realizan en levaduras o en E. coli.
Editar genomas solo con complejos proteicos
Más allá de añadir episomas, los investigadores demostraron que podían entregar complejos proteína‑ARN de CRISPR–Cas9 ya ensamblados directamente en las células de diatomeas usando su método de electroporación optimizado. Dirigidos a un gen llamado PtAPT, que controla la sensibilidad a un análogo tóxico de la adenina, generaron miles de mutantes resistentes sin introducir ADN adicional en el genoma. Muchos de estos mutantes presentaron pequeñas inserciones o deleciones en el sitio diana; algunos incluso capturaron fragmentos de ADN «transportador» que se habían añadido para amortiguar la descarga eléctrica. El equipo combinó luego la entrega de complejos CRISPR y episomas en un solo paso, encontrando que aproximadamente una de cada diez colonias presentaba tanto una edición genómica como un episoma seleccionable: una forma eficiente de rastrear cambios génicos que de otro modo serían invisibles. 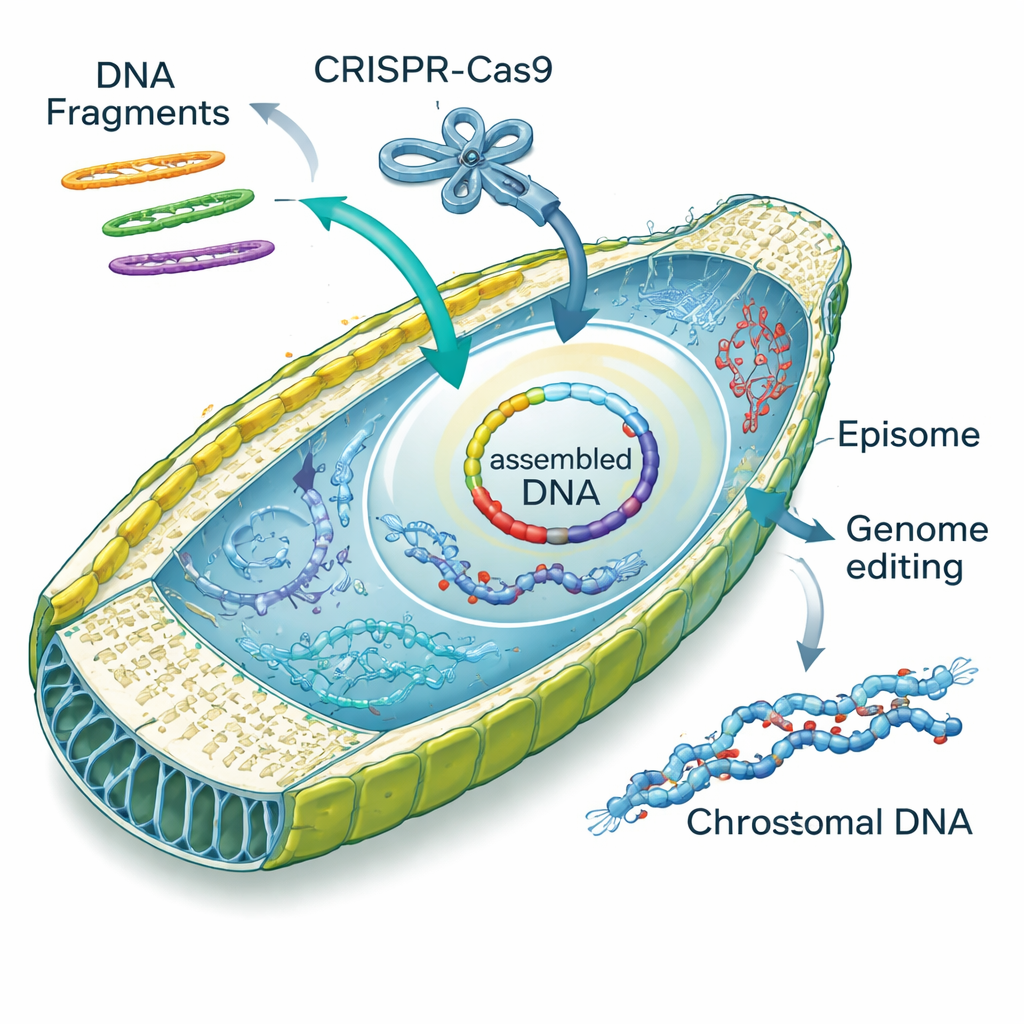
Hacia diatomeas diseñadas para un futuro sostenible
Para el público general, el mensaje clave es que las diatomeas están mucho más cerca de convertirse en organismos prácticos y programables. Al romper o suavizar con delicadeza la pared celular, los autores convirtieron un proceso quisquilloso y de bajo rendimiento en una canalización robusta que usa pequeñas cantidades de ADN, funciona con constructos genéticos grandes e incluso permite que la propia célula ensamble y edite su ADN. Estos avances acortan el camino desde una secuencia diseñada por ordenador hasta una cepa viva y evaluada. A largo plazo, tales herramientas podrían acelerar los esfuerzos para construir diatomeas con cromosomas totalmente sintéticos y para aprovechar estos microbios oceánicos en la producción de combustibles más limpios, química climáticamente más favorable y nuevos descubrimientos biológicos.
Cita: Walker, E.J.L., Pampuch, M., Deng, L. et al. Breaking the cell wall for efficient DNA delivery to diatoms. Nat Commun 17, 1848 (2026). https://doi.org/10.1038/s41467-026-68562-6
Palabras clave: biotecnología de diatomeas, transformación genética, edición genómica CRISPR, biología sintética, ingeniería de microalgas