Clear Sky Science · es
Estructuras de la telomerasa humana unida a nucleótidos en varios pasos de su ciclo de adición repetida de ADN telomérico
Por qué importan los extremos de nuestros cromosomas
Cada vez que una célula se divide, las tapas protectoras en los extremos de nuestros cromosomas —llamadas telómeros— se acortan un poco. Si se hacen demasiado cortas, las células dejan de dividirse o funcionan mal, lo que contribuye al envejecimiento y a enfermedades. Una máquina molecular llamada telomerasa puede reconstruir estas tapas y está inusualmente activa en la mayoría de los cánceres. Este estudio revela, con un detalle sin precedentes, cómo la telomerasa humana agarra y alarga los telómeros paso a paso, ofreciendo pistas sobre cómo algún día podríamos ajustar finamente esta enzima en trastornos relacionados con la edad y en el cáncer.
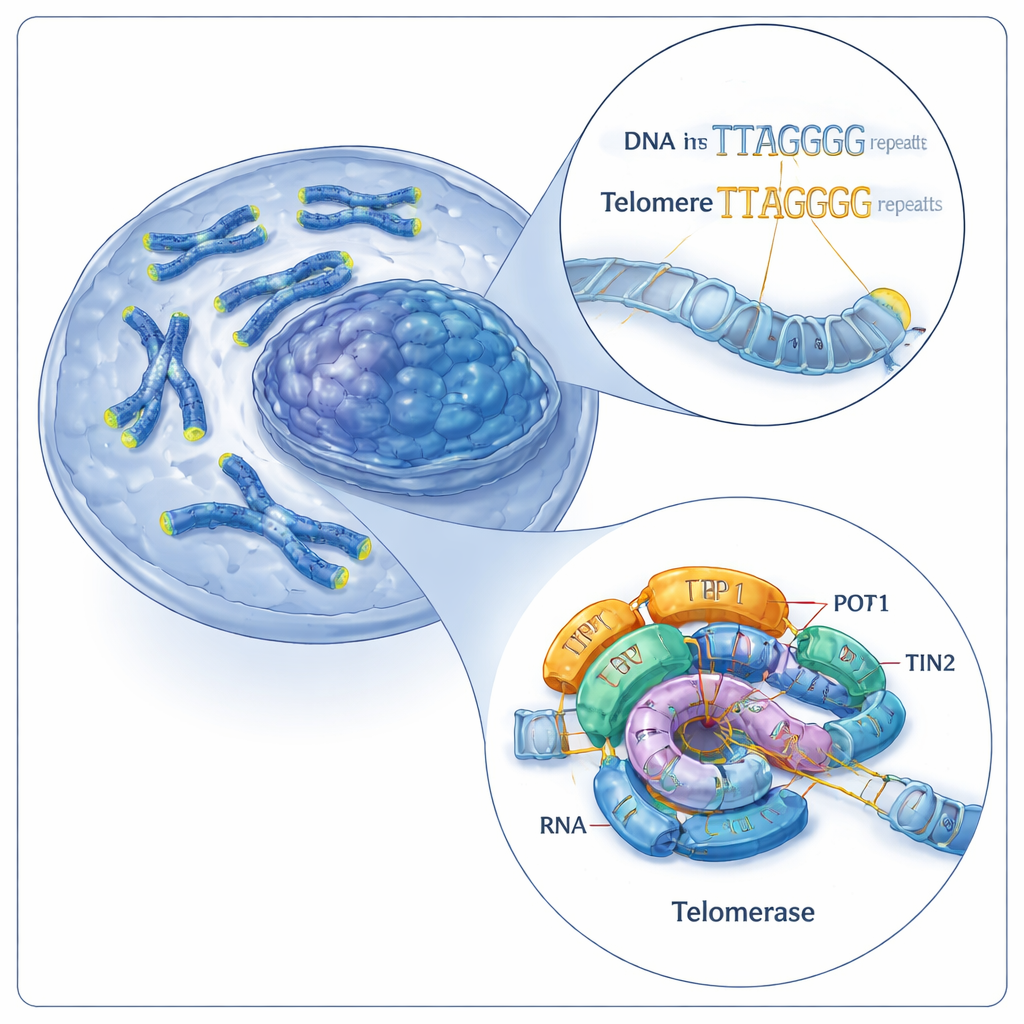
El equipo de reparación de las tapas cromosómicas de la célula
Los telómeros están formados por secuencias cortas y repetidas de ADN (en humanos, un patrón de seis letras: TTAGGG). La telomerasa alarga los telómeros añadiendo más de estas repeticiones en los extremos cromosómicos. Lo hace usando dos partes principales: una proteína llamada telomerasa transcriptasa inversa (TERT) y una molécula de ARN incorporada (hTR) que actúa como plantilla. Juntos, estos componentes forman un núcleo catalítico, al que ayudan proteínas accesorias conocidas como shelterin, que incluyen un trío llamado TPP1–POT1–TIN2. Trabajos previos habían visualizado la telomerasa humana en un solo estado de funcionamiento, dejando abierta una pregunta importante: ¿cómo añade esta máquina repetidamente nuevas repeticiones sin soltarse del ADN?
Congelar la telomerasa en acción
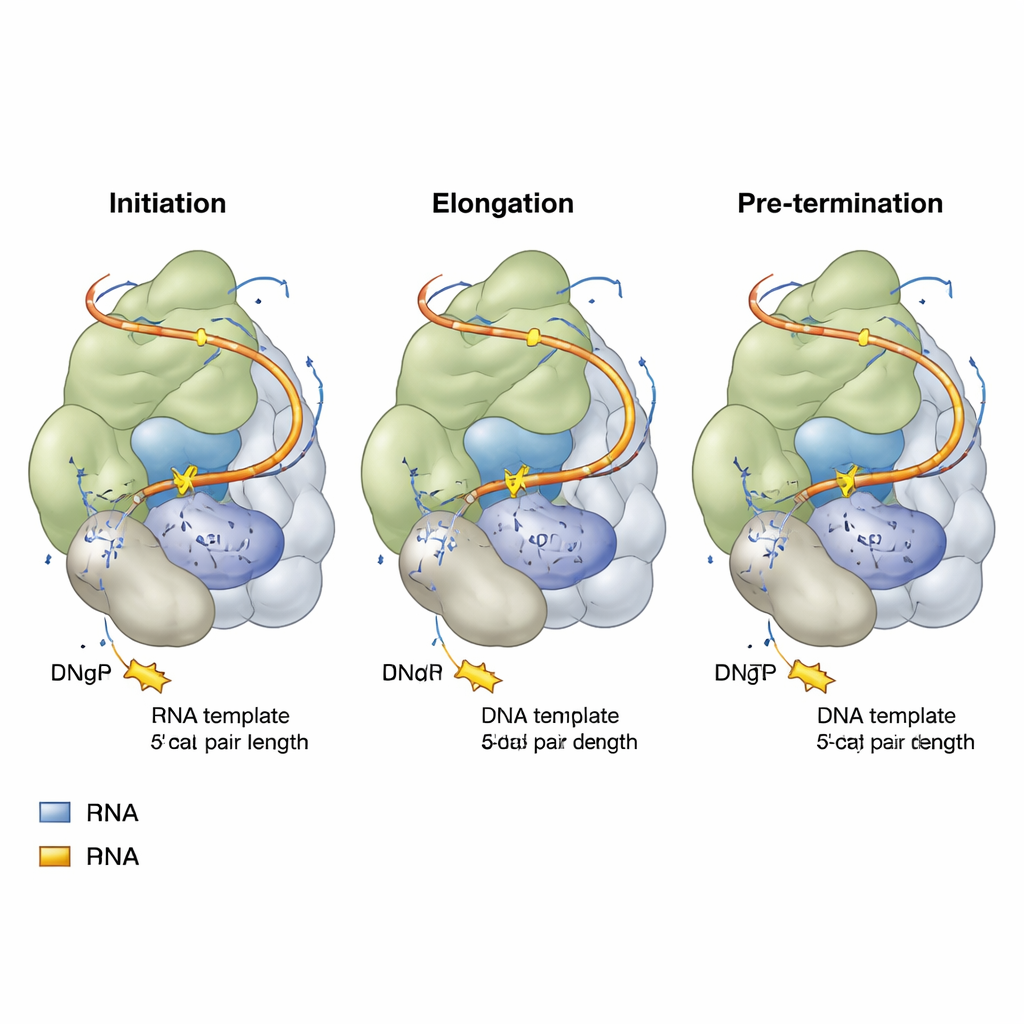
Los investigadores reconstruyeron la telomerasa humana en células humanas y luego la ensamblaron con fragmentos diseñados de ADN telomérico y análogos nucleotídicos no reactivos —moléculas que se parecen a las letras del ADN pero no pueden incorporarse completamente. Usando microscopía crioelectrónica de alta resolución, capturaron instantáneas de la telomerasa en tres etapas clave de su ciclo de adición de repeticiones: el inicio (iniciación), el punto medio de la copia (elongación) y justo antes de completar una repetición (pre‑terminación). Cada instantánea mostró el núcleo catalítico de la telomerasa abrazando un híbrido corto de ADN y ARN, con un nucleótido entrante posado en el sitio activo, listo para añadirse a la cadena de ADN en crecimiento.
Una pequeña cremallera que controla un gran proceso
En las tres etapas surgió un tema sorprendente: el híbrido ADN‑ARN dentro de la telomerasa se mantiene esencialmente de la misma longitud —solo cuatro pares de bases, temporalmente extendido a cinco cuando entra un nuevo nucleótido. Un aminoácido específico en TERT, apodado "cabeza de cremallera", marca consistentemente el extremo de este híbrido corto e impide que crezca más. A medida que se añaden nuevas letras de ADN, un par de bases en el extremo lejano se deshace, de modo que el híbrido nunca se extiende más allá de esta ventana estrecha de cuatro a cinco pares. Este diseño compacto probablemente facilita la separación y el desplazamiento de las hebras, permitiendo que la enzima avance y comience la siguiente repetición sin soltarse completamente del ADN. Diferencias sutiles en qué letras del ADN y del ARN ocupan este corto híbrido explican por qué algunas secuencias terminales teloméricas se unen con más fuerza a la telomerasa que otras.
Enlaces flexibles de ARN y piezas móviles
La plantilla de ARN dentro de la telomerasa no flota libremente; está anclada por tramos flexibles a ambos lados, llamados enlaces de plantilla 5′ y 3′. A medida que la telomerasa avanza desde la iniciación hasta la pre‑terminación, el enlace aguas arriba (5′) se tensa como una cuerda elástica, alcanzando finalmente un estado totalmente estirado que ayuda a señalar el final de una repetición. Mientras tanto, el enlace aguas abajo (3′) se abulta hacia afuera y se aproxima a otra estructura de ARN (la horquilla P6.1) y regiones proteicas cercanas. Si estos enlaces se vuelven demasiado cortos o demasiado largos, o si se altera P6.1, la capacidad de la telomerasa para añadir repetición tras repetición cae drásticamente. Importa también que ciertas regiones proteicas —el dominio TEN y un inserto específico de la telomerasa llamado cuña TRAP— actúan como guías ajustables, contactando tanto el ADN como estos enlaces de ARN. Mutaciones que reducen el volumen de la cuña TRAP pueden, de hecho, hacer que la enzima sea más procesiva, lo que sugiere que esta cuña normalmente actúa como una barrera controlada que temporiza el movimiento de la plantilla.
Nuevas ideas sobre un objetivo terapéutico
Al combinar instantáneas estructurales con pruebas funcionales de mutaciones dirigidas, el estudio propone un modelo mecánico detallado de cómo la telomerasa humana extiende repetidamente los telómeros. La enzima sostiene un híbrido ADN‑ARN muy corto, usa un residuo tipo cremallera para imponer esa longitud y depende de enlaces de ARN flexibles y elementos proteicos móviles para avanzar la plantilla y mantener el ADN anclado durante múltiples rondas de copia. Para no especialistas, el mensaje clave es que la telomerasa no funciona como una máquina de copiar estática sino como un dispositivo finamente ajustado y cargado con resortes cuya geometría y piezas móviles determinan cuánto y con qué eficiencia puede mantener los telómeros. Entender esta coreografía abre la puerta a fármacos que podrían atenuar la telomerasa en cánceres o estabilizar su función en enfermedades de envejecimiento prematuro.
Cita: Balch, S., Franco-Echevarría, E., Ghanim, G.E. et al. Structures of nucleotide-bound human telomerase at several steps of its telomeric DNA repeat addition cycle. Nat Commun 17, 1847 (2026). https://doi.org/10.1038/s41467-026-68560-8
Palabras clave: telomerasa, telómeros, crio‑EM, estabilidad genómica, biología del cáncer