Clear Sky Science · es
Metilación del ADN y lncRNA controlan la replicación asíncrona del ADN en dominios genómicos improntados específicos
Por qué importa el calendario de copiado del ADN de la célula
Cada vez que una célula se divide, debe copiar todo su ADN, pero no todas las regiones se duplican al mismo tiempo. Algunos tramos se copian pronto, otros más tarde, siguiendo un preciso “horario” del genoma. Este artículo explora por qué, en algunos cúmulos genéticos especiales que recuerdan de qué progenitor proceden, las copias materna y paterna se replican en momentos distintos. Comprender este ritmo inusual ayuda a desvelar cómo las marcas químicas en el ADN y los ARN largos no codificantes (lncRNAs) contribuyen a organizar el genoma y pueden influir en el desarrollo y la enfermedad.
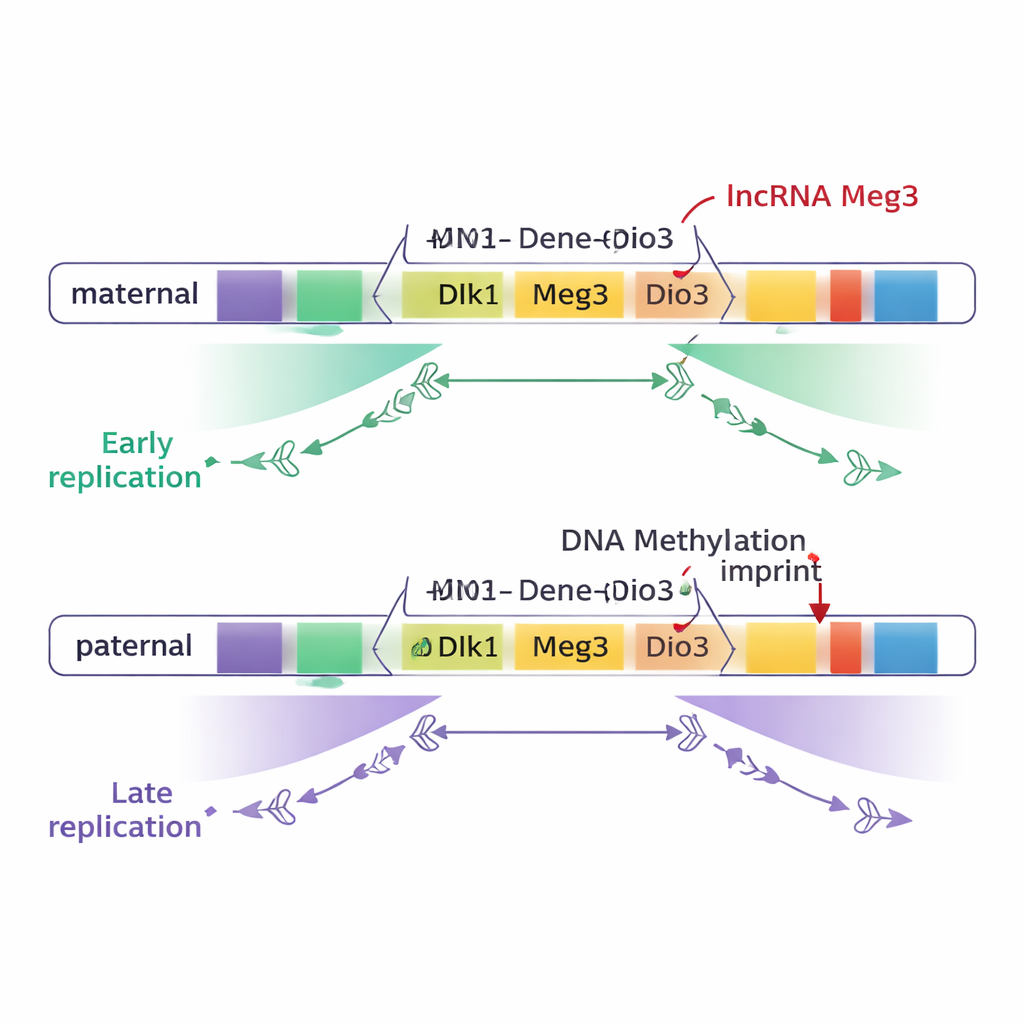
Recuerdos parentales escritos en el ADN
En mamíferos, un pequeño número de dominios genómicos “improntados” se comportan de forma diferente según se hereden de la madre o del padre. Este efecto de origen parental está controlado por la metilación del ADN—pequeñas marcas químicas añadidas en regiones específicas conocidas como regiones diferencialmente metiladas (DMR)—y por cambios en el plegamiento cromosómico. Los autores estudiaron células madre embrionarias de ratón, que se parecen a las células de muy temprano embrión. Compararon células con solo genomas maternos, solo genomas paternos y hibridados normales que llevan uno de cada uno. Siguiendo cuándo se copia cada fragmento de ADN durante el ciclo celular, cartografiaron el momento de replicación a lo largo del genoma y se centraron en regiones improntadas conocidas.
Dos regiones improntadas rompen las reglas
La mayor parte del genoma, incluidas la mayoría de las regiones improntadas, resultó replicarse al mismo tiempo en los cromosomas materno y paterno. Sin embargo, destacaron dos grandes dominios improntados: el dominio Dlk1–Dio3 en el cromosoma 12 y la región Snrpn en el cromosoma 7. En estas zonas, un amplio tramo de ADN—unos tres cuartas partes de millón de pares de bases en Dlk1–Dio3—se copiaba pronto en un cromosoma parental y tarde en el otro. De forma crucial, esta diferencia seguía el origen parental, no la línea genética: la copia materna de genes clave como Dlk1 y del gen lncRNA Meg3 se replicaba de forma consistente pronto, mientras que las copias paternas lo hacían más tarde.
La metilación del ADN fija el interruptor temporal
Para probar qué causa esta diferencia de tiempo, los investigadores diseñaron células madre en las que el patrón normal de metilación en las DMR era borrado o forzado en ambos cromosomas parentales. Cuando ambas copias parentales de las DMR de Dlk1–Dio3 estaban metiladas, toda la región se replicaba tarde en ambos cromosomas. Cuando la metilación se eliminó en gran medida de ambas copias, la misma región se replicó pronto en ambos. Experimentos similares en Snrpn también produjeron la pérdida de las diferencias temporales. Estos resultados muestran que la metilación del ADN específica de cada progenitor es esencial para crear el contraste temprano-versus-tarde entre cromosomas maternos y paternos, al menos en estos dos dominios.
Un ARN largo afinando la replicación temprana
Sin embargo, la metilación del ADN por sí sola no explicaba todo. La región Dlk1–Dio3 también produce un ARN largo no codificante llamado Meg3 como parte de un gran “policistrón” de ARN. En el cromosoma materno, las DMR no metiladas permiten la expresión de Meg3; en el cromosoma paterno, la metilación la mantiene silenciada. Al crear deleciones precisas que apagaban Meg3 pero dejaban intacta la metilación del ADN, los autores mostraron que la pérdida del ARN Meg3 provocaba que partes específicas del dominio materno pasaran de replicarse temprano a hacerlo más tarde. En otras palabras, el ARN Meg3 contribuye a promover la copia temprana en tramos cercanos del cromosoma materno, añadiendo una segunda capa de control además de la metilación del ADN.
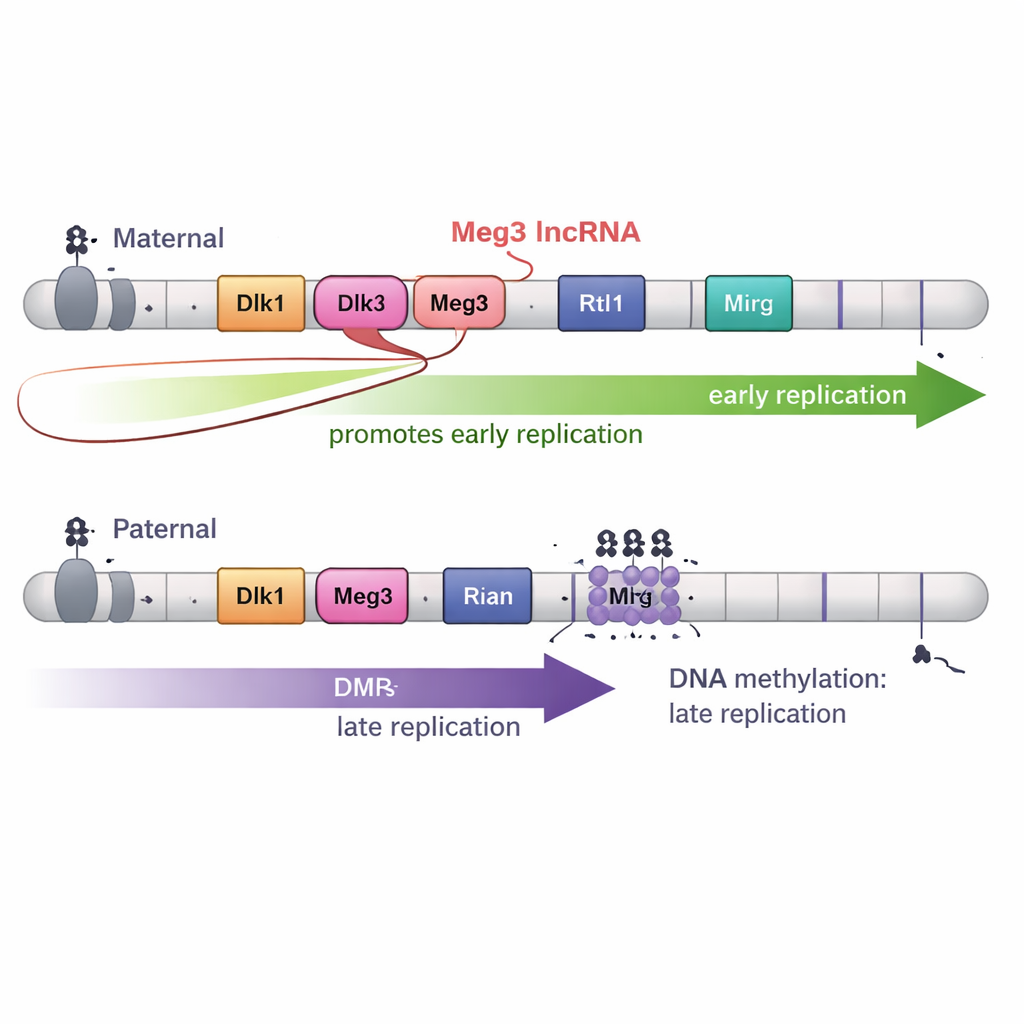
El plegamiento 3D y el desarrollo añaden más matices
Dado que el plegamiento del genoma suele relacionarse con el momento de replicación, el equipo también cartografió la arquitectura cromosómica 3D con gran detalle. Sorprendentemente, en la región Dlk1–Dio3, los bordes de los dominios 3D no coincidían con los límites de replicación temprana y tardía. Incluso cuando se alteraron los patrones de metilación y cambió el tiempo de replicación, las unidades básicas de plegamiento—dominios de asociación topológica—se desplazaron de modos distintos. Finalmente, cuando las células madre se diferenciaron en progenitores neurales, las marcadas diferencias de tiempo entre las copias materna y paterna desaparecieron en gran medida, aunque las marcas de impronta y muchos aspectos de la estructura 3D permanecieron. Esto sugiere que las señales del desarrollo pueden anular el patrón especial temprano-versus-tarde observado en células madre.
Qué significa esto en términos simples
Este estudio revela que, en algunos vecindarios génicos especiales que recuerdan de qué progenitor proceden, el calendario de copiado del ADN de la célula está controlado por una combinación de marcas químicas en el ADN y ARN largos no codificantes. La metilación del ADN en las regiones de control improntadas establece un tiempo básico de temprano o tarde para cada cromosoma parental, y el lncRNA Meg3 empuja además a que el ADN materno cercano se copie antes. Estos efectos actúan en gran medida de forma independiente del plegamiento cromosómico en 3D. Durante el desarrollo, a medida que las células se especializan, este ritmo inusual se desvanece, mostrando que es una característica del estado pluripotente de las células madre. En conjunto, el trabajo explica cómo las “memorias” epigenéticas parentales y los ARN no codificantes pueden anular localmente el horario habitual de replicación del genoma.
Cita: Imaizumi, Y., Charon, F., Surcis, C. et al. DNA methylation and lncRNA control asynchronous DNA replication at specific imprinted gene domains. Nat Commun 17, 1844 (2026). https://doi.org/10.1038/s41467-026-68558-2
Palabras clave: impronta genómica, metilación del ADN, sincronización de la replicación, ARN largo no codificante, células madre embrionarias