Clear Sky Science · es
La activación microbiana del GLP-2R mitiga la inflamación gastrointestinal
Por qué importa una proteína amigable para el intestino
Mientras el mundo busca formas sostenibles de alimentar a una población en crecimiento, los científicos miran más allá de granjas y campos hacia grandes tanques de acero que cultivan microbios para alimento. Este estudio explora si una de esas proteínas de origen microbiano puede hacer algo más que nutrirnos. Los investigadores se preguntaron: ¿puede una proteína derivada de bacterias inofensivas tanto cubrir necesidades dietéticas como proteger activamente el intestino frente a la inflamación, un problema central en afecciones como la enfermedad inflamatoria intestinal y el daño intestinal inducido por quimioterapia?
Un nuevo tipo de proteína procedente de microbios
La proteína en el centro de este trabajo proviene de una bacteria del suelo llamada Methylococcus capsulatus Bath (McB). En lugar de consumirse como bacterias vivas, McB se procesa en un lisado microbiano —esencialmente una mezcla pulverizada de células bacterianas rotas— producido comercialmente bajo el nombre FeedKind®. Se alimentó a los ratones con dietas en las que este lisado suministraba la mayor parte de la proteína, ya fuera en una dieta simple o en una dieta “compleja” más parecida a la humana. El equipo siguió entonces cómo esa dieta cambió la composición de los microbios intestinales, las células inmunitarias que patrullan el intestino y la capacidad del intestino para resistir distintos tipos de lesión.
Reconfigurando el vecindario microbiano
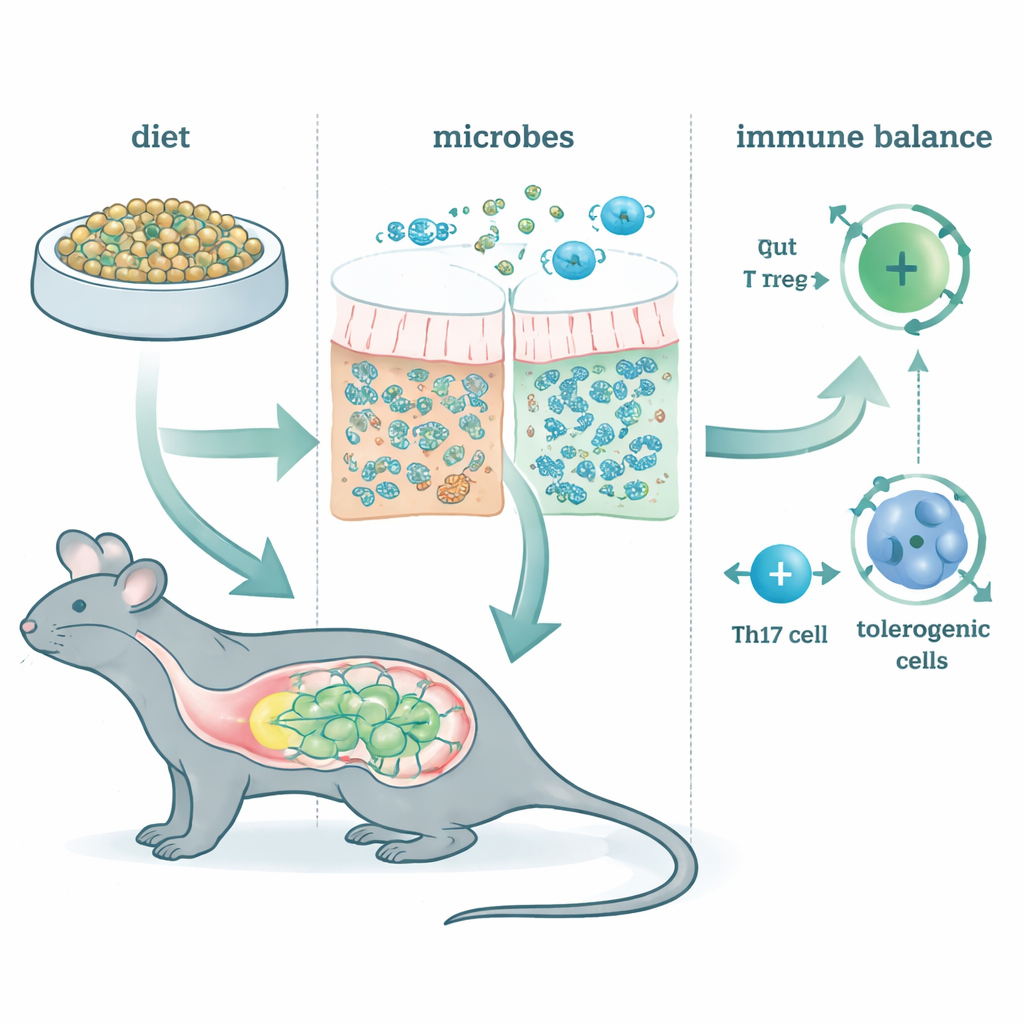
La alimentación con McB alteró rápida y persistentemente la microbiota intestinal, independientemente de la dieta de fondo que consumieran los animales. Solo una fracción mínima de McB apareció en las heces, lo que indica que el material se aprovechó casi por completo en el intestino. En su lugar, prosperó un puñado de especies bacterianas de familias como Lachnospiraceae y Bacteroidaceae. Los análisis genéticos mostraron que estas comunidades estaban enriquecidas en vías de fermentación que producen ácidos grasos de cadena corta —pequeñas moléculas ya conocidas por nutrir las células intestinales e influir en la inmunidad. En otras palabras, McB actuó menos como una proteína convencional y más como un combustible dirigido que remodela la actividad de los microbios residentes.
Enseñando al sistema inmunitario a tolerar
Los autores examinaron a continuación tipos clave de células T que ayudan a decidir si el intestino reacciona con calma o con agresividad a lo que pasa por él. Un grupo, las células T reguladoras inducidas periféricamente (pTregs), ayuda a prevenir la sobrerreacción ante alimentos y microbios amistosos. Otro grupo, las células Th17, puede o bien impulsar inflamación dañina o contribuir al mantenimiento de una barrera saludable, según su “estado”. La alimentación con McB aumentó de forma marcada las pTregs a lo largo de todo el intestino, incluso cuando la mayor parte de los microbios intestinales fueron eliminados con antibióticos. En contraste, los efectos de McB sobre las células Th17 dependieron de la presencia y la función normal de las bacterias intestinales. En ratones con microbiota intacta, McB inclinó a las Th17 hacia un estado más calmante, productor de IL‑10 y menos inflamatorio. Cuando se bloqueó la fermentación, ese cambio tolerogénico desapareció, subrayando que McB actúa en parte reruteando las conversaciones entre microbios e inmunidad.
Protegiendo el intestino durante la lesión
Para ver si estos cambios se traducían en protección real, los investigadores desafiaronn a los ratones con dos agresiones intestinales severas. Una fue un fármaco de quimioterapia, 5‑fluorouracilo, que causa daño generalizado y acortamiento de las vellosidades en forma de dedo que absorben nutrientes. La otra fue un químico (DSS) que desencadena colitis, un modelo de inflamación del intestino grueso. Los ratones con la dieta McB perdieron menos peso, mantuvieron vellosidades y longitud de colon mayores, mostraron menos lesiones sangrantes y tuvieron puntuaciones de daño microscópico más bajas en ambos modelos. Estos beneficios persistieron incluso cuando las células T CD4 fueron eliminadas experimentalmente, lo que sugiere que las acciones protectorass de McB no se deben únicamente a células inmunitarias adaptativas sino que también implican efectos directos sobre el revestimiento intestinal.
Un receptor hormonal, pero sin hormona adicional
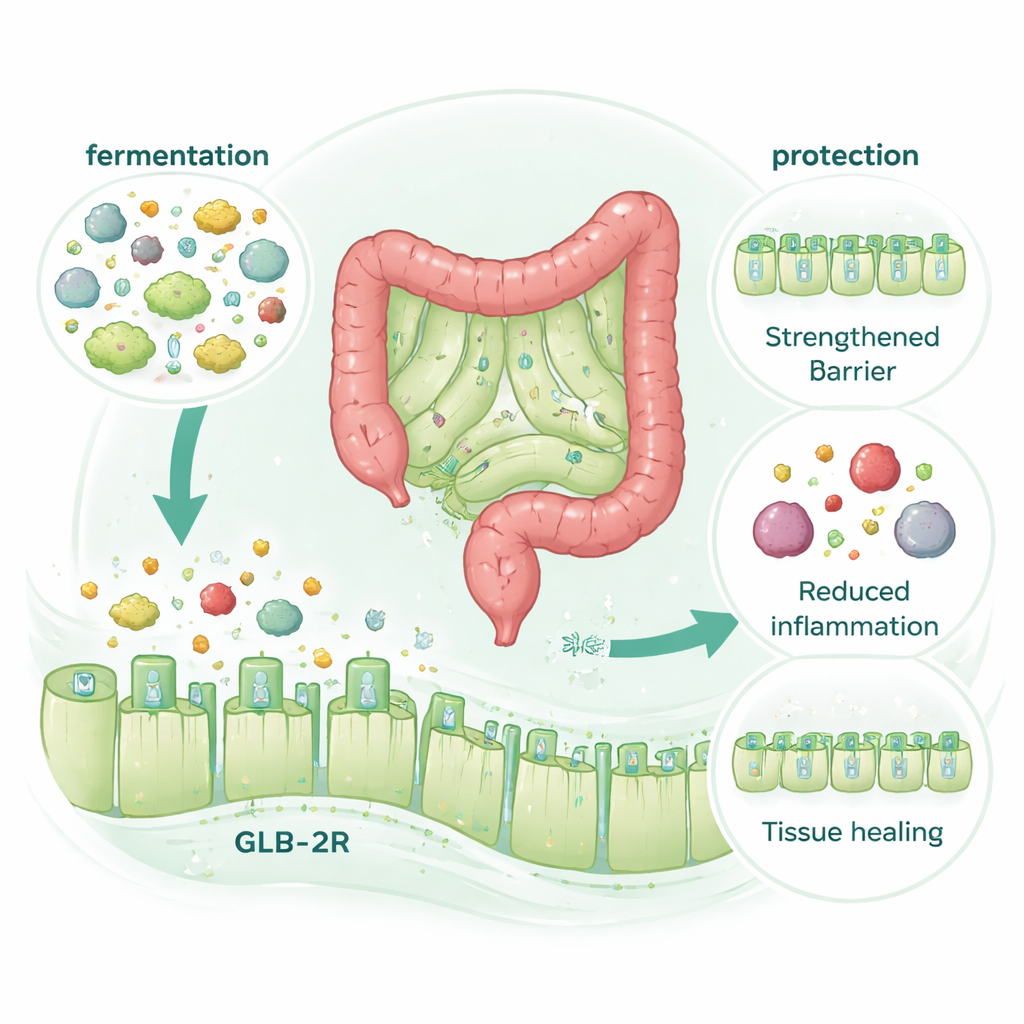
Un giro sorprendente fue el descubrimiento de que el efecto protector de McB requería absolutamente el receptor intestinal de una hormona promotora de la reparación llamada GLP‑2 (el receptor GLP‑2, o GLP‑2R), pero no el receptor relacionado GLP‑1. Cuando los ratones carecían de GLP‑2R, McB dejó de protegerlos del daño por quimioterapia o colitis. Sin embargo, McB por sí mismo no aumentó los niveles de GLP‑2 en sangre, incluso cuando la digestión y la degradación hormonal se controlaron cuidadosamente. En cambio, los beneficios desaparecieron cuando la fermentación microbiana en el colon fue bloqueada químicamente, aunque la composición global de la microbiota cambiara muy poco. Esto apunta a un mecanismo en el que la degradación microbiana de McB genera pequeños compuestos que actúan como “miméticos” de GLP‑2, activando su receptor para fortalecer la barrera y promover la reparación sin liberación adicional de la hormona.
Qué podría significar esto para los alimentos del futuro
Para un lector profano, la conclusión es que algunas fuentes de proteína del futuro podrían diseñarse no solo para ser climáticamente favorables, sino también para apoyar activamente la salud intestinal. En ratones, un lisado de McB escalable comercialmente reorientó la inmunidad hacia la tolerancia y ayudó al intestino a soportar lesiones graves mediante dos vías parcialmente independientes: un aumento directo de las células T reguladoras y una activación del receptor GLP‑2 impulsada por la fermentación que favorece la reparación tisular. Aunque aún hacen falta estudios en humanos, el trabajo sugiere que las proteínas de origen microbiano podrían formar una nueva clase de alimentos “inteligentes”: capaces de alimentarnos, colaborar con nuestros propios microbios y reforzar discretamente las defensas naturales del intestino contra la inflamación.
Cita: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
Palabras clave: inflamación intestinal, proteína microbiana, microbioma, receptor de GLP-2, células T reguladoras