Clear Sky Science · es
FUNDC1 endotelial regula la reprogramación metabólica y la transición obesidad-diabetes a través del eje SIRT3/GATA2/endotelina-1
Por qué importan las células de los vasos sanguíneos en la obesidad y la diabetes
La obesidad y la diabetes tipo 2 suelen atribuirse al tejido adiposo, al hígado o al páncreas. Pero este estudio revela un culpable sorprendente: la delgada capa de células que recubre nuestros vasos sanguíneos, llamadas células endoteliales. Los investigadores muestran que una pequeña proteína mitocondrial en estas células, denominada FUNDC1, puede ayudar a impulsar al organismo desde una simple ganancia de peso hacia una diabetes completa al cambiar la manera en que los vasos se comunican con los órganos metabólicos.
Estrés en la “piel” interna del cuerpo
Las células endoteliales forman una vasta y delicada red que controla el flujo sanguíneo, la entrega de nutrientes y las señales hacia los tejidos cercanos. En condiciones sanas equilibran factores relajantes, como el óxido nítrico, con factores constrictores, como la endotelina-1 (ET-1). En la obesidad y en las fases iniciales de la diabetes, este equilibrio se inclina hacia ET-1, que no solo estrecha los vasos sino que también altera cómo las células de grasa, músculo e hígado manejan el azúcar y las grasas. Los autores empezaron mostrando en ratones que la disfunción vascular aparece tras solo dos meses con una dieta alta en grasas, antes de que se desarrolle una resistencia a la insulina clara, lo que sugiere que el endotelio dañado puede ayudar a desencadenar la enfermedad metabólica en lugar de limitarse a responder a ella.
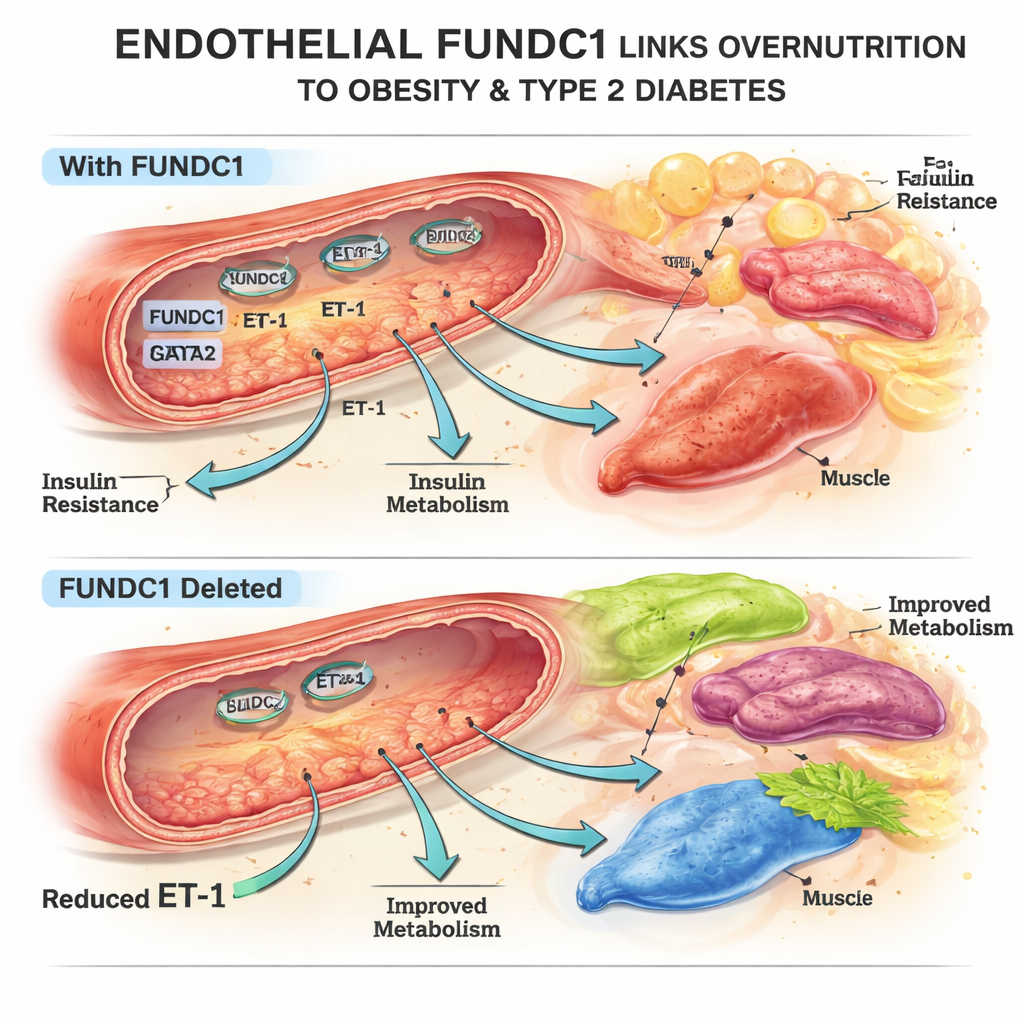
Un interruptor mitocondrial que moldea la grasa corporal
El equipo se centró en FUNDC1, una proteína en la superficie de las mitocondrias, las fábricas de energía de la célula. En células endoteliales de ratón y humano expuestas a exceso de grasa, los niveles de FUNDC1 cambiaron con el tiempo: disminuyeron al principio y luego aumentaron de forma marcada con la sobrealimentación prolongada. Usando ratones genéticamente modificados que carecen de FUNDC1 únicamente en las células endoteliales, los investigadores descubrieron que estos animales estaban parcialmente protegidos contra la ganancia de peso por dieta alta en grasas, tenían menos grasa corporal, adipocitos más pequeños y mejor control de la glucemia. Sus tejidos adiposo, hepático y de grasa parda respondían con mayor fuerza a la insulina, aunque los niveles de insulina no eran más altos. Estos cambios no podían explicarse por diferencias en la ingesta de alimento o la actividad, apuntando en cambio a la influencia del sistema vascular sobre el metabolismo.
Un mensajero químico que provoca resistencia a la insulina
Para averiguar cómo FUNDC1 endotelial afecta a órganos distantes, los autores cribaron varias sustancias secretadas por las células endoteliales. Una destacó: la ET-1. Cuando se eliminó FUNDC1 en las células endoteliales, la producción de ET-1 en los vasos y en la circulación descendió notablemente, tanto en condiciones normales como con dieta alta en grasas. Experimentos en cultivos de adipocitos, hepatocitos y células musculares mostraron que la ET-1 promovía el crecimiento de preadipocitos, alteraba el almacenamiento y la degradación de grasa y agravaba la acumulación de lípidos en hígado y músculo expuestos a alta grasa —un patrón conocido por fomentar la resistencia a la insulina. En ratones vivos, la infusión de ET-1 al inicio de una dieta alta en grasas borró los beneficios protectores de la deleción de FUNDC1 endotelial: el peso corporal, la masa grasa, el control de la glucemia y la función vascular empeoraron, subrayando a la ET-1 como un vínculo clave entre el endotelio y la enfermedad metabólica.
Un eje de señalización interno: FUNDC1, SIRT3 y GATA2
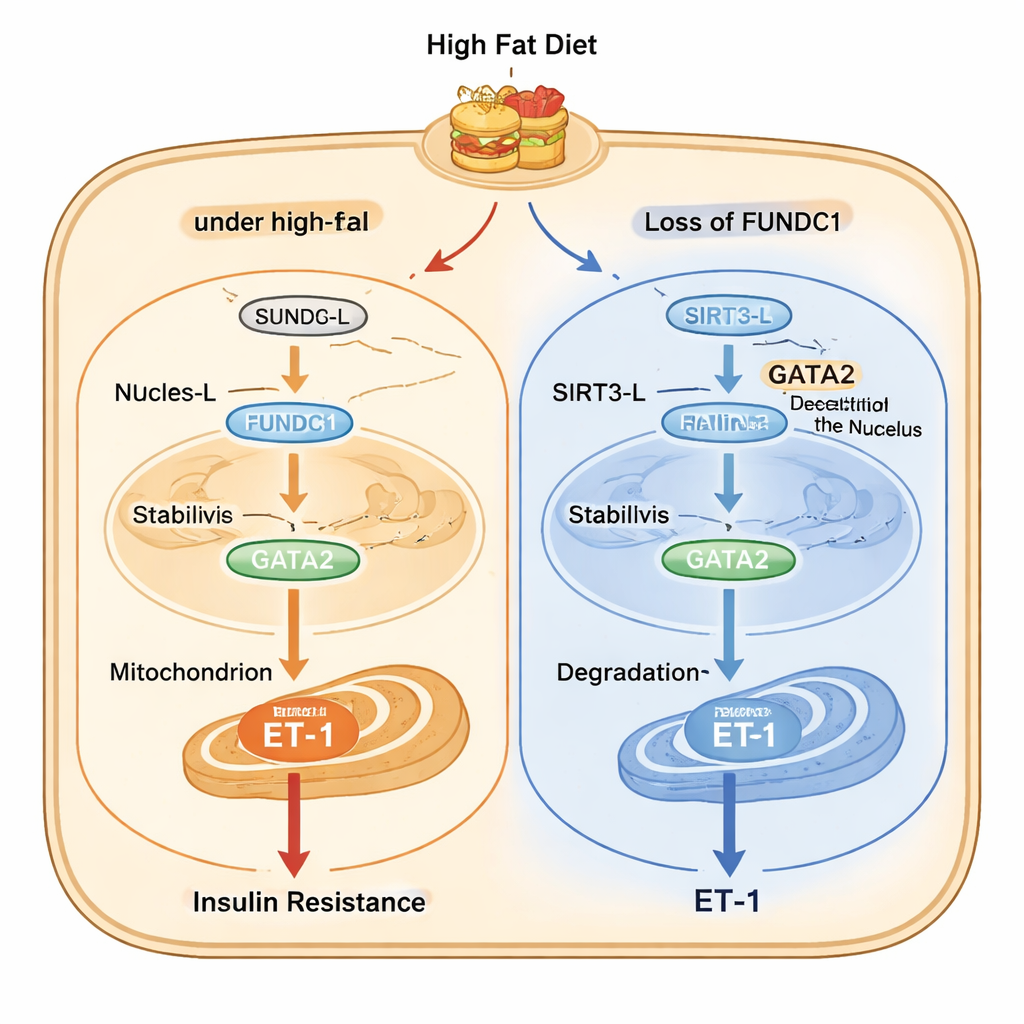
El estudio traza a continuación una cadena molecular detallada dentro de las células endoteliales. Bajo estrés por alta grasa, una forma larga de la enzima SIRT3 (SIRT3-L), que puede residir tanto en el núcleo como en las mitocondrias, se desplaza desde el núcleo hacia las mitocondrias con la ayuda de FUNDC1 y de una proteína chaperona llamada HSC70. Una vez secuestrada en las mitocondrias, hay menos SIRT3-L disponible en el núcleo para eliminar grupos acetilo de GATA2, un factor de transcripción que aumenta la actividad del gen de ET-1. GATA2 más acetilada es más estable y promueve mayor producción de ET-1. Cuando FUNDC1 está ausente, SIRT3-L permanece en el núcleo, donde desacetila a GATA2, lo que conduce a la degradación de GATA2 y a una menor producción de ET-1. De forma intrigante, SIRT3 a su vez favorece la degradación de FUNDC1, creando un circuito de retroalimentación que normalmente modera la vía pero que se desregula durante la sobrealimentación crónica.
De modelos en ratón a la enfermedad humana
Para comprobar si este mecanismo tiene relevancia en personas, los investigadores examinaron sangre y pequeñas arterias de individuos con obesidad y diabetes tipo 2 y de voluntarios sanos. Los pacientes con ambas condiciones presentaban niveles sanguíneos más altos de ET-1 y mayor expresión de FUNDC1, GATA2 y del gen de ET-1 en el revestimiento de sus vasos. La cantidad de ET-1 en sangre se relacionó estrechamente con el índice de masa corporal y la glucemia a largo plazo (HbA1c), y los niveles del gen ET-1 en los vasos correlacionaron fuertemente con FUNDC1 y GATA2. Estos patrones reflejan los hallazgos en ratones y respaldan la idea de que un eje FUNDC1–SIRT3–GATA2–ET-1 hiperactivo actúa en el tejido vascular humano bajo estrés metabólico.
Un nuevo blanco en la lucha contra la diabetes
Para el público general, el mensaje central es que el daño por exceso de comida puede manifestarse primero en las células que recubren los vasos sanguíneos. Allí, una proteína mitocondrial, FUNDC1, ayuda a desviar una enzima reguladora, SIRT3, fuera del núcleo, permitiendo que otro factor, GATA2, aumente la producción de ET-1, una señal con efecto hormonal que promueve tanto el endurecimiento vascular como la resistencia a la insulina. Bloquear esta vía —reduciendo la actividad de FUNDC1 endotelial o atenuando la ET-1— podría ayudar a prevenir la transición de la obesidad a la diabetes y, al mismo tiempo, proteger los vasos sanguíneos.
Cita: Li, J., Li, D., Zhao, F. et al. Endothelial FUNDC1 regulates metabolic reprogramming and the obesity-diabetes transition through the SIRT3/GATA2/endothelin-1 axis. Nat Commun 17, 1836 (2026). https://doi.org/10.1038/s41467-026-68548-4
Palabras clave: células endoteliales, mitocondrias, endotelina-1, obesidad, diabetes tipo 2